Mini-Batteri, Maxi-Messaggi: Le Sorprendenti Vescicole dei Mollicutes
Ciao a tutti! Oggi voglio portarvi con me in un viaggio affascinante nel mondo microscopico, alla scoperta di creature tanto piccole quanto potenti: i Mollicutes. Immaginate batteri così minimalisti da aver rinunciato persino alla parete cellulare, una caratteristica quasi universale nel regno batterico. Sono tra gli organismi più piccoli capaci di vita autonoma, ma non lasciatevi ingannare dalle dimensioni ridotte! Questi esserini pleomorfi, cioè capaci di cambiare forma, hanno sviluppato strategie incredibilmente sofisticate per interagire con l’ambiente e con i loro ospiti, spesso causando malattie in animali e piante.
Messaggeri Nascosti: Le Vescicole Extracellulari (EVs)
Una delle scoperte più intriganti degli ultimi anni riguarda un modo tutto particolare che i batteri, inclusi i nostri Mollicutes, usano per comunicare e influenzare ciò che li circonda: le vescicole extracellulari, o EVs (Extracellular Vesicles). Pensatele come piccole “bolle” o pacchetti che si staccano dalla membrana della cellula batterica e viaggiano all’esterno, portando con sé un carico prezioso. Questo carico può includere proteine, lipidi, acidi nucleici (come DNA e RNA) e altre molecole.
Nel mondo batterico, queste EVs sono dei veri e propri tuttofare: aiutano a eliminare scarti, a catturare nutrienti, a difendersi da antibiotici o attacchi, a comunicare tra batteri e persino a interagire con le cellule dell’ospite, modulando la risposta immunitaria o consegnando fattori di virulenza. Nei batteri Gram-negativi, queste vescicole si formano dalla membrana esterna, mentre nei Gram-positivi (gli antenati dei Mollicutes) derivano dalla membrana citoplasmatica.
Sebbene sapessimo da tempo che anche alcuni Mollicutes producono EVs (le prime osservazioni risalgono agli anni ’70!), mancava una comprensione profonda della loro composizione e, soprattutto, della loro funzione. Cosa c’è dentro queste mini-vescicole? E cosa fanno esattamente? Queste sono le domande che hanno guidato la ricerca di cui vi parlo oggi.
La Sfida dell’Isolamento e l’Analisi del Contenuto
Studiare le EVs dei Mollicutes non è una passeggiata. La loro piccola taglia (tra 100 e 800 nanometri) e l’assenza di parete cellulare rendono difficile separare le vescicole dalle cellule batteriche stesse, che sono così piccole e flessibili da poter passare attraverso filtri che normalmente bloccherebbero altri batteri (come quelli da 0.22 µm). Per superare questo ostacolo, abbiamo dovuto mettere a punto un protocollo di isolamento più stringente, utilizzando filtrazioni seriali fino a pori di 0.1 µm, seguite da ultracentrifugazione per concentrare le vescicole.
Anche l’osservazione e la quantificazione si sono rivelate complesse. Tecniche come la Nanoparticle Tracking Analysis (NTA), che funziona bene per altre EVs, faticavano a distinguere le vescicole dal “rumore di fondo” del terreno di coltura. Tuttavia, grazie alla microscopia elettronica a trasmissione (TEM), siamo riusciti a visualizzare queste sfere membranose che gemmano dalle cellule di Mycoplasma mycoides subsp. capri (Mmc) e Mycoplasma bovis, due importanti patogeni veterinari.
E il contenuto? L’analisi proteomica (lo studio su larga scala delle proteine) ha rivelato qualcosa di fondamentale: le proteine trovate nelle EVs sono in gran parte un riflesso del proteoma della cellula madre. È come se la vescicola fosse uno specchio in miniatura della composizione proteica del batterio che l’ha prodotta. Abbiamo trovato proteine di membrana, citoplasmatiche ed extracellulari, con una leggera abbondanza maggiore di proteine di membrana nelle EVs rispetto alle cellule intere.
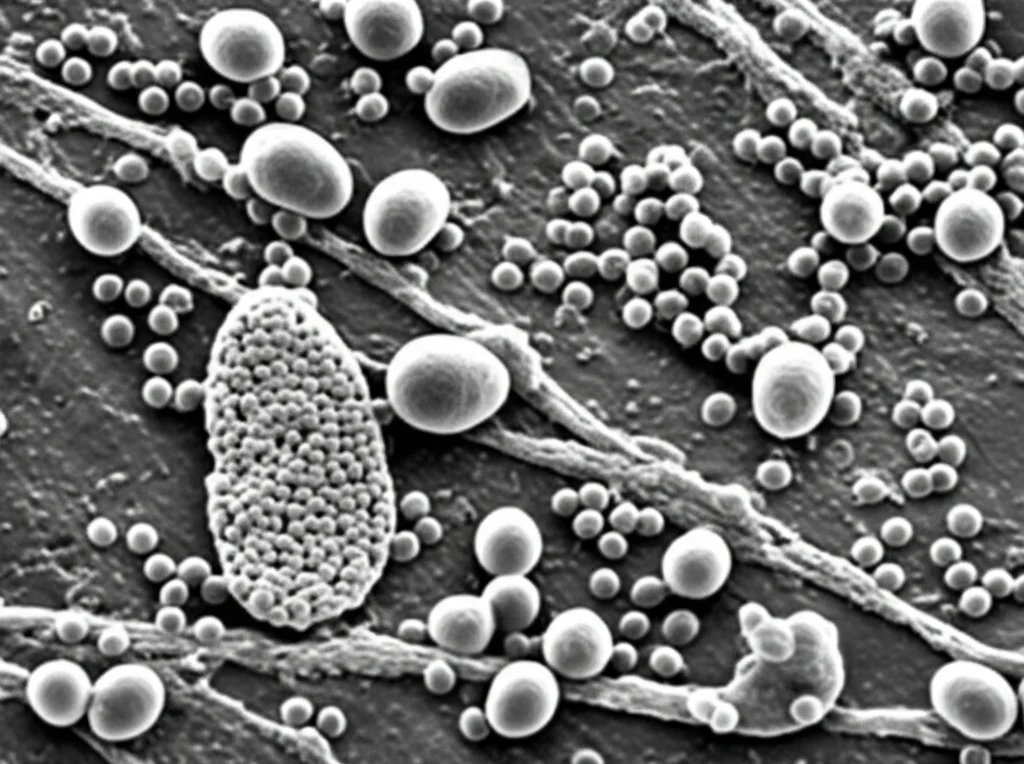
Funzioni Emergenti: Dalle Interazioni con l’Ospite alle Nucleasi
Tra le proteine identificate nelle EVs di Mmc e M. bovis, ne abbiamo trovate molte note per il loro ruolo nell’interazione con l’ospite. Ad esempio, proteine coinvolte nell’adesione alle cellule ospiti, come le lipoproteine variabili di superficie (Vsp) in M. bovis, erano presenti sia nelle cellule che nelle loro vescicole. Questo suggerisce che le EVs potrebbero giocare un ruolo diretto nel processo infettivo, magari preparando il terreno per l’arrivo dei batteri o interagendo direttamente con le cellule ospiti.
Un’altra scoperta interessante riguarda la presenza di nucleasi funzionanti nelle EVs. Le nucleasi sono enzimi che tagliano gli acidi nucleici (DNA e RNA). In M. bovis, queste sono importanti per acquisire nutrienti dal DNA dell’ospite e per eludere la risposta immunitaria, ad esempio degradando le “trappole extracellulari” (NETs) rilasciate dai neutrofili. Abbiamo dimostrato che sia le cellule batteriche che le EVs isolate di M. bovis erano in grado di degradare DNA plasmidico, sia circolare che linearizzato, indicando la presenza di attività endo- ed eso-nucleasica. Anche per Mmc, dove l’attività nucleasica era meno caratterizzata, abbiamo identificato potenziali nucleasi nel proteoma delle EVs e confermato sperimentalmente la loro capacità di degradare DNA. Questa attività enzimatica protetta all’interno delle vescicole potrebbe essere cruciale per la sopravvivenza e la patogenicità dei Mollicutes.
Le EVs come Modulatori Immunitari
Sapendo che le EVs di altri batteri possono influenzare il sistema immunitario dell’ospite, ci siamo chiesti se lo stesso valesse per quelle di M. bovis. Abbiamo esposto cellule mononucleate del sangue periferico bovino (PBMCs) alle EVs isolate e confrontato la risposta con quella indotta dai batteri vivi. I risultati sono stati chiari: le EVs stimolavano le cellule immunitarie bovine in modo molto simile ai batteri vivi, sebbene con un’intensità generalmente inferiore.
In particolare, abbiamo osservato una marcata attivazione delle cellule dendritiche (DCs), cellule immunitarie cruciali che fanno da ponte tra l’immunità innata e quella adattativa. Sia i batteri che le EVs inducevano l’espressione di marcatori di attivazione (CD25) e di migrazione (CCR7) sulle DCs. Questo suggerisce fortemente che le EVs rilasciate durante un’infezione da M. bovis possano interagire direttamente con il sistema immunitario dell’ospite, modulandone la risposta. Considerando le alte concentrazioni che questi batteri possono raggiungere in vivo, è probabile che anche le EVs vengano prodotte in quantità significative, contribuendo alla patogenesi.
Vesiduzione: Un Nuovo Canale per il Trasferimento Genico Orizzontale
Forse una delle scoperte più sorprendenti di questo studio riguarda un’altra funzione delle EVs: il trasferimento genico orizzontale (HGT). L’HGT è il passaggio di materiale genetico tra organismi diversi dalla classica trasmissione verticale da genitore a figlio. È un motore potentissimo dell’evoluzione batterica, permettendo la rapida acquisizione di nuovi geni, come quelli per la resistenza agli antibiotici o per la virulenza.
Sapevamo che i Mollicutes possono scambiarsi geni, e alcuni ospitano plasmidi (piccole molecole di DNA circolare extra-cromosomico). Ci siamo chiesti: potrebbero le EVs fungere da veicoli per trasportare questi plasmidi da un batterio all’altro? Questo meccanismo, chiamato “vesiduzione”, era stato descritto in Archaea e in alcuni batteri Gram-negativi, ma mai nei Mollicutes (e solo in una specie Gram-positiva).
Per investigare, abbiamo prima verificato se i plasmidi fossero presenti nelle EVs. Utilizzando la qPCR (una tecnica molecolare molto sensibile), abbiamo scoperto che le EVs di un ceppo di Mmc contenente un piccolo plasmide naturale (pKMK1) erano enormemente arricchite di questo plasmide rispetto al DNA cromosomico. Lo stesso valeva per un ceppo di Mmc modificato per portare un plasmide artificiale (pIVB08) con geni di resistenza agli antibiotici: le EVs contenevano molto più DNA plasmidico che cromosomico. Questo indicava che i plasmidi vengono effettivamente “impacchettati” nelle vescicole.
Il passo successivo era dimostrare il trasferimento. Abbiamo condotto esperimenti di vesiduzione, mettendo in contatto EVs isolate dal ceppo Mmc pIVB08 (trattate con DNasi per eliminare DNA libero esterno) con cellule riceventi di Mmc senza plasmide. Ebbene sì, siamo riusciti a ottenere trasformanti, cioè cellule riceventi che avevano acquisito il plasmide e la resistenza alla tetraciclina! Le frequenze di trasferimento non erano altissime, ma dimostravano la fattibilità del processo.
Ancora più interessante, abbiamo testato la vesiduzione tra specie diverse (trasferimento eterologo). Le EVs di Mmc pIVB08 sono state in grado di trasferire il plasmide a specie correlate come Mycoplasma capricolum subsp. capricolum (Mcap) e Mycoplasma leachii. Questo suggerisce che la vesiduzione potrebbe facilitare lo scambio di geni anche tra specie diverse di Mollicutes che condividono lo stesso ambiente o ospite.
Il Meccanismo Protetto della Vesiduzione
Come funziona esattamente la vesiduzione e cosa la influenza? Abbiamo condotto ulteriori esperimenti per capirlo. Abbiamo visto che trattamenti che danneggiano l’integrità della membrana delle EVs, come la lisi alcalina (aumento del pH) o lo stress termico (riscaldamento a 50-56°C), abolivano completamente la capacità di trasferire il plasmide. Questo conferma che le vescicole devono essere intatte per poter consegnare il loro carico.
Al contrario, trattare le EVs con Proteinase K (un enzima che digerisce le proteine) non ha influenzato la frequenza di vesiduzione. Questo, insieme al fatto che il trattamento iniziale con DNasi non impediva il trasferimento, suggerisce che il DNA plasmidico è protetto all’interno della vescicola, al riparo da enzimi degradativi presenti nell’ambiente esterno. Le EVs agiscono quindi come delle piccole capsule protettive per il materiale genetico che trasportano.
Conclusioni e Prospettive Future
Questo studio apre una nuova finestra sulla biologia complessa e affascinante dei Mollicutes. Abbiamo dimostrato che le loro vescicole extracellulari non sono semplici scarti, ma veri e propri mediatori multifunzionali. Riflettono la composizione della cellula madre, contengono proteine funzionali (come le nucleasi), possono modulare la risposta immunitaria dell’ospite e, cosa forse più sorprendente, possono facilitare il trasferimento orizzontale di geni tramite vesiduzione, anche tra specie diverse.
Queste scoperte ci aiutano a capire meglio come questi batteri minimalisti interagiscono con l’ambiente, causano malattie e si evolvono. La vesiduzione, in particolare, potrebbe essere un meccanismo importante, finora sottovalutato, per la diffusione di geni di virulenza o resistenza agli antibiotici all’interno delle popolazioni di Mollicutes.
Certo, rimangono ancora molte domande aperte. Quali fattori influenzano l’efficienza della vesiduzione? Quali altri tipi di molecole (RNA, metaboliti) vengono trasportate dalle EVs? Come interagiscono esattamente con le diverse cellule dell’ospite? Il lavoro futuro cercherà di rispondere a queste domande, approfondendo la nostra comprensione di questi incredibili messaggeri microscopici e del loro impatto sulla salute animale e umana. È un campo di ricerca in pieno fermento, e sono sicuro che i Mollicutes e le loro vescicole ci riserveranno ancora molte sorprese!
Fonte: Springer







