Epigraph: La Scommessa Vinta Contro l’Influenza Suina? Un Vaccino Ottimizzato che Promette Scudi Duraturi!
Il Nemico Invisibile negli Allevamenti (e non solo)
Parliamoci chiaro: l’influenza suina, o meglio, il virus dell’Influenza A nei suini (IAV-S), è una bella gatta da pelare. Non solo mette in ginocchio l’industria suinicola con perdite economiche stimate in centinaia di milioni solo negli Stati Uniti, ma rappresenta anche una minaccia costante per la salute pubblica. Perché? Perché i maiali sono considerati dei “recipienti di miscelazione” ideali per i virus influenzali. Hanno recettori sia per i virus suini che per quelli aviari e umani. Questo significa che se un maiale si becca più ceppi contemporaneamente, questi virus possono scambiarsi pezzi di materiale genetico (un processo chiamato riassortimento genetico) e dare vita a nuovi virus influenzali potenzialmente capaci di scatenare pandemie umane. Ricordate l’influenza suina del 2009? Ecco, quella è partita proprio da lì, infettando circa un quarto della popolazione mondiale e causando centinaia di migliaia di morti nel primo anno. L’Organizzazione Mondiale della Sanità non a caso considera l’influenza una priorità e i suini un serbatoio chiave per virus pandemici. Vaccinare i maiali, quindi, non è solo una questione economica per gli allevatori, ma una strategia cruciale per proteggere tutti noi.
I Vaccini Attuali: Un’Arma Spuntata?
Il problema è che i vaccini contro l’IAV-S attualmente in uso hanno i loro limiti. Spesso vengono aggiornati di rado e tendono a fornire un’immunità molto specifica per il ceppo virale contenuto nel vaccino. Ma l’IAV-S è un trasformista incredibile: muta rapidamente (deriva antigenica) e si scambia pezzi (shift antigenico), soprattutto la sua proteina di superficie più bersagliata dai vaccini, l’emoagglutinina (HA). Esistono diversi sottotipi (H1N1, H1N2, H3N2) e, all’interno del sottotipo H1 (il più diffuso e geneticamente vario nei suini USA), ci sono diverse linee genetiche (1A, 1B, 1C) e ulteriori sotto-cladi (α, β, γ, δ1, δ2, npdm). Spesso, l’immunità contro una linea non protegge dalle altre.
La strategia più comune è usare vaccini a virus intero inattivato (WIV), somministrati alle scrofe per passare gli anticorpi ai suinetti tramite il latte (immunità materna, MDA). Tuttavia, questa immunità può essere di breve durata, specifica per ceppo e, paradossalmente, in alcuni casi la MDA o la vaccinazione WIV stessa sono state associate a un peggioramento della malattia respiratoria (VAERD) se l’animale incontra poi un virus influenzale diverso da quello del vaccino. Si stanno esplorando nuove piattaforme, come i vaccini a particelle repliconiche (RP) o vaccini basati su vettori virali (adenovirus, Orf virus), ma anche queste hanno sfide, come la possibile interferenza degli anticorpi materni. C’è un bisogno disperato di vaccini più efficaci, ad ampio spettro e che inducano un’immunità duratura.

La Svolta Computazionale: Nasce Epigraph
Ed è qui che entro in gioco io, o meglio, la tecnologia che voglio raccontarvi: l’Epigraph. Immaginate di poter analizzare migliaia di sequenze genetiche del virus dell’influenza suina H1, raccolte dal 1930 al 2021, e usare un algoritmo intelligente per “disegnare” delle proteine HA vaccinali non basate su un singolo virus, ma ottimizzate per contenere gli “epitopi” più comuni e rappresentativi dell’intera popolazione virale. Gli epitopi sono quelle piccole porzioni del virus che il nostro sistema immunitario (sia i linfociti B che producono anticorpi, sia i linfociti T) impara a riconoscere e attaccare. L’idea di Epigraph è semplice quanto potente: creare degli immunogeni “mosaico” che insegnino al sistema immunitario a riconoscere un ventaglio molto più ampio di varianti virali. Abbiamo usato un approccio basato su grafi per identificare e assemblare questi epitopi chiave (sia T che B, considerando anche le combinazioni di aminoacidi vicini che possono formare epitopi conformazionali importanti per gli anticorpi), creando un cocktail di tre immunogeni Epigraph distinti (Epigraph 1, 2 e 3) per massimizzare la copertura. L’analisi ha mostrato che questo metodo permette di incorporare una percentuale significativamente maggiore di epitopi (fino al 6-10% in più) rispetto a ceppi virali selvaggi (wildtype, WT) rappresentativi o a quelli presenti in un vaccino commerciale di riferimento (FluSure XP®).
I Primi Test: Risultati Incoraggianti nei Topi
Per verificare se questa idea funzionasse, abbiamo prima testato il vaccino Epigraph (veicolato da un vettore adenovirale innocuo, Ad5) sui topi, confrontandolo con un vaccino simile contenente però le proteine HA di tre ceppi WT “naturali” (scelti per essere i più simili agli immunogeni Epigraph) e con il vaccino commerciale FluSure XP®. Abbiamo immunizzato i topi due volte e poi li abbiamo infettati con ceppi di IAV-S H1 appartenenti a diverse linee genetiche (α, γ, δ1), alcune molto diverse dagli immunogeni del vaccino. I risultati? Sorprendenti! Contro il ceppo più divergente (α clade), solo i topi vaccinati con Epigraph erano completamente protetti dalla perdita di peso e dalla morte, con una carica virale nei polmoni significativamente ridotta rispetto agli altri gruppi. Contro i ceppi più simili (γ e δ1), sia Epigraph che il vaccino WT proteggevano bene, ma Epigraph mostrava comunque una tendenza a ridurre maggiormente la carica virale. Il vaccino commerciale ha mostrato una protezione parziale e variabile. Questi dati preliminari ci hanno dato una grande spinta: l’ottimizzazione degli epitopi sembrava davvero fare la differenza, almeno nei topi.

La Prova del Nove: Epigraph nei Suini
Ma il vero banco di prova erano i suini, l’animale target. Abbiamo vaccinato suinetti di 3-4 settimane con Epigraph (sempre il cocktail dei tre immunogeni veicolati da Ad5), con il vaccino WT (stesso vettore Ad5) o con FluSure XP® (alla dose raccomandata). E abbiamo misurato la risposta immunitaria.
Anticorpi da Urlo: Già dopo una sola dose, i suini Epigraph mostravano titoli anticorpali inibenti l’emoagglutinazione (HI) – un indicatore chiave di protezione – considerati protettivi (≥1:40) contro ben 7 su 12 ceppi H1 diversi testati (suini di varie cladi, umani pandemici, aviari)! Il vaccino WT arrivava a 4/12, mentre FluSure XP® a nessuno. Dopo la seconda dose (il richiamo), Epigraph ha fatto centro: titoli protettivi contro TUTTI e 12 i ceppi (100%)! Il vaccino WT si è fermato a 8/12 (67%), mostrando una protezione più specifica per ceppi simili. FluSure XP®, pur migliorando dopo il richiamo, ha raggiunto la soglia protettiva solo per 6/12 ceppi (50%) e con titoli mediamente 3-5 volte inferiori a Epigraph e WT. Anche l’analisi degli anticorpi IgG leganti ha confermato la superiorità di Epigraph nel riconoscere un’ampia gamma di virus H1, inclusi ceppi asiatici.
Linfociti T Super-Attivati: Ma non ci sono solo gli anticorpi. I linfociti T sono cruciali per eliminare le cellule già infettate. Abbiamo misurato la loro attivazione (tramite produzione di interferone-gamma, IFN-γ, con test ELISpot) contro peptidi derivati da tre ceppi H1 molto diversi (un ceppo suino classico del 1931, un ceppo umano ancestrale PR/8/34 e il ceppo pandemico del 2009 CA/09). Risultato: i suini vaccinati con Epigraph hanno mostrato una risposta T cellulare significativamente più alta e più ampia (riconoscendo un maggior numero di epitopi diversi su tutti e tre i ceppi) rispetto ai suini vaccinati con WT, sia dopo la prima dose che, soprattutto, dopo il richiamo. Il vaccino FluSure XP®, essendo un WIV, come atteso non ha indotto risposte T cellulari significative. Questa potenziata risposta T cellulare è fondamentale e probabilmente contribuisce alla maggiore efficacia di Epigraph.
Protezione sul Campo (Simulato): Meno Febbre, Meno Virus, Polmoni più Sani
Ok, l’immunità sembra ottima, ma protegge davvero dalla malattia? Abbiamo infettato i suini vaccinati (due dosi) con un ceppo H1N1 γ circolante (A/swine/Minnesota/9606/2015). I suini vaccinati con Epigraph e WT non hanno mostrato febbre significativa, a differenza dei gruppi FluSure XP® e controllo (DPBS). Ma la vera differenza l’abbiamo vista nella diffusione del virus: i suini Epigraph avevano livelli di virus infettivo nei tamponi nasali significativamente più bassi rispetto a tutti gli altri gruppi (inclusi WT e FluSure XP®) e smettevano di diffondere il virus molto prima. A 5 giorni dall’infezione, quasi tutti i suini degli altri gruppi eliminavano ancora virus, mentre nel gruppo Epigraph solo un animale su cinque ne aveva tracce minime. Questo è importantissimo: ridurre la diffusione del virus negli allevamenti è cruciale!
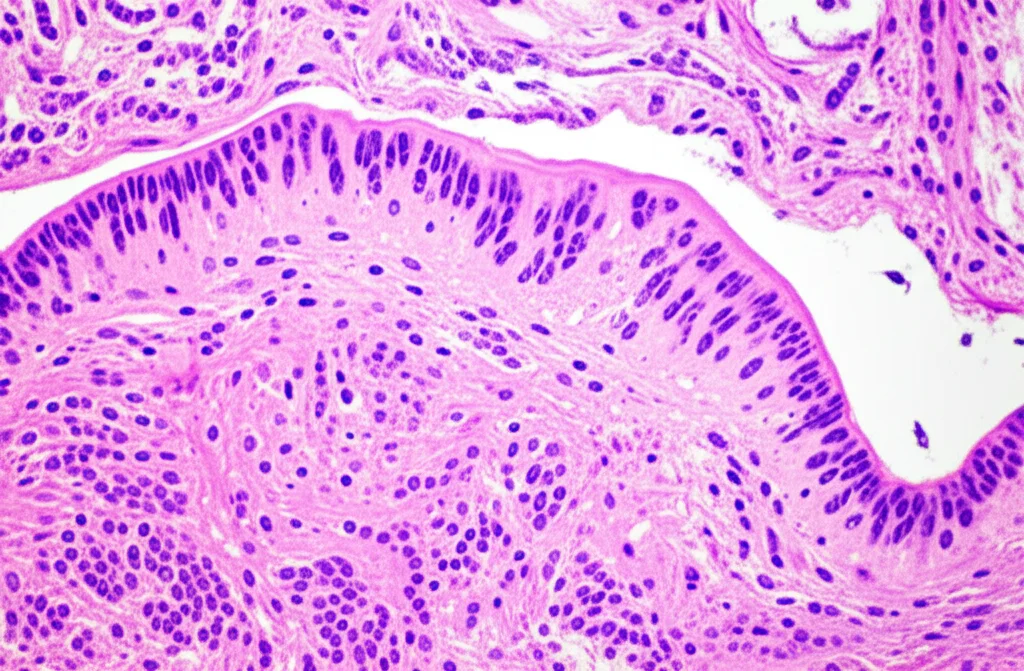
E i polmoni? Cinque giorni dopo l’infezione, abbiamo esaminato i polmoni. I suini Epigraph e WT avevano lesioni macroscopiche quasi assenti. Quelli vaccinati con FluSure XP® mostravano lesioni moderate, mentre i controlli avevano gravi consolidamenti polmonari tipici dell’influenza. A livello microscopico, Epigraph ha mostrato tessuti polmonari e tracheali sani, senza tracce di antigene virale. Il gruppo WT aveva una lieve polmonite interstiziale, ma senza virus rilevabile. Sorprendentemente, il gruppo FluSure XP® mostrava una polmonite interstiziale severa con cellule positive all’antigene virale, nonostante la carica virale nel lavaggio broncoalveolare (BAL) fosse bassa (simile a Epigraph e WT). Questo suggerisce che le lesioni in questo gruppo potrebbero essere più legate a una risposta immunitaria eccessiva (forse un accenno di VAERD?) piuttosto che alla replicazione virale diretta. I controlli, ovviamente, avevano il quadro peggiore, con bronchiolite, polmonite e molto antigene virale.
Immunità che Dura nel Tempo: Uno Scudo per Sei Mesi
Un buon vaccino deve proteggere a lungo. Quanto dura l’effetto di Epigraph? Abbiamo seguito un gruppo di suini vaccinati (Epigraph, FluSure XP® o controllo) per sei mesi, monitorando i loro anticorpi HI. La vita media di un suino da mercato negli USA è proprio di 6-7 mesi, quindi questo periodo è molto significativo. I risultati sono stati netti: Epigraph ha indotto rapidamente (entro 14-21 giorni dalla prima dose) anticorpi protettivi contro la stragrande maggioranza dei ceppi testati. Questi livelli sono aumentati dopo il richiamo (giorno 21) e, cosa fondamentale, sono rimasti alti e protettivi per tutti i 6 mesi dello studio contro praticamente tutti i ceppi (suini, umani, aviari). Al contrario, gli anticorpi indotti da FluSure XP® (che sono comparsi solo dopo il richiamo) sono scesi sotto la soglia protettiva già 30-60 giorni dopo il richiamo per molti ceppi. Questo dimostra che Epigraph non solo induce un’immunità più ampia, ma anche molto più duratura, potenzialmente coprendo l’intero ciclo di vita di un suino da ingrasso con un ciclo vaccinale standard.
Perché Epigraph Funziona Meglio?
La nostra ipotesi è che l’ottimizzazione degli epitopi sia la chiave. Includendo nel vaccino le “firme” immunologiche più comuni e conservate tra tantissimi ceppi virali diversi, alleniamo il sistema immunitario a riconoscere un bersaglio più ampio. Questo si traduce in:
- Anticorpi più “flessibili”: Capaci di neutralizzare non solo i ceppi simili ma anche quelli più distanti geneticamente.
- Risposta T cellulare potenziata: Una maggiore attivazione dei linfociti T, sia helper (che aiutano i linfociti B a produrre anticorpi migliori) sia citotossici (che uccidono le cellule infette), contribuisce a eliminare più rapidamente l’infezione e probabilmente alla durata dell’immunità.
È importante sottolineare che abbiamo usato lo stesso vettore adenovirale (Ad5) sia per Epigraph che per gli immunogeni WT. Questo ci permette di dire con buona confidenza che i vantaggi osservati per Epigraph derivano proprio dal design computazionale degli immunogeni e non dal vettore in sé. Il vettore Ad5 ha i suoi vantaggi (facile produzione, basso costo, resistenza all’interferenza da anticorpi materni – un plus non da poco per vaccinare i suinetti!), ma anche svantaggi (possibile immunità pre-esistente o indotta contro il vettore stesso, che potrebbe limitare l’efficacia dei richiami, anche se si possono usare sierotipi diversi).

Guardando al Futuro: Verso un Vaccino Universale?
I dati che abbiamo raccolto sono davvero promettenti. Dimostrano che un approccio computazionale come Epigraph può superare significativamente i vaccini tradizionali e anche immunogeni WT veicolati nello stesso modo, inducendo un’immunità contro l’H1 suino che è:
- Ampia: Copre diverse linee genetiche di IAV-S, ceppi umani pandemici e persino un ceppo aviario.
- Robusta: Alti livelli di anticorpi neutralizzanti e forte risposta T cellulare.
- Protettiva: Riduce malattia clinica, diffusione virale e danni polmonari.
- Duratura: Mantiene livelli protettivi per almeno 6 mesi.
Questo lavoro apre la strada a futuri vaccini “universali” contro l’influenza suina, che potrebbero non solo proteggere meglio la salute e la produttività degli allevamenti, ma anche ridurre drasticamente il rischio che dai maiali emergano nuovi virus influenzali pericolosi per l’uomo. La ricerca continua, ma Epigraph rappresenta un passo avanti significativo e affascinante.
Fonte: Springer