Hackerare il Sistema Immunitario: Come Stiamo Progettando un Vaccino Digitale Contro un Nemico Insidioso
Ciao a tutti! Oggi voglio parlarvi di un’avventura scientifica davvero affascinante che ci porta nel mondo microscopico dei batteri e nel futuro della medicina: la progettazione di vaccini al computer. Sì, avete capito bene, stiamo usando la potenza dei computer per creare armi su misura contro nemici invisibili ma pericolosissimi. E il nostro “cattivo” di oggi si chiama Fusobacterium necrophorum.
Chi è questo Fusobacterium necrophorum? Un ospite indesiderato
Immaginate un batterio Gram-negativo, anaerobico (cioè che vive senza ossigeno), che normalmente se ne sta tranquillo nella nostra bocca o nel nostro intestino, e anche in quello di molti animali. Sembra innocuo, vero? Beh, F. necrophorum è un classico opportunista. Appena le condizioni gli sono favorevoli, questo commensale si trasforma in un patogeno capace di causare infezioni necrotizzanti davvero gravi.
Nell’uomo, è il principale responsabile della sindrome di Lemierre, un’infezione rara ma potenzialmente letale che colpisce soprattutto i giovani adulti dopo un mal di gola. Ma non si ferma qui: può causare ascessi al fegato, infezioni dei tessuti molli e malattie parodontali.
E per gli animali? È un vero flagello per l’agricoltura, essendo la causa principale della pododermatite bovina (nota anche come “foot rot”), una malattia che provoca zoppia e gravi perdite economiche negli allevamenti di bovini e ovini in tutto il mondo. Pensate che in alcune regioni colpite, può interessare dal 30% all’80% delle mandrie! La sua presenza è segnalata ovunque, dall’Europa al Nord America, dall’Asia all’Africa, fino all’Oceania e al Sud America. Un problema globale, insomma.
Il problema: Antibiotici spuntati e assenza di scudi
Come combattiamo oggi questo batterio? Principalmente con gli antibiotici, come penicillina, metronidazolo e clindamicina. Ma c’è un “ma” grande come una casa: la resistenza antimicrobica. Anche i batteri anaerobi come il nostro Fusobacterium stanno diventando sempre più resistenti ai farmaci, rendendo le cure meno efficaci. Spesso, per le infezioni gravi, bisogna ricorrere anche alla chirurgia per drenare gli ascessi.
Il vero tallone d’Achille? Non esiste ancora un vaccino efficace contro F. necrophorum, né per l’uomo né per gli animali. Questa mancanza ci costringe a dipendere dagli antibiotici, alimentando il circolo vizioso della resistenza. È chiaro che abbiamo bisogno urgentemente di alternative, di nuove strategie. Ed è qui che entra in gioco la nostra ricerca.
L’idea geniale: Progettare un vaccino al computer
E se potessimo costruire un vaccino pezzo per pezzo, scegliendo solo le parti del batterio più “interessanti” per il nostro sistema immunitario, e assemblandole in una super-molecola? È esattamente quello che stiamo facendo usando la biologia computazionale e l’immunoinformatica. Il nostro obiettivo è creare un vaccino multi-epitopo.
Cosa significa? In pratica, andiamo a “studiare” il batterio al computer per identificare i suoi punti deboli, le molecole che il nostro sistema immunitario può riconoscere più facilmente per scatenare una risposta protettiva. Ci siamo concentrati sulle proteine transmembrana. Perché proprio queste? Perché sono esposte sulla superficie del batterio, quindi più accessibili per le nostre difese immunitarie, e spesso giocano ruoli chiave nell’adesione alle cellule ospiti, nell’invasione e nella virulenza generale del batterio. Sono come le “maniglie” a cui il sistema immunitario può aggrapparsi.
La “ricetta” digitale del nostro vaccino
Il primo passo è stato recuperare le sequenze di queste proteine da database pubblici come UniProt. Abbiamo selezionato quattro candidate promettenti: Protein translocase subunit SecA, ATP-dependent zinc metalloprotease FtsH, Outer membrane efflux protein, e Protein-export membrane protein SecF.
Poi, è iniziata la fase di “screening digitale”:
- Antigenicità: Abbiamo usato strumenti come VaxiJen per assicurarci che fossero fortemente antigeniche, cioè capaci di stimolare una risposta immunitaria (punteggio > 0.4).
- Sicurezza: Con AllerTOP e Toxipred abbiamo verificato che non fossero allergeniche né tossiche. La sicurezza prima di tutto!
- Localizzazione: Abbiamo confermato con TMHMM che fossero effettivamente proteine transmembrana.
Superato questo primo “controllo qualità”, siamo andati a caccia degli epitopi: piccoli frammenti di queste proteine che sono i veri e propri “bersagli” per le cellule immunitarie. Abbiamo cercato:
- Epitopi per cellule B: Usando Bepipred 2.0, abbiamo identificato le zone che possono essere riconosciute direttamente dagli anticorpi.
- Epitopi per cellule T (MHC-I e MHC-II): Con strumenti basati su reti neurali (ANN 4.0, NN-align) sull’Infrastructure for Epitope Data and Analysis (IEDB), abbiamo trovato i frammenti che vengono “presentati” dalle molecole MHC alle cellule T (CD8+ e CD4+), fondamentali per orchestrare la risposta immunitaria cellulare. Abbiamo selezionato solo quelli con un’alta affinità di legame (IC50 < 100 nM).
Abbiamo raccolto un bel bottino: 4 epitopi B, 8 epitopi MHC-I e 8 epitopi MHC-II, tutti rigorosamente non allergenici, non tossici e altamente antigenici.
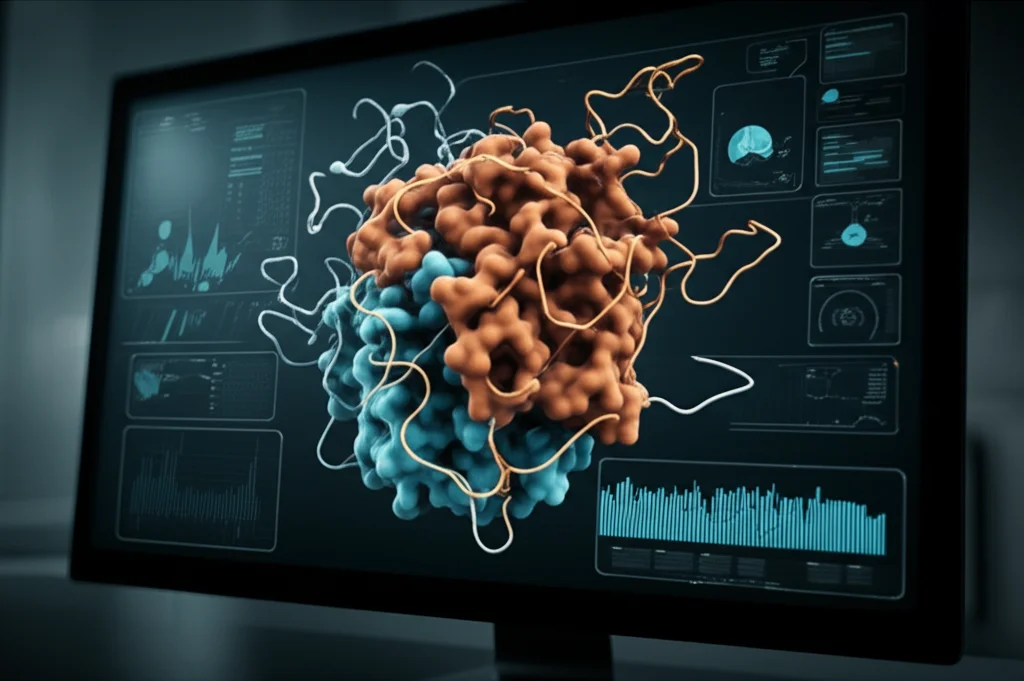
Costruire la “Super-Molecola”: L’arte dell’assemblaggio
Ora viene il bello: assemblare questi pezzi in un’unica molecola vaccinale. Non basta metterli uno dopo l’altro a caso! Abbiamo usato dei “linker” specifici, piccole sequenze di amminoacidi, per collegare gli epitopi in modo ottimale:
- GPGPG: Per separare i diversi tipi di epitopi, garantendo flessibilità e corretto processamento.
- KK (Lisina-Lisina): Per unire gli epitopi B, facilitando il riconoscimento da parte dei recettori delle cellule B.
- AAY e AYY: Per collegare rispettivamente gli epitopi MHC-I e MHC-II, ottimizzati per il taglio da parte del proteasoma e la presentazione alle cellule T.
Ma non è finita qui! Per dare una “spinta” in più alla risposta immunitaria, abbiamo aggiunto all’inizio (N-terminale) della nostra molecola un adiuvante, specificamente una sequenza di beta-defensina, nota per potenziare l’immunità. E alla fine (C-terminale), abbiamo inserito una sequenza “Padre” e una coda di 6 istidine (6X His-tag), utili per la futura purificazione del vaccino in laboratorio.
Il risultato? Un costrutto vaccinale di 353 amminoacidi, progettato razionalmente in ogni suo dettaglio.
Test virtuali: Il nostro vaccino sotto la lente d’ingrandimento digitale
Prima di pensare di produrlo davvero, dovevamo essere sicuri che il nostro “progetto” fosse solido. E qui la bioinformatica ci dà strumenti potentissimi.
Abbiamo analizzato le sue proprietà fisico-chimiche (peso molecolare circa 40.3 kDa, punto isoelettrico basico 9.63, indice di instabilità basso 23.71 che indica stabilità, valore GRAVY negativo -0.134 che suggerisce idrofilicità). Sembra stabile e ben comportato!
Poi siamo passati alla struttura 3D. Con strumenti come PSIPRED e GOR IV abbiamo predetto la struttura secondaria (elicje alfa, foglietti beta, regioni coil), e con TrRosetta abbiamo costruito il modello tridimensionale. La validazione è stata cruciale: il plot di Ramachandran ha mostrato che il 97.4% degli amminoacidi si trova in regioni “favorevoli”, e il programma ERRAT ha dato un punteggio di qualità altissimo (97.078). Insomma, la struttura sembra robusta e ben ripiegata.
Abbiamo anche usato Ellipro per identificare gli epitopi B discontinui (quelli formati da pezzi di proteina lontani nella sequenza ma vicini nello spazio 3D) e Disulfide by Design per ingegnerizzare dei ponti disolfuro (legami chimici forti) in punti strategici, per aumentare ulteriormente la stabilità della molecola.
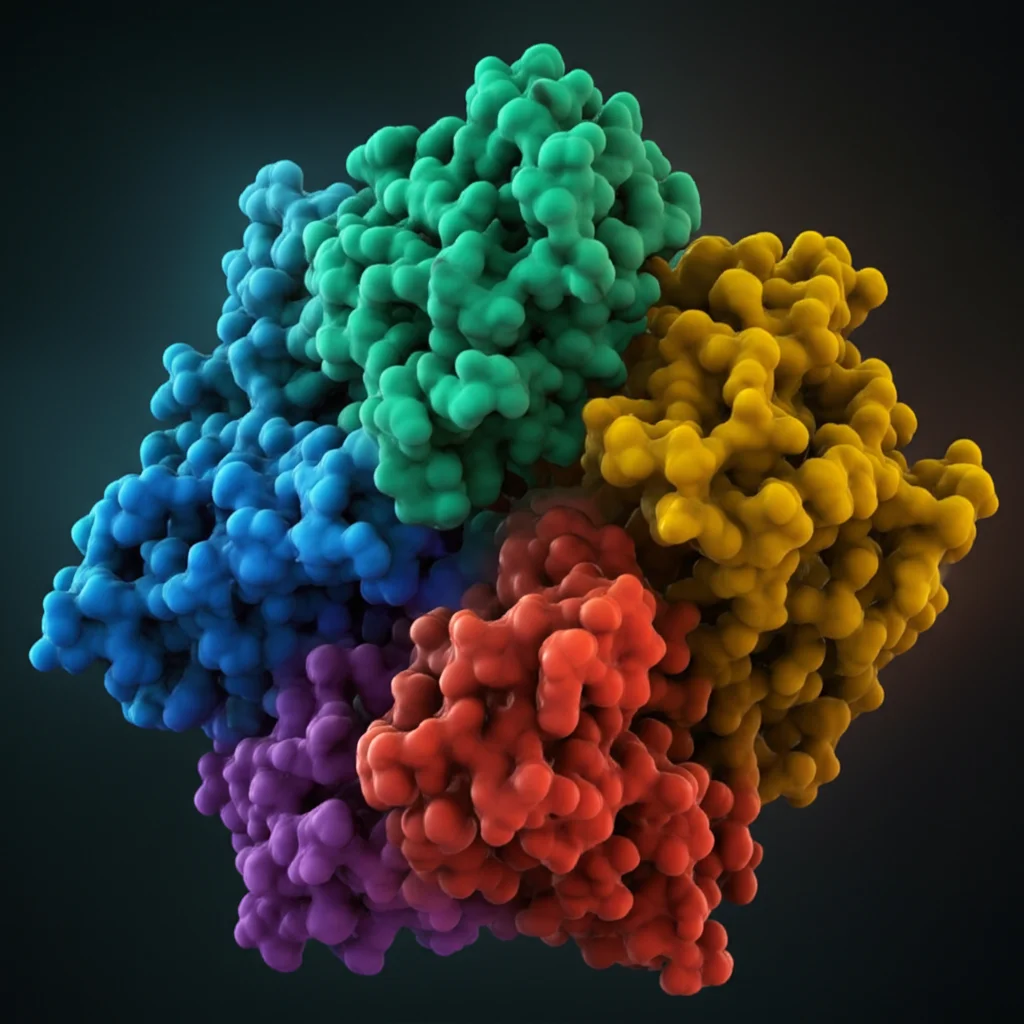
La prova del nove: L’interazione con il sistema immunitario (simulata!)
Un vaccino deve interagire con il sistema immunitario. Come capire se il nostro lo fa bene? Con il molecular docking. Abbiamo simulato l'”aggancio” del nostro vaccino a recettori chiave dell’immunità innata, i Toll-Like Receptors (TLR), in particolare TLR3, TLR4, TLR7 e TLR8, noti per riconoscere componenti batteriche.
I risultati? Interazioni deboli con TLR3 e TLR4, ma legami molto forti con TLR7 e soprattutto TLR8! Il complesso vaccino-TLR8(B) ha mostrato ben 13 legami idrogeno e un’energia di legame molto bassa (-1434.6 kcal/mol), segno di un’interazione stabile e potente. Questo è fantastico, perché TLR7 e TLR8 sono importantissimi per riconoscere acidi nucleici batterici e attivare la risposta immunitaria.
Per essere ancora più sicuri, abbiamo sottoposto il complesso vaccino-TLR8 a simulazioni di dinamica molecolare (MD) per ben 500 nanosecondi. È come mettere il complesso in un “ambiente virtuale” che simula le condizioni del corpo e vedere come si comporta nel tempo. I risultati sono stati eccellenti:
- RMSD (Root Mean Square Deviation): Si è stabilizzato intorno a 4-5 Å, indicando che la struttura complessiva rimane stabile senza grandi cambiamenti.
- RMSF (Root Mean Square Fluctuation): Ha mostrato che la maggior parte della molecola è stabile (fluttuazioni basse, 1.5-2.5 Å), con solo alcune regioni più flessibili (probabilmente loop esterni).
- Rg (Radius of Gyration): È rimasto costante intorno a 36 Å, confermando che il complesso non si “srotola” ma mantiene la sua compattezza.
- Analisi Energetica (MM/PBSA, FEL): Ha rivelato un’energia di legame libera molto favorevole (media intorno a -5000 kJ/mol) e paesaggi energetici che indicano uno stato stabile e termodinamicamente favorito per il complesso.
- PCA e DCCM: Hanno analizzato i movimenti interni, confermando la stabilità strutturale pur permettendo la flessibilità necessaria per l’attività biologica.
In sintesi, le simulazioni ci dicono che il nostro vaccino si lega saldamente a TLR8 e rimane stabile, pronto a “suonare l’allarme” per il sistema immunitario.
Verso il mondo reale: Ottimizzazione e simulazione della risposta
Un buon progetto digitale deve poter diventare realtà. Abbiamo ottimizzato la sequenza di DNA che codifica per il nostro vaccino per massimizzare la sua espressione nel batterio E. coli (un “cavallo di battaglia” per produrre proteine ricombinanti), abbassando il contenuto di GC e verificando che l’mRNA non formasse strutture secondarie problematiche. Abbiamo anche simulato l’inserimento del gene nel vettore di espressione pET-29a(+) usando il software SnapGene. Tutto pronto per la produzione!
E come reagirebbe il sistema immunitario? Abbiamo usato il server C-IMMSIM per una simulazione immunitaria. I risultati predicono una risposta robusta:
- Aumento significativo delle cellule B e produzione di anticorpi (IgM e IgG, con picchi fino a 5000 unità).
- Attivazione delle cellule T.
- Rilascio di citochine importanti come l’Interferone-gamma (IFN-γ), cruciale per eliminare i patogeni intracellulari e attivare i macrofagi.
Sembra proprio che il nostro vaccino possa stimolare sia l’immunità umorale (anticorpi) che quella cellulare.

Conclusioni (provvisorie) e prossimi passi: Dal bit all’atomo
Quindi, cosa abbiamo ottenuto? Abbiamo progettato al computer un candidato vaccino multi-epitopo contro Fusobacterium necrophorum che, sulla carta (o meglio, sullo schermo!), sembra davvero promettente: è potenzialmente sicuro (non tossico, non allergenico), fortemente immunogenico, strutturalmente stabile, si lega efficacemente a recettori immunitari chiave come TLR8, e le simulazioni prevedono una forte risposta immunitaria protettiva. Inoltre, ha una copertura di popolazione globale prevista altissima (>99%), il che significa che potrebbe funzionare in persone di diverse etnie.
Questo approccio computazionale è incredibilmente potente: ci permette di esplorare, progettare e testare candidati vaccinali in modo rapido ed economico, riducendo drasticamente i tempi e i costi rispetto ai metodi tradizionali, e soprattutto diminuendo la necessità di testare un gran numero di molecole sugli animali nelle fasi preliminari.
Ma attenzione! Tutto questo lavoro, per quanto entusiasmante, è stato fatto in silico, cioè al computer. È un primo passo fondamentale, una base solidissima, ma ora viene il bello (e il difficile): la validazione sperimentale. Dobbiamo produrre questo vaccino in laboratorio, testarlo in vitro (su cellule) e poi in vivo (su modelli animali) per confermare la sua sicurezza, la sua capacità di indurre la risposta immunitaria che abbiamo previsto e, soprattutto, la sua efficacia nel proteggere dalle infezioni da F. necrophorum.
Ci sono sfide da affrontare, come la produzione su larga scala, la formulazione del vaccino per garantirne stabilità e rilascio ottimale, e la possibile variabilità della risposta immunitaria tra individui diversi. Ma la strada è tracciata, e i risultati computazionali ci danno grande fiducia.
Questa ricerca è un esempio lampante di come la biologia computazionale stia rivoluzionando lo sviluppo di farmaci e vaccini, offrendoci nuove armi contro vecchi e nuovi nemici. Speriamo che questo lavoro possa contribuire un giorno a sconfiggere le pericolose infezioni causate da Fusobacterium necrophorum, proteggendo sia la salute umana che quella animale e aiutandoci a combattere la crescente minaccia della resistenza antimicrobica. L’avventura continua!
Fonte: Springer