Tumori Sinonasali e Mutazione BRAF: Sveliamo i Segreti di 5 Casi Complessi!
Ciao a tutti, appassionati di scienza e scoperte mediche! Oggi voglio portarvi con me in un viaggio affascinante, ma anche un po’ tortuoso, nel mondo dei tumori ameloblastici sinonasali. So che il nome suona complicato, ma fidatevi, la storia che si cela dietro è degna di un thriller scientifico. Immaginatevi dei tumori rari, che nascono nelle cavità nasali e paranasali, e che si comportano in modo diverso rispetto ai loro “cugini” più comuni che colpiscono la mandibola. Ebbene sì, perché la medicina è piena di queste sfumature!
Un Nemico Insidioso: I Tumori Ameloblastici Sinonasali
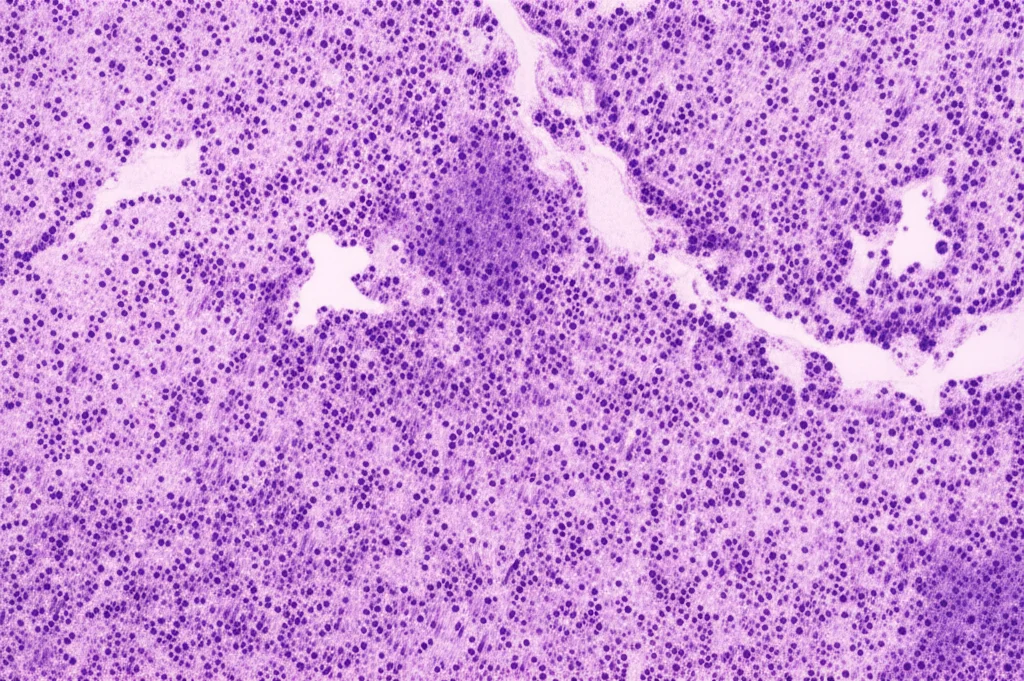
Allora, partiamo dalle basi. I tumori ameloblastici sono neoplasie epiteliali odontogene, il che significa che originano dai tessuti che normalmente formano i denti. Tra questi, troviamo l’ameloblastoma, l’ameloblastoma metastatizzante (che, come dice il nome, può dare metastasi) e il carcinoma ameloblastico, che è la forma maligna. L’ameloblastoma, pur essendo classificato come benigno dall’Organizzazione Mondiale della Sanità nel 2017, ha un caratteraccio: è localmente invasivo, tende a recidivare spesso e, a volte, decide di fare le valigie e viaggiare in altre parti del corpo (ecco l’ameloblastoma metastatizzante).
La maggior parte di questi tumori si sviluppa nella mandibola. Tuttavia, circa il 15% sceglie una location più “esclusiva”: la regione sinonasale. E qui le cose si complicano. Pensate che ad oggi sono documentati solo un centinaio di casi di tumori ameloblastici sinonasali. Questa rarità rende difficile capire a fondo il loro comportamento e, di conseguenza, trovare le strategie terapeutiche più efficaci. Un bel rompicapo, non trovate?
Una delle cose che ci ha sempre incuriosito è la differenza di comportamento tra i tumori della mandibola e quelli della mascella, anche se appartengono alla stessa “famiglia”. Questa discrepanza sembra dovuta a più fattori. Da un lato, c’è l’aspetto fisico: la mascella, con il suo osso più spugnoso, permette ai tumori di infiltrarsi più facilmente negli organi circostanti, come occhi e muscoli pterigoidei, rispetto alla più compatta mandibola. Dall’altro, e qui entriamo nel vivo del nostro discorso, ci sono le differenze genetiche. Nei tumori mandibolari, infatti, si riscontrano frequentemente mutazioni del gene BRAF, mentre nei casi mascellari queste mutazioni sono estremamente rare. Sembra quasi che lo stesso tipo di tumore cambi “personalità” a seconda di dove nasce!
Il Nostro Studio: Cinque Casi Sotto la Lente
Proprio per cercare di far luce su questi aspetti, nel nostro ospedale universitario di Kyushu, abbiamo analizzato cinque casi di pazienti giapponesi (quattro uomini e una donna, con età tra i 43 e i 73 anni) affetti da tumori ameloblastici sinonasali. Volevamo capire meglio il loro decorso clinico, i trattamenti ricevuti e, soprattutto, la presenza o meno della famosa mutazione BRAF.
Vi racconto brevemente le loro storie, perché ogni caso è un pezzetto del puzzle:
- Tre pazienti avevano una diagnosi di ameloblastoma. Uno di questi, purtroppo, ha avuto una recidiva che è progredita fino a diventare una condizione critica, proprio per la mancanza di trattamenti efficaci.
- Un paziente aveva un carcinoma ameloblastico, la forma maligna.
- L’ultimo paziente, sebbene la diagnosi istologica fosse di ameloblastoma, presentava metastasi ai linfonodi, configurandosi quindi come un ameloblastoma metastatizzante, con una malignità clinica evidente.
Tutti e cinque i pazienti sono stati sottoposti a una resezione radicale locale, cioè un intervento chirurgico mirato a rimuovere completamente il tumore. Tuttavia, la battaglia non è sempre facile: in tre di loro, i margini di resezione sono risultati positivi, il che significa che alcune cellule tumorali potrebbero essere rimaste. Due di questi pazienti hanno ricevuto una terapia post-operatoria (chemioterapia o radioterapia). La recidiva si è presentata in due pazienti; uno di loro, dopo chemio-radioterapia, ha ottenuto un controllo locale della malattia.
E la mutazione BRAF? Sorprendentemente, l’abbiamo rilevata solo in uno dei cinque pazienti. Questo dato, seppur su un piccolo numero di casi, sembra confermare la bassa frequenza di questa mutazione nei tumori sinonasali.

La Sfida della Resezione e il Fantasma della Recidiva
Parliamoci chiaro: i tumori ameloblastici sinonasali hanno una prognosi spesso infausta, con alti tassi di recidiva, malignità e metastasi. Perché? Le sfide anatomiche giocano un ruolo cruciale. Rimuovere completamente un tumore in questa zona, vicina a strutture vitali, è estremamente difficile. Non a caso, tre dei nostri pazienti avevano margini di resezione positivi, e spesso il limite era vicino alla base del processo pterigoideo – un punto anatomicamente critico.
Ma non è solo una questione di “geografia” tumorale. Anche i fattori istologici pesano. Il carcinoma ameloblastico, per esempio, ha tassi di sopravvivenza libera da malattia a 5 e 10 anni rispettivamente del 60.8% e 52.1%. L’ameloblastoma metastatizzante, pur essendo istologicamente benigno, può essere letale, con tassi di recidiva che vanno dal 24.6% al 71.1% e tassi di mortalità tra il 18.4% e il 25%. Quindi, i tumori sinonasali, che hanno una maggiore probabilità di includere queste varianti aggressive, partono già svantaggiati.
Il Mistero della Mutazione BRAF: Un Indizio Cruciale?
Torniamo un attimo alle mutazioni genetiche. Recenti scoperte hanno evidenziato che le mutazioni BRAF sono prevalenti (50-90%) negli ameloblastomi, ma principalmente in quelli della mandibola. Nella mascella, invece, sono più comuni le mutazioni del gene SMO. Si ipotizza che questa differenza nei geni “pilota” (driver gene) possa riflettere segnali distinti durante lo sviluppo dei denti superiori e inferiori, ma è ancora un’ipotesi da confermare. Quello che sembra emergere, però, è che una mancanza di mutazioni BRAF sia associata a una prognosi peggiore. E questo potrebbe contribuire alla prognosi sfavorevole dei tumori ameloblastici sinonasali, dove, come abbiamo visto anche nel nostro piccolo studio, la mutazione BRAF è rara.
Pensate un po’: il gene BRAF è coinvolto in una via di segnalazione cellulare che, se alterata, può portare alla crescita incontrollata delle cellule. Esistono farmaci, i cosiddetti inibitori di BRAF, che si sono dimostrati efficaci in alcuni tumori solidi BRAF-positivi. Ma se questi tumori sinonasali sono prevalentemente BRAF-negativi, questa opzione terapeutica viene a mancare quando la malattia recidiva. Ecco perché prevenire la recidiva con il trattamento iniziale diventa ancora più cruciale.

Verso Nuove Strategie Terapeutiche: Un Barlume di Speranza?
Quindi, come dovremmo trattare questi tumori così ostici? Basandoci sulla nostra esperienza, seppur limitata a cinque casi, proponiamo di considerare una chemioradioterapia adiuvante post-operatoria. Tradizionalmente, gli ameloblastomi sono considerati radioresistenti, e la radioterapia a scopo curativo per quelli operabili non è la prima scelta. Tuttavia, report recenti suggeriscono benefici della radioterapia post-operatoria nel controllo locale. Addirittura, terapie con fasci di particelle o protoni sembrano promettenti per casi inoperabili. Anche l’efficacia del cisplatino in chemioradioterapia per pazienti inoperabili è stata segnalata.
Nel nostro studio, un paziente che ha ricevuto chemioradioterapia al momento della recidiva ha ottenuto un controllo locale della malattia per 4 anni, un risultato incoraggiante. Al contrario, in un altro caso in cui è stata applicata solo radioterapia post-operatoria, la recidiva locale si è comunque verificata. Questo ci suggerisce che la combinazione di cisplatino e radioterapia potrebbe essere più efficace.
È fondamentale capire che i tumori ameloblastici sinonasali, anche se diagnosticati istologicamente come benigni, possono diventare un problema serio in caso di recidiva, quando un secondo intervento chirurgico potrebbe non essere fattibile. Nonostante una diagnosi istologica “tranquilla”, il decorso clinico può assomigliare a quello di una vera e propria malignità.
Cosa Ci Riserva il Futuro?
Sulla base della nostra esperienza, ci sentiamo di proporre alcune conclusioni, seppur con la dovuta cautela data la casistica limitata. Riteniamo che in presenza di uno dei seguenti fattori:
- Margini di resezione positivi
- Diagnosi istologica di carcinoma ameloblastico
- Presenza di metastasi ai linfonodi
una terapia adiuvante post-operatoria con cisplatino combinato a radioterapia potrebbe contribuire a migliorare la prognosi. È importante sottolineare che questa è una proposta basata sulla nostra esperienza diretta con questi cinque pazienti, non su evidenze consolidate da grandi studi, che purtroppo mancano per malattie così rare.
In conclusione, i tumori ameloblastici sinonasali che originano nella mascella presentano profili clinici e anomalie genetiche distinti rispetto alla maggior parte dei tumori ameloblastici che insorgono nella mandibola. Data l’alta incidenza di recidiva, malignità e potenziale metastatico, suggeriamo di valutare l’aggiunta della chemioradioterapia come trattamento adiuvante post-operatorio quando si identificano fattori che indicano una maggiore probabilità di recidiva dopo la resezione radicale.
Ovviamente, la strada è ancora lunga. C’è un disperato bisogno di raccogliere più casi, di condividere esperienze e di condurre studi multicentrici per definire strategie di gestione appropriate per questi tumori rari ma aggressivi. Ogni piccolo passo avanti nella comprensione è una speranza in più per i pazienti.

Fonte: Springer