TRPV2: Il Segreto del Cuore per Resistere allo Stress (Svelato!)
Amici scienziati e cuori curiosi, benvenuti! Oggi voglio parlarvi di una scoperta che mi ha davvero affascinato e che riguarda il nostro organo più instancabile: il cuore. Sappiamo tutti che il cuore è una macchina pazzesca, capace di adattarsi e compensare dinamicamente gli stress emodinamici, un po’ come un atleta che si allena per una maratona. Ma come si forma questa incredibile “resilienza” durante la crescita del cuore? Ecco, è proprio qui che entra in gioco il protagonista della nostra storia: un canale ionico chiamato TRPV2 (Transient Receptor Potential Vanilloid family 2).
Un Cuore a Prova di Stress: Ma Come Fa?
La maturazione è l’ultima, cruciale fase dello sviluppo cardiaco. È come se il cuore facesse l’ultimo sprint per prepararsi a pompare sangue in modo forte ed efficiente per tutta la vita. Durante questa fase, le cellule muscolari del cuore, i cardiomiociti, crescono, si specializzano e imparano a contrarsi in modo coordinato. È un processo complesso, e capire come tutti questi ingranaggi si incastrano perfettamente è fondamentale, soprattutto per la medicina rigenerativa e per studiare patologie come l’insufficienza cardiaca.
Il cuore, pensateci, risponde al carico emodinamico, cioè alla pressione e al volume di sangue che deve gestire, modificando la sua forma e funzione. Ma come fa a “sentire” questo stress meccanico e a rispondere di conseguenza? Per anni, gli scienziati hanno cercato il meccanismo di meccanotrasduzione, ovvero come lo stress meccanico si traduce in segnali biochimici che modificano le cellule. Si è pensato a un canale chiamato Piezo1, ma studi su topolini geneticamente modificati hanno mostrato che, pur essendo un sensore meccanico, il suo ruolo nello sviluppo e nella crescita del cuore sembra marginale.
TRPV2: Un Canale Ionico Sotto i Riflettori
Qui la storia si fa interessante. Esiste una famiglia di canali ionici, chiamati TRP (Transient Receptor Potential), che sembrano avere un ruolo chiave nel rimodellamento del cuore in risposta, ad esempio, a un sovraccarico di pressione. Alcuni membri di questa famiglia, come TRPC3, TRPC6 e TRPV4, sono stati studiati, ma il loro contributo alla maturazione dei cardiomiociti sembra limitato.
E poi c’è lui, TRPV2. In studi precedenti, il mio team (metaforicamente parlando, ovviamente!) e altri ricercatori avevamo già notato qualcosa di speciale. Avevamo visto che TRPV2 può essere attivato da stimoli meccanici, come lo stiramento cellulare o variazioni di tonicità. E, cosa ancora più intrigante, l’eliminazione specifica di TRPV2 nel cuore di topi adulti portava a una grave disfunzione cardiaca, con problemi strutturali ai dischi intercalari (le giunzioni che connettono i cardiomiociti tra loro, fondamentali per la comunicazione meccanica ed elettrica) e un calo nei segnali di crescita come quello mediato dal recettore IGF-1 (Insulin-like growth factor 1 receptor).
Quindi, la domanda sorgeva spontanea: che ruolo gioca TRPV2 durante la crescita postnatale del cuore e la maturazione dei cardiomiociti? Per scoprirlo, abbiamo utilizzato un modello di topolini in cui potevamo “spegnere” il gene TRPV2 specificamente nel cuore e in un momento preciso, cioè durante la fase giovanile (a 2 settimane di età).
Cosa Succede Senza TRPV2? L’Esperimento sui Topolini
Abbiamo somministrato tamoxifene a questi topolini per indurre lo spegnimento del gene TRPV2 e poi li abbiamo lasciati crescere fino all’età adulta (12 settimane), confrontandoli con topolini di controllo. I risultati sono stati illuminanti! I cuori dei topolini senza TRPV2 (chiamiamoli MCM-TRPV2-cKO) rimanevano più piccoli rispetto ai controlli, quasi come se non fossero maturati del tutto. La loro contrattilità era più debole e mostravano una bassa espressione di proteine chiave come SERCA2a (fondamentale per il ciclo del calcio) e di molecole legate alla via di segnalazione del Fattore di Risposta Sierico (SRF) e dell’IGF-1, entrambi cruciali per la crescita e la maturazione.
Analizzando i singoli cardiomiociti isolati da questi cuori, abbiamo confermato che la loro capacità contrattile era ridotta e che la gestione del calcio (essenziale per la contrazione) era anomala. Immaginate il calcio come il direttore d’orchestra della contrazione cardiaca: se non dà i comandi giusti al momento giusto, la musica (cioè il battito) ne risente.
Anche in colture di cardiomiociti neonatali, abbiamo visto che TRPV2 è necessario per la risposta meccanica al calcio, per l’accoppiamento eccitazione-contrazione, per il contenuto di calcio nel reticolo sarcoplasmatico (una sorta di magazzino del calcio), per la formazione delle fibre di actina (parte dell’apparato contrattile) e per la corretta localizzazione nucleare di fattori di trascrizione come MEF2c, oltre che per l’espressione di IGF-1.
Dischi Intercalari in Disordine e Calcio “Distratto”
Scendendo più nel dettaglio, abbiamo osservato che nei cuori adulti senza TRPV2, la localizzazione delle proteine che regolano il calcio era disorganizzata. Normalmente, queste proteine (come i canali del calcio di tipo L, lo scambiatore sodio-calcio NCX1, SERCA2a e la giuntofilina-2 o JP2) formano una struttura ordinata, a “scala”, essenziale per un efficiente ciclo del calcio. Nei cuori MCM-TRPV2-cKO, questa organizzazione era persa. Era come se gli operai specializzati di un cantiere (le proteine del calcio) non fossero più nelle loro postazioni corrette, compromettendo l’intero lavoro (la contrazione).
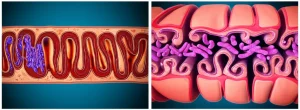
Inoltre, i dischi intercalari, che nei cuori sani adulti mostrano una caratteristica struttura a “fisarmonica”, nei cuori senza TRPV2 apparivano irregolari e disorganizzati, con una localizzazione diffusa della connessina 43, una proteina fondamentale per le giunzioni comunicanti. Questo suggerisce che TRPV2 è cruciale per lo sviluppo corretto di queste importanti strutture di connessione intercellulare.
Un altro dato interessante riguarda SERCA2a: la sua espressione era drasticamente ridotta nei cuori giovani MCM-TRPV2-cKO, per poi aumentare (ma non normalizzare la funzione) negli adulti. Questo suggerisce che la mancanza di TRPV2 in giovane età ha un impatto profondo sulla regolazione di questa proteina, influenzando poi lo sviluppo della funzione contrattile e l’integrità dei sarcomeri (le unità contrattili fondamentali del muscolo).
Segnali Interrotti: Le Vie di SRF e IGF-1
Per capire il meccanismo molecolare dietro questi difetti, abbiamo analizzato le vie di segnalazione intracellulare. La via dell’IGF-1, che regola la maturazione dei cardiomiociti, risultava attenuata nei cuori giovani senza TRPV2. Anche l’espressione di SRF, un altro regolatore chiave della maturazione, era bassa sia nei cuori giovani che adulti MCM-TRPV2-cKO. Questi risultati indicano che TRPV2 è un tassello fondamentale per attivare queste vie di segnalazione che promuovono la crescita e la maturazione fisiologica del cuore.
Abbiamo provato a “soccorrere” questi cuori somministrando IGF-1, ma sebbene ci fosse un parziale miglioramento, non si arrivava a una correzione completa dell’ipertrofia. Questo ci dice che il segnale mediato da TRPV2 è più complesso e non si limita solo alla via dell’IGF-1, ma probabilmente coinvolge in modo critico anche SRF.
Sotto Pressione: Come Reagiscono i Cuori Senza TRPV2?
Ma la vera prova del nove per la resilienza è la risposta allo stress. Abbiamo quindi sottoposto i nostri topolini a diversi tipi di stress cardiaco.
- Stress da Dobutamina: La dobutamina è un farmaco che stimola il cuore ad aumentare frequenza e contrattilità. Nei topolini di controllo, la contrattilità aumentava notevolmente. Nei cuori senza TRPV2, invece, l’aumento era minimo. Era come se non avessero la “riserva contrattile” per rispondere allo stimolo.
- Stress Cronico da Fenilefrina: La fenilefrina induce ipertrofia (un ingrossamento del cuore). I cuori di controllo rispondevano con un’ipertrofia adattativa. I cuori MCM-TRPV2-cKO, invece, non mostravano ipertrofia adattativa, ma andavano incontro a dilatazione, fibrosi e grave disfunzione. Non riuscivano ad adattarsi allo stress cronico.
- Sovraccarico di Pressione (TAC): Abbiamo indotto un restringimento dell’aorta (Transverse Aortic Constriction – TAC) per simulare un sovraccarico di pressione. I cuori di controllo sviluppavano ipertrofia e, a lungo termine, insufficienza. Sorprendentemente, i cuori senza TRPV2 non mostravano cambiamenti significativi né morfologici né funzionali dopo la TAC. Era come se… non “sentissero” il sovraccarico di pressione!
Questi esperimenti suggeriscono fortemente che TRPV2 è un componente chiave del sistema meccanotrasduttivo dei cardiomiociti. Senza di esso, il cuore non solo non matura correttamente, ma perde anche la capacità di percepire e rispondere adeguatamente agli stress emodinamici.
TRPV2: Una Nuova Speranza per le Malattie Cardiache?
Cosa ci portiamo a casa da tutta questa ricerca? Beh, sembra proprio che TRPV2 sia cruciale per la maturazione della resilienza allo stress nei cardiomiociti. Questo canale ionico non è solo un “operaio” nella cellula, ma un vero e proprio “capocantiere” che dirige la crescita, la maturazione strutturale e funzionale, e la capacità del cuore di rispondere e adattarsi alle sfide.
Pensiamo a due ipotesi principali. Primo, la ridotta trascrizione mediata da SRF nel cuore in crescita senza TRPV2 sopprime la maturazione dei cardiomiociti. SRF è come un interruttore generale per la crescita fisiologica e l’ipertrofia patologica. Secondo, i dischi intercalari anomali e la ridotta contrattilità dei cardiomiociti nei cuori senza TRPV2 riducono l’integrità cardiaca. Questo, a sua volta, porta a una ridotta percezione dello stress biomeccanico, che è essenziale per una normale maturazione funzionale e morfologica. È un circolo vizioso: se non senti lo stress, non ti adatti; se non ti adatti, sei più vulnerabile.
La ridotta espressione di SERCA2a in giovane età nei cuori MCM-TRPV2-cKO potrebbe influenzare l’omeostasi del calcio e, di conseguenza, la via IGF1R/PI3K/Akt, contribuendo ai difetti di maturazione. Anche se l’espressione di SERCA2a aumenta nell’adulto, i danni strutturali alla diade (l’accoppiamento tra tubuli T e reticolo sarcoplasmatico) ormai avvenuti impediscono un recupero funzionale completo.
TRPV2 sembra quindi regolare i segnali coinvolti nella formazione dei tubuli T e della struttura diadica, oltre a controllare l’espressione di IGF-1, forse attraverso SRF. L’aumento della contrattilità durante la crescita, a sua volta, potenzia la maturazione dei cardiomiociti attraverso un feedback meccanico positivo, e TRPV2, con il suo ruolo nella risposta al calcio dipendente dallo stress meccanico e nella formazione delle miofibrille, è al centro di questo processo.
Capire a fondo il ruolo di TRPV2 potrebbe aprire la strada a nuove strategie terapeutiche. Immaginate di poter “allenare” meglio i cuori immaturi o di poter migliorare la resilienza di cuori malati agendo su questo canale. È un campo di ricerca ancora aperto, ma le prospettive sono davvero entusiasmanti. La promozione dell’attività di TRPV2 nei cardiomiociti immaturi potrebbe essere una strategia efficace per indurre la maturazione e la differenziazione, con applicazioni nell’ingegneria tissutale e nella medicina rigenerativa.
Certo, ci sono ancora molte domande a cui rispondere, come ad esempio se TRPV2 senta direttamente lo stress meccanico o sia parte di un complesso più ampio. E bisogna considerare che TRPV2 è espresso in molti tessuti, quindi il suo ruolo specifico nel sistema cardiovascolare va ulteriormente chiarito. Ma ogni scoperta ci avvicina un po’ di più a svelare i complessi meccanismi che governano la salute del nostro cuore.
Per oggi è tutto, spero di avervi trasmesso un po’ della mia passione per questa incredibile ricerca. Alla prossima!
Fonte: Springer