Cancro Ovarico: Come la Trombospondina-1 Spegne le Nostre Difese Immunitarie (e Come Possiamo Riaccenderle!)
Ciao a tutti, appassionati di scienza e curiosi! Oggi voglio parlarvi di una scoperta che mi ha davvero colpito nel campo della lotta contro uno dei nemici più subdoli della salute femminile: il cancro ovarico. Sapete, questa malattia è particolarmente aggressiva e spesso viene diagnosticata tardi, il che complica parecchio le cose. Ma la ricerca non si ferma mai, e ogni giorno facciamo piccoli (o grandi) passi avanti per capirne i meccanismi e, speriamo, per sconfiggerla.
Il Campo di Battaglia: il Microambiente Tumorale
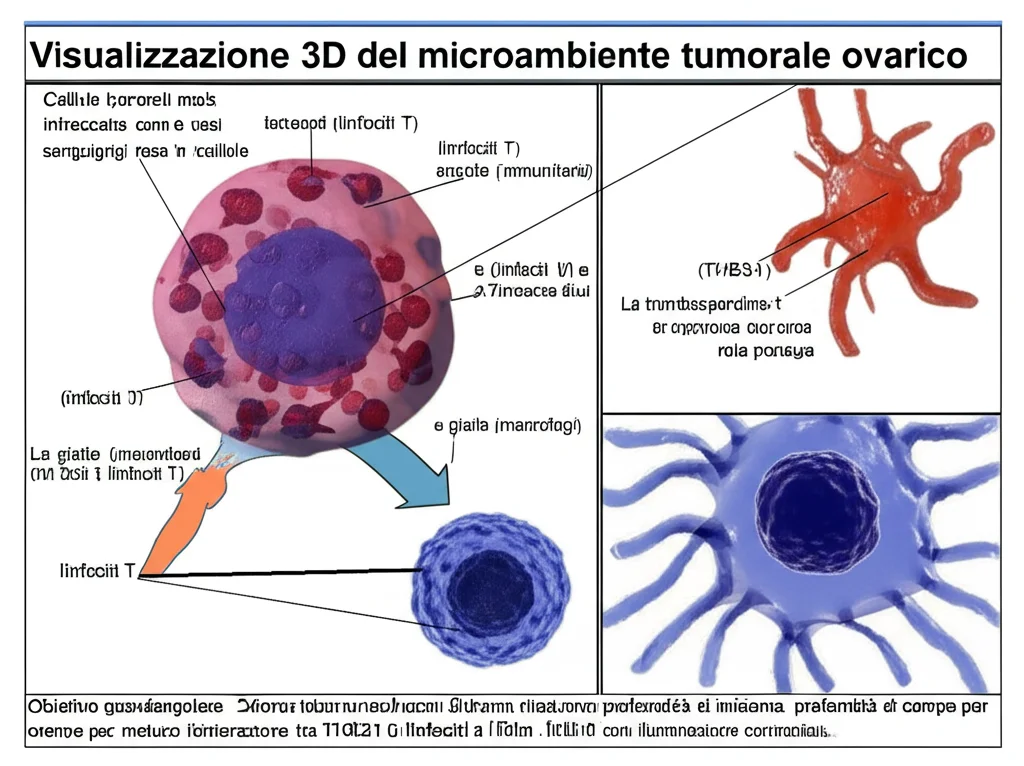
Immaginate il tumore non come una massa isolata, ma come una sorta di “cittadella fortificata” con un suo ecosistema interno: il microambiente tumorale (TME). È un mix complesso di cellule tumorali, cellule di supporto (stromali), vasi sanguigni e, cosa fondamentale per il nostro discorso, cellule immunitarie. Il problema è che, spesso, questo TME è un ambiente ostile per le nostre difese, un po’ come se i nostri soldati (le cellule immunitarie) venissero ingannati o indeboliti dal nemico.
Tra i protagonisti di questo “dramma” cellulare ci sono i macrofagi associati al tumore (TAM) e i linfociti T. I TAM, in particolare quelli “polarizzati” in senso M2, invece di combattere il tumore, finiscono per aiutarlo, un po’ come dei disertori che passano al nemico. I linfociti T, soprattutto i CD8+ che sono i nostri killer specializzati, possono andare incontro a un fenomeno chiamato “esaurimento”: in pratica, si stancano e perdono la capacità di attaccare efficacemente le cellule tumorali. È frustrante, vero? Come avere un esercito potente ma demotivato e senza armi.
La Trombospondina-1 (THBS1): Un Regista Occulto dell’Immunosoppressione
Ed è qui che entra in gioco la protagonista della nostra storia, una proteina chiamata Trombospondina-1 (THBS1). Studi recenti, come quello che vi racconto oggi, hanno messo in luce il suo ruolo, ahimè, negativo nel cancro ovarico. Pensate alla THBS1 come a un abile sabotatore che lavora nell’ombra.
Abbiamo scoperto che la THBS1 è significativamente sovraespressa nei tessuti tumorali ovarici rispetto ai tessuti sani. E, purtroppo, alti livelli di THBS1 sono associati a una prognosi peggiore per le pazienti. Ma cosa fa esattamente questa proteina per meritarsi la nostra attenzione (e preoccupazione)?
Beh, sembra che la THBS1 sia una maestra nel manipolare il TME a favore del tumore. Ecco i suoi “trucchi”:
- Attira i “disertori”: Promuove il reclutamento dei macrofagi nel tumore.
- Li converte alla “causa oscura”: Induce la polarizzazione di questi macrofagi verso il fenotipo M2, quello pro-tumorale, attraverso segnali come TGF-β1 e IL-4. Questi TAM M2 poi rilasciano sostanze che aiutano il tumore a crescere e a eludere il sistema immunitario.
- Spegne i nostri “soldati”: La THBS1 contribuisce all’esaurimento dei linfociti T CD8+. Lo fa, tra le altre cose, aumentando l’espressione di molecole chiamate “checkpoint immunitari”, come PD-L1 e GAL-3, sulla superficie delle cellule tumorali o di altre cellule del TME. Questi checkpoint sono come dei segnali di “stop” per i linfociti T: quando si legano ai loro recettori sui linfociti, ne bloccano l’attività. Immaginate un soldato pronto all’attacco che viene improvvisamente immobilizzato.
SNF2H: Il “Burattinaio” Dietro le Quinte di THBS1
Ma la storia non finisce qui. Ci siamo chiesti: cosa causa questa sovraespressione di THBS1? È come cercare il mandante di un crimine. Ebbene, le indagini ci hanno portato a un altro attore molecolare: una proteina chiamata SNF2H. Questa SNF2H è un “rimodellatore della cromatina”, il che significa che può influenzare l’espressione dei geni agendo sul modo in cui il DNA è impacchettato.
Abbiamo scoperto che SNF2H è anch’essa sovraespressa nel cancro ovarico e, guarda caso, la sua espressione è correlata positivamente con quella di THBS1. Attraverso esperimenti sofisticati (come la ChIP, immunoprecipitazione della cromatina), abbiamo dimostrato che SNF2H si lega direttamente al promotore del gene THBS1, cioè alla regione che ne controlla l’accensione. In pratica, SNF2H agisce come un interruttore che tiene costantemente acceso il gene THBS1, portando alla sua produzione eccessiva.
Cosa Abbiamo Visto negli Esperimenti?
Per arrivare a queste conclusioni, non ci siamo basati solo su analisi di database (come TCGA-OV o GSE14407, che sono miniere d’oro di informazioni genetiche). Abbiamo fatto esperimenti in laboratorio:
- Su cellule in coltura: Abbiamo usato linee cellulari di cancro ovarico (come SKOV3 e A2780) e le abbiamo messe a contatto con monociti umani (THP-1, che possono diventare macrofagi) o con linfociti T CD8+. Quando le cellule tumorali esprimevano tanta THBS1, i macrofagi venivano attratti più facilmente e si trasformavano in M2. I linfociti T, invece, mostravano segni di esaurimento e perdevano la loro capacità di uccidere le cellule tumorali.
- Su modelli animali: Abbiamo usato topi con cancro ovarico. Nei topi in cui THBS1 era “spenta” (knockout), la crescita tumorale era ridotta. Abbiamo osservato meno macrofagi M2 e più linfociti T CD8+ attivi nel tumore. Inoltre, i livelli dei checkpoint immunitari PD-L1 e GAL-3 erano più bassi. Questo ci dice che bloccare THBS1 in vivo può davvero fare la differenza nel riattivare una risposta immunitaria anti-tumorale.
Quando abbiamo “silenziato” SNF2H nelle cellule tumorali, abbiamo visto una riduzione dell’espressione di THBS1. Questo conferma il legame tra i due.
Implicazioni Terapeutiche: Una Nuova Speranza?
Ora, perché tutto questo è così affascinante e importante? Perché apre nuove prospettive terapeutiche. Se THBS1 è un attore chiave nel creare un ambiente immunosoppressivo e nel far “stancare” i nostri linfociti T, allora bersagliarla potrebbe essere una strategia vincente.
Immaginate di poter:
- Ridurre il reclutamento e la polarizzazione dei macrofagi M2.
- Diminuire l’espressione di PD-L1 e GAL-3.
- “Risvegliare” i linfociti T CD8+ esauriti, ripristinando la loro capacità di combattere il tumore.
Questo potrebbe rendere il microambiente tumorale meno ospitale per il cancro e, soprattutto, potrebbe migliorare l’efficacia delle immunoterapie esistenti, come quelle basate sugli inibitori dei checkpoint immunitari. Se già blocchiamo PD-1/PD-L1, ma THBS1 continua a remare contro, l’effetto potrebbe essere limitato. Agire su THBS1 (o persino sul suo regolatore SNF2H) potrebbe essere la chiave per sbloccare una risposta immunitaria più potente e duratura.
Certo, la strada è ancora lunga. Bisogna sviluppare farmaci specifici, testarli, assicurarsi che siano sicuri ed efficaci. Ma ogni scoperta come questa ci avvicina un po’ di più all’obiettivo. Capire i meccanismi molecolari alla base della progressione del cancro e dell’evasione immunitaria è fondamentale.
Questo studio, quindi, non solo ci dice che THBS1 è un “cattivo” nel cancro ovarico, ma ci svela anche chi lo comanda (SNF2H) e ci suggerisce come potremmo neutralizzarlo. È un bell’esempio di come la ricerca di base possa gettare le fondamenta per future terapie innovative. E io, da appassionato, non posso che essere entusiasta di vedere cosa ci riserverà il futuro in questo campo!
Spero che questo viaggio nel mondo della ricerca sul cancro ovarico vi sia piaciuto. Continuate a seguirci per altre scoperte affascinanti!
Fonte: Springer