Tigeciclina: L’Antibiotico Amico-Nemico che Colpisce i Nostri Linfociti T
Introduzione: Antibiotici, Resistenza e… Effetti Collaterali Inaspettati?
Ragazzi, parliamoci chiaro: gli antibiotici sono stati una delle più grandi rivoluzioni della medicina. Farmaci come le tetracicline ci hanno salvato la pelle (letteralmente!) da infezioni batteriche che un tempo erano mortali. Pensate alla peste, alla malattia di Lyme… insomma, roba seria. Il problema è che i batteri sono furbi e sviluppano resistenze, costringendoci a cercare continuamente nuove armi o a modificare quelle esistenti. Ma c’è un aspetto che forse non tutti considerano: questi farmaci, progettati per colpire i batteri, come interagiscono con le *nostre* cellule?
Mi sono sempre chiesto se potessero esserci degli “effetti collaterali” nascosti, magari proprio sul nostro sistema immunitario. Dopotutto, alcuni antibiotici, come le stesse tetracicline o il cloramfenicolo, sono noti per causare problemi (tossicità a reni e fegato, soppressione del midollo osseo) ma anche per avere effetti anti-infiammatori, usati persino in malattie autoimmuni o neurodegenerative. Come mai? La risposta potrebbe nascondersi in minuscole strutture dentro le nostre cellule: i mitocondri.
Mitocondri: Le Centrali Energetiche (e un Bersaglio Inatteso)
Pensate ai mitocondri come alle centrali energetiche delle nostre cellule. Producono ATP, la “benzina” cellulare, attraverso un processo chiamato fosforilazione ossidativa (OXPHOS). Ma la cosa affascinante è che i mitocondri hanno una storia antichissima: discendono da batteri che miliardi di anni fa hanno iniziato a vivere in simbiosi dentro altre cellule. E indovinate un po’? Hanno mantenuto un loro piccolo DNA e, soprattutto, i loro ribosomi (i “mitoribosomi”) per produrre alcune proteine essenziali per l’OXPHOS.
Questi mitoribosomi assomigliano parecchio a quelli dei batteri. Ed ecco il punto: gli antibiotici che bloccano la sintesi proteica nei batteri legandosi ai loro ribosomi potrebbero, per errore, legarsi anche ai nostri mitoribosomi! Questo potrebbe interferire con la produzione di energia, specialmente in cellule che ne hanno un gran bisogno.
E quali cellule dipendono tantissimo dall’energia mitocondriale per attivarsi e moltiplicarsi? Esatto, i nostri linfociti T, i soldati del sistema immunitario! Quando devono combattere un’infezione o rispondere a uno stimolo, i linfociti T “accendono i motori” mitocondriali per sostenere la loro espansione e attività. Se un antibiotico blocca questo processo, cosa succede alla nostra risposta immunitaria?
Tigeciclina Sotto i Riflettori: Un Duro Colpo per i Linfociti T
Proprio per capirci di più, abbiamo deciso (io e il mio team di ricerca, s’intende!) di testare diversi antibiotici noti per colpire i ribosomi batterici, per vedere come influenzassero la sopravvivenza e la funzione dei linfociti T umani. Abbiamo usato sia linee cellulari (come le Jurkat T) sia cellule T primarie isolate da donatori sani.
Tra i vari composti testati (cloramfenicolo, doxiciclina e altre tetracicline come minociclina, ossiciclina), una in particolare ha mostrato una tossicità decisamente marcata sui linfociti T: la tigeciclina. La tigeciclina è una tetraciclina di terza generazione, più potente contro i batteri resistenti. Ebbene, a concentrazioni relativamente basse (parliamo di micromoli, μM), la tigeciclina riduceva significativamente la sopravvivenza sia delle cellule Jurkat T sia delle cellule mononucleate del sangue periferico (PBMC), che contengono i linfociti T. Curiosamente, altre cellule come le HeLa sembravano meno sensibili, suggerendo una certa specificità per le cellule immunitarie.
Ma la tigeciclina si limita a uccidere le cellule? No, fa molto di più (o meglio, di meno!). Abbiamo scoperto che:
- Inibisce specificamente la traduzione proteica mitocondriale: le cellule smettono di produrre le proteine codificate dal DNA mitocondriale, ma la produzione generale di proteine nel citoplasma continua quasi indisturbata.
- Riduce l’espressione delle subunità dei complessi I, III e IV della catena di trasporto degli elettroni (OXPHOS), quelli che contengono appunto componenti mitocondriali. I complessi II e V, codificati interamente dal nucleo, erano meno colpiti.
- Diminuisce la capacità delle cellule T di effettuare la respirazione mitocondriale (il consumo di ossigeno), fondamentale per produrre energia.
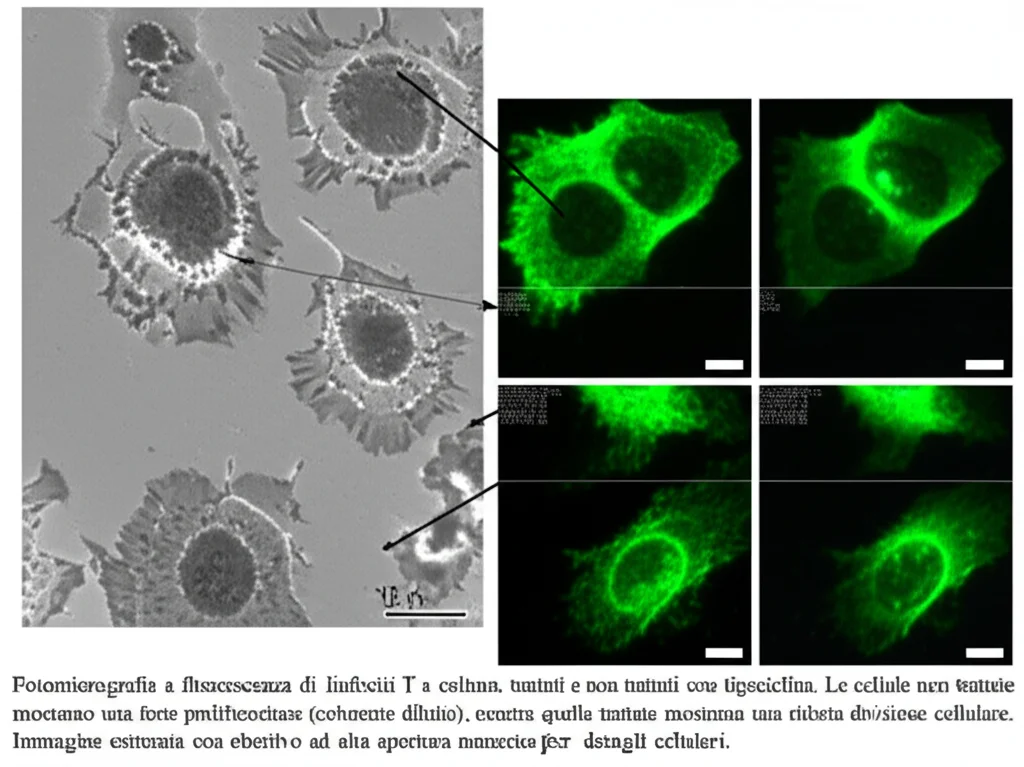
- Ostacola l’attivazione dei linfociti T (riducendo l’espressione del marcatore CD25) e ne blocca la proliferazione (la capacità di moltiplicarsi) in risposta a stimoli, un processo chiave per montare una risposta immunitaria efficace.
Questo effetto anti-proliferativo è stato osservato sia sui linfociti T CD4+ che CD8+, e anche su specifici sottotipi come le cellule T naïve e quelle della memoria centrale. Insomma, la tigeciclina sembra mettere KO la capacità dei linfociti T di “carburare” e rispondere.
Dentro il Mitoribosoma: La Scoperta dei Tre Siti di Legame
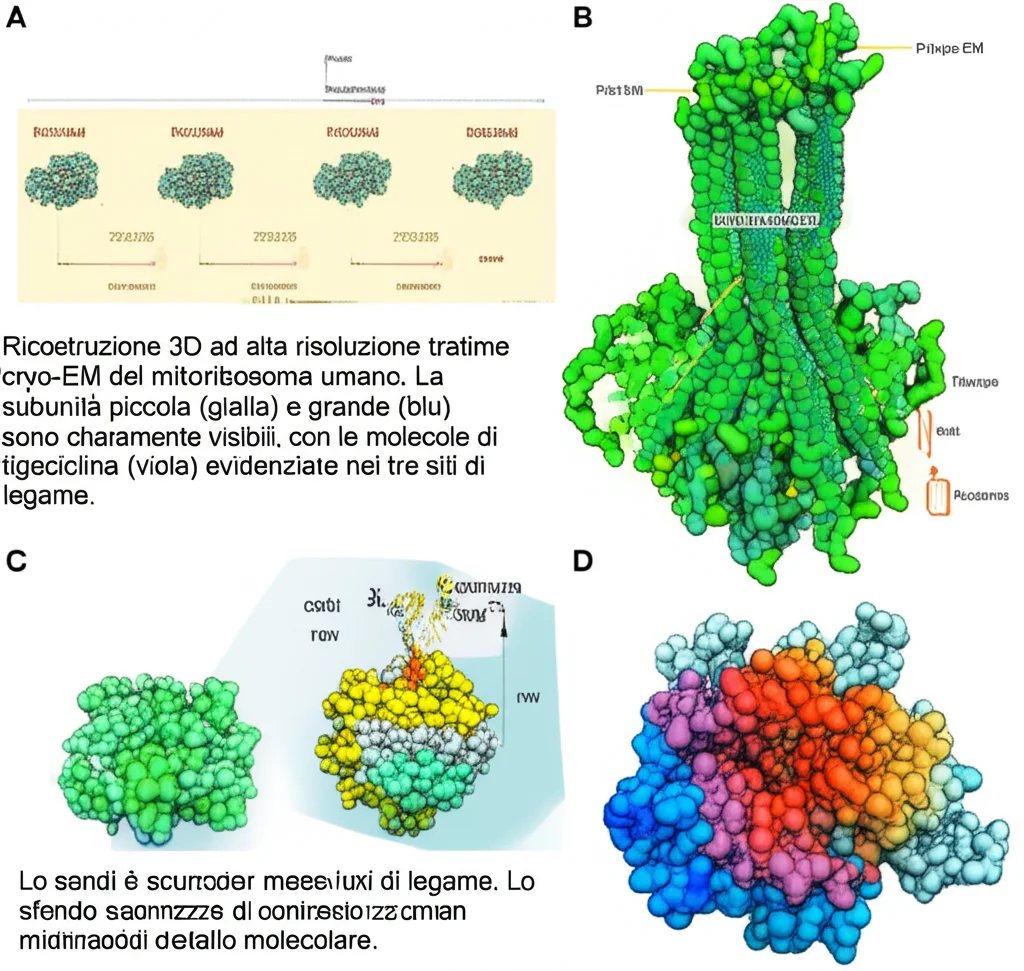
Ok, la tigeciclina è tossica per i linfociti T perché blocca i mitocondri. Ma *come* lo fa esattamente? Qual è il meccanismo molecolare? Per vederci chiaro, abbiamo usato una tecnica potentissima: la crio-microscopia elettronica (cryo-EM). Questa tecnica permette di “fotografare” le molecole a risoluzioni quasi atomiche, congelandole rapidamente.
Abbiamo isolato i mitoribosomi da cellule Jurkat T, li abbiamo incubati con la tigeciclina e poi li abbiamo analizzati al cryo-EM. E qui è arrivata la sorpresa più grande. Mentre negli studi sui batteri si era sempre visto che la tigeciclina (e le tetracicline in generale) si lega a un solo sito principale sul ribosoma (nella subunità piccola, il sito A, bloccando l’arrivo degli tRNA carichi di aminoacidi), nei mitoribosomi umani abbiamo trovato ben tre siti di legame distinti per la tigeciclina!
Ecco dove si piazza la tigeciclina nel nostro mitoribosoma:
- Sito sulla subunità piccola (mtSSU): Simile al sito A batterico, blocca l’ingresso dell’aminoacil-tRNA. Questo era atteso, data la conservazione di questa regione. La tigeciclina si lega all’rRNA 12S e coordina ioni magnesio (Mg2+), un meccanismo tipico delle tetracicline.
- Sito 1 sulla subunità grande (mtLSU site-1): Questo è stato del tutto inaspettato! La tigeciclina si infila in una tasca formata da eliche dell’rRNA 16S (in particolare l’elica 71), vicino a dove si posiziona il tRNA nel sito P. Per far spazio al farmaco, alcune parti dell’rRNA devono cambiare forma in modo significativo. Perché questo sito è presente qui e non nei batteri? Un’ipotesi affascinante è che nei batteri, questa regione dell’rRNA ha delle modifiche chimiche (metilazioni) che la rendono più rigida e impediscono il legame del farmaco. Nei nostri mitoribosomi, queste metilazioni mancano! Questo sito potrebbe interferire con il movimento dei tRNA durante la sintesi proteica o con il riciclo dei mitoribosomi.
- Sito 2 sulla subunità grande (mtLSU site-2), nel Centro Peptidil Transferasico (PTC): La tigeciclina si lega anche proprio nel cuore catalitico del ribosoma, dove si forma il legame peptidico tra gli aminoacidi. Anche se con un’occupazione leggermente inferiore rispetto agli altri due siti, la sua presenza qui è significativa. Potrebbe ostacolare la crescita della catena proteica nascente mentre esce dal tunnel ribosomiale. Curiosamente, altri antibiotici simili (come la sareciclina) si legano in questa zona nei batteri, ma la tigeciclina non era mai stata vista qui prima d’ora.
Cosa Significa Tutto Questo? Implicazioni e Prospettive Future
Questa scoperta dei tre siti di legame della tigeciclina sul mitoribosoma umano è fondamentale. Innanzitutto, fornisce una spiegazione molecolare dettagliata del perché questo antibiotico sia così tossico per i linfociti T (e potenzialmente per altre cellule che dipendono molto dall’OXPHOS). Il fatto che ci siano tre siti di legame, invece di uno solo come nei batteri, suggerisce che l’inibizione della traduzione mitocondriale sia particolarmente potente.
Questo potrebbe anche gettare nuova luce sugli effetti anti-infiammatori osservati con alcune tetracicline. Forse, parte di questo effetto è dovuto proprio alla capacità di “spegnere” l’attivazione e la proliferazione dei linfociti T, che sono attori chiave nell’infiammazione e nelle malattie autoimmuni.
Inoltre, conoscere esattamente come e dove questi farmaci interagiscono con i nostri mitoribosomi è cruciale per il futuro. Ci permette di:
- Progettare antibiotici migliori: Si potrebbero modificare le molecole esistenti per ridurre il legame ai mitoribosomi umani, mantenendo l’efficacia contro i batteri. Questo porterebbe a farmaci più sicuri e con meno effetti collaterali.
- Comprendere la tossicità: Aiuta a capire perché alcuni pazienti rispondono male a certi antibiotici e a identificare potenziali rischi, specialmente in contesti dove la funzione immunitaria è critica (infezioni, cancro, trapianti).
- Sfruttare l’inibizione mitocondriale: Paradossalmente, la capacità di inibire i mitocondri potrebbe essere sfruttata terapeuticamente. Già si studiano farmaci che bloccano l’OXPHOS come potenziali terapie anti-cancro, dato che molte cellule tumorali dipendono dai mitocondri. La tigeciclina stessa è stata studiata in questo contesto. Tuttavia, i nostri dati mostrano che cellule diverse (linfociti T vs HeLa vs Hek293) hanno sensibilità diverse, quindi l’approccio deve essere mirato e cauto.
È importante notare che i nostri esperimenti sono stati fatti in vitro. Le concentrazioni di tigeciclina che abbiamo trovato essere tossiche sono però rilevanti rispetto a quelle che si possono raggiungere nei tessuti dei pazienti trattati per infezioni batteriche. Serviranno studi futuri in vivo per capire come questi effetti si traducano nel complesso scenario di un organismo, considerando l’interazione tra sistema immunitario, patogeni e riparazione dei tessuti.
Insomma, la storia della tigeciclina e dei mitoribosomi ci ricorda che la biologia è complessa e interconnessa. Un farmaco pensato per un bersaglio può averne altri, con conseguenze inaspettate ma potenzialmente molto importanti, sia in negativo (tossicità) che, chissà, forse anche in positivo (nuove strategie terapeutiche). Capire questi meccanismi a livello molecolare è la chiave per sviluppare farmaci più intelligenti e sicuri.
Fonte: Springer