Cancro della Cistifellea: E Se la Soluzione Fosse Potenziare una Proteina? Ecco THBS1!
Ciao a tutti! Oggi voglio parlarvi di qualcosa di veramente affascinante che sta emergendo dalla ricerca oncologica, un campo in cui ogni piccolo passo avanti può fare un’enorme differenza. Parliamo di un nemico silenzioso e aggressivo: il cancro della cistifellea.
Sapete, la cistifellea è un piccolo organo, spesso trascurato, ma i tumori che la colpiscono sono tra i più comuni del tratto biliare e, purtroppo, hanno una prognosi spesso infausta. Perché? Beh, principalmente perché questo tipo di cancro è subdolo. Non dà sintomi specifici nelle fasi iniziali, e quando ci si accorge di qualcosa, spesso è troppo tardi per l’intervento chirurgico radicale, l’unica vera chance di cura. Per chi non può essere operato, resta la chemioterapia sistemica, spesso con risultati limitati. Insomma, c’è un bisogno disperato di nuove strategie.
La Caccia al Tesoro nei Geni: Come Abbiamo Trovato THBS1
Ed è qui che entra in gioco la ricerca più avanzata. Immaginate di avere a disposizione enormi archivi di dati genetici provenienti da tessuti tumorali. È quello che abbiamo fatto noi (e tanti altri ricercatori nel mondo!) utilizzando database pubblici come il Gene Expression Omnibus (GEO). Abbiamo setacciato i dati di espressione genica di tumori delle vie biliari, cercando di capire quali geni fossero “accesi” o “spenti” in modo anomalo rispetto ai tessuti sani.
Analizzando due specifici set di dati (GSE127897 e GSE132305), abbiamo identificato un bel po’ di geni con espressione alterata. Ma non basta. Bisogna capire come questi geni interagiscono tra loro, come in una complessa rete. Usando strumenti bioinformatici come il database STRING e software di visualizzazione come Cytoscape, abbiamo costruito questa rete e cercato i “nodi” centrali, i geni più importanti, quelli che sembrano tirare le fila.
E indovinate un po’? Tra i 10 geni “hub” più significativi è emerso un nome: Trombospondina-1, o più semplicemente THBS1. La cosa sorprendente? L’analisi indicava che nel cancro della cistifellea, l’espressione di THBS1 era bassa. Questo ci ha subito fatto drizzare le antenne: e se THBS1 fosse un gene “buono”, un oncosoppressore, che il tumore cerca di silenziare per poter crescere indisturbato?
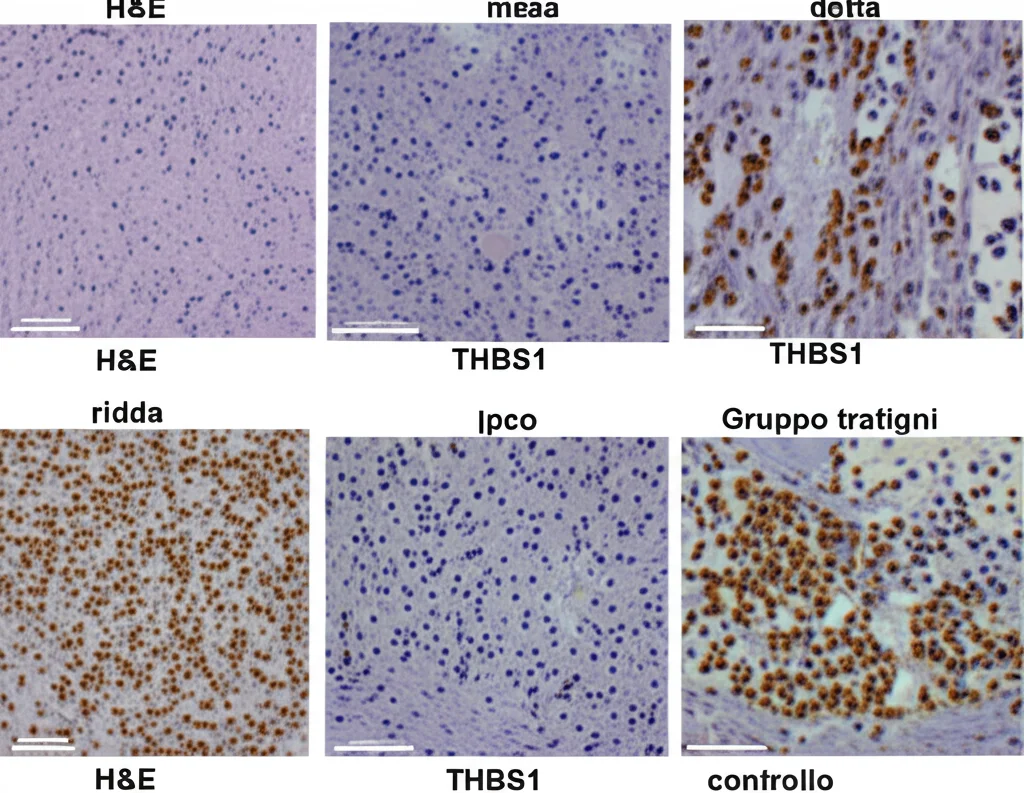
Per confermare, abbiamo anche analizzato campioni reali di tessuto: cinque casi di cancro della cistifellea e cinque di colecistite (infiammazione della cistifellea, usata come controllo “quasi sano”). L’immunoistochimica, una tecnica che colora le proteine nei tessuti, ha mostrato chiaramente che THBS1 era molto meno presente nei tessuti tumorali rispetto a quelli infiammati ma non cancerosi. Bingo! L’ipotesi sembrava reggere.

Mettere THBS1 alla Prova: Esperimenti in Laboratorio
Ma non ci siamo fermati alla bioinformatica e all’analisi dei tessuti. Dovevamo vedere THBS1 in azione. Cosa succede se prendiamo delle cellule di cancro della cistifellea (abbiamo usato una linea cellulare chiamata NOZ) e le “costringiamo” a produrre più THBS1?
Per farlo, abbiamo usato una tecnica chiamata trasfezione lentivirale. In pratica, abbiamo usato un virus modificato (reso innocuo) per inserire nelle cellule tumorali le istruzioni per produrre più THBS1. Abbiamo creato così un gruppo di cellule “potenziate” (THBS1-OE, over-expression) e le abbiamo confrontate con cellule di controllo (THBS1-NC, con un virus vuoto) e cellule normali non trattate.
I risultati sono stati davvero incoraggianti:
- Meno Proliferazione: Le cellule potenziate con THBS1 formavano molte meno colonie in coltura. In pratica, la loro capacità di moltiplicarsi era significativamente ridotta. È come se THBS1 mettesse un freno alla loro crescita sfrenata.
- Meno Mobilità e Invasività: Abbiamo fatto dei test specifici per vedere quanto le cellule si muovessero e invadessero. Nel test “wound healing” (guarigione della ferita), le cellule THBS1-OE erano molto più lente a richiudere un “graffio” fatto nello strato cellulare. Nei test Transwell, che misurano la capacità di attraversare una membrana (con o senza una matrice che simula il tessuto connettivo), le cellule potenziate passavano molto meno. Questo suggerisce che THBS1 ostacola la capacità del cancro di diffondersi e invadere i tessuti circostanti.
- Più Apoptosi (Morte Cellulare Programmata): Il cancro è bravo a evitare la morte. Ma THBS1 sembrava remare contro. Analizzando le proteine chiave coinvolte nell’apoptosi (usando una tecnica chiamata Western Blot), abbiamo visto che nelle cellule THBS1-OE aumentavano le proteine pro-apoptotiche (come Bax e Caspase-3) e diminuiva una proteina anti-apoptotica (Bcl-2). Anche la citometria a flusso ha confermato un tasso di apoptosi più alto in queste cellule. THBS1, quindi, sembra spingere le cellule tumorali verso l’autodistruzione.
La Prova del Nove: THBS1 Contro il Cancro nei Topi
Ok, i risultati in provetta erano promettenti, ma funzionerà anche in un organismo complesso? Per scoprirlo, siamo passati ai modelli animali. Abbiamo iniettato i tre gruppi di cellule (THBS1-OE, THBS1-NC, Controllo) sottocute in topi nudi (topi con un sistema immunitario deficitario, che non rigettano le cellule umane).
Abbiamo monitorato la crescita dei tumori per 30 giorni. Ebbene, i risultati hanno confermato quanto visto in vitro: i tumori formati dalle cellule THBS1-OE erano significativamente più piccoli e leggeri rispetto a quelli degli altri due gruppi. L’analisi immunoistochimica dei tumori asportati ha confermato l’alta espressione di THBS1 nel gruppo OE.
Ma c’è di più. Abbiamo esaminato i tumori al microscopio dopo averli colorati con ematossilina ed eosina (HeE staining). Abbiamo notato che nei tumori THBS1-OE c’erano molti meno nuovi vasi sanguigni (neoangiogenesi). Questo è importantissimo! I tumori hanno bisogno di nuovi vasi per nutrirsi e crescere. Il fatto che THBS1 riduca l’angiogenesi potrebbe essere uno dei meccanismi chiave con cui frena la progressione del cancro.
Cosa Ci Dice Tutto Questo? Il Futuro della Lotta al Cancro della Cistifellea
Mettendo insieme tutti i pezzi – l’analisi bioinformatica, gli esperimenti in vitro e quelli in vivo – emerge un quadro piuttosto chiaro: la Trombospondina-1 (THBS1) agisce come un gene oncosoppressore nel cancro della cistifellea. La sua bassa espressione sembra favorire la malattia, mentre la sua sovraespressione ne inibisce la progressione agendo su più fronti: proliferazione, migrazione, invasione, apoptosi e angiogenesi.
Questo apre scenari davvero interessanti. THBS1 potrebbe diventare:
- Un biomarcatore: Misurare i livelli di THBS1 potrebbe aiutare nella diagnosi precoce o nella prognosi del cancro della cistifellea.
- Un bersaglio terapeutico: Si potrebbero sviluppare farmaci o strategie (magari terapie geniche?) per aumentare i livelli o l’attività di THBS1 nelle cellule tumorali, offrendo così una nuova arma contro questa malattia difficile.
Certo, la strada è ancora lunga. Questi sono studi preclinici, e serviranno ulteriori ricerche per confermare questi risultati e tradurli in terapie efficaci e sicure per i pazienti. Ma è un passo avanti significativo. Aver identificato un attore chiave come THBS1, che sembra mettere i bastoni tra le ruote a questo tumore aggressivo, ci dà una nuova speranza e una direzione chiara per la ricerca futura. È la bellezza della scienza: pezzo dopo pezzo, costruiamo la conoscenza che un giorno potrebbe salvare vite. E io sono entusiasta di poter condividere queste scoperte con voi!
Fonte: Springer