DNA Mitocondriale in Fuga: Svelato il Meccanismo Segreto dell’Infiammazione Intestinale Post-Ischemia!
Ciao a tutti! Oggi voglio parlarvi di qualcosa di affascinante che sta emergendo dalla ricerca biomedica, un meccanismo intricato che riguarda il nostro intestino e come reagisce a situazioni di stress estremo, come l’ischemia-riperfusione. Immaginate una situazione critica, magari durante un intervento chirurgico complesso o a causa di un blocco del flusso sanguigno: l’intestino, uno degli organi più sensibili del nostro corpo, soffre per la mancanza di ossigeno (ischemia) e poi subisce un ulteriore “shock” quando il sangue torna a fluire (riperfusione). Questo fenomeno, noto come danno da ischemia-riperfusione intestinale (IIR), è una condizione clinica seria e purtroppo comune, che può portare a complicazioni gravi come la sindrome da risposta infiammatoria sistemica (SIRS) e la disfunzione multiorgano (MODS).
Nonostante i progressi nelle cure perioperatorie, l’IIR rimane un osso duro, associato a prognosi infauste e degenze ospedaliere prolungate. Ma cosa scatena esattamente questa tempesta infiammatoria nell’intestino? È qui che la nostra ricerca entra in gioco, cercando di svelare i meccanismi molecolari nascosti.
Il Danno da Ischemia-Riperfusione Intestinale: Un Nemico Visibile al Microscopio
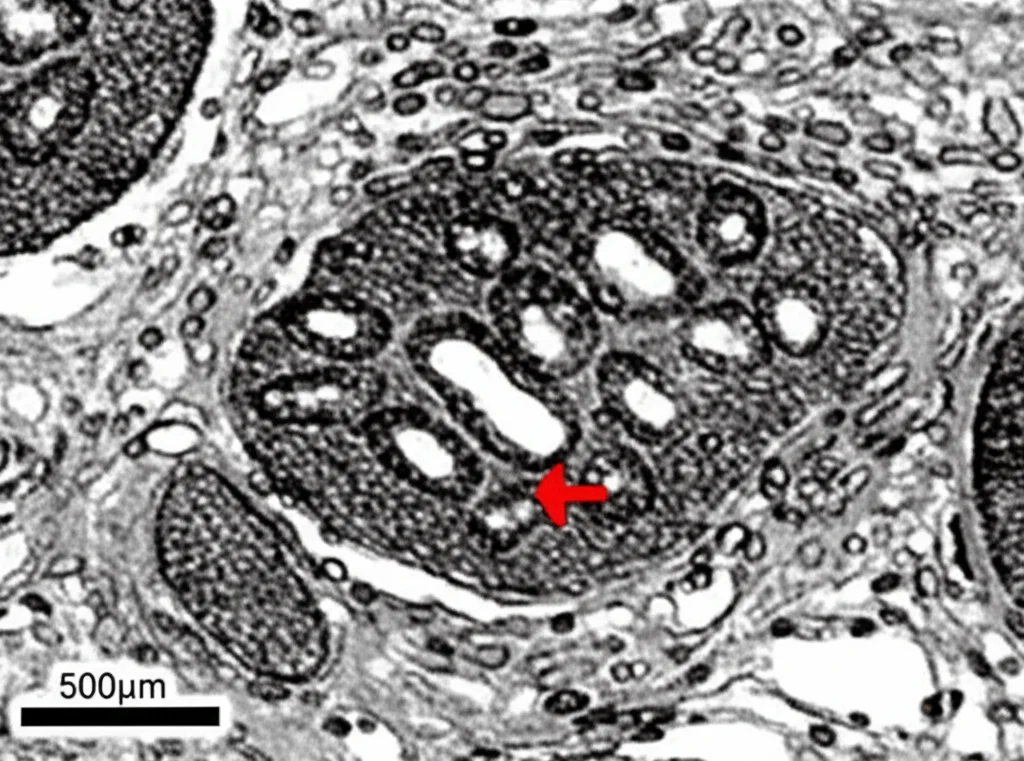
Per capire meglio, abbiamo utilizzato modelli sperimentali, sia su topi che in vitro (usando cellule intestinali umane HT-29 e organoidi di intestino tenue – delle mini-versioni dell’intestino coltivate in laboratorio!). Quello che abbiamo osservato è piuttosto chiaro: l’IIR provoca un forte stress ossidativo e scatena una potente risposta infiammatoria. Guardando al microscopio i tessuti intestinali dopo IIR, abbiamo visto danni evidenti: i villi intestinali, quelle delicate strutture che assorbono i nutrienti, apparivano gonfi (edematosi), distaccati, a volte addirittura spezzati. Anche a livello cellulare, usando la microscopia elettronica a trasmissione, abbiamo notato alterazioni preoccupanti: mitocondri (le centrali energetiche delle cellule) gonfi, pieni di vacuoli, con le loro creste interne distorte o scomparse. Questo è un segno inequivocabile che i mitocondri sono in sofferenza.
Abbiamo anche misurato i livelli di marcatori di danno e infiammazione: i punteggi di danno tissutale (secondo la scala di Chiu) erano più alti, così come i livelli di lattato deidrogenasi (LDH) e malondialdeide (MDA), entrambi indicatori di stress ossidativo e danno cellulare. Inoltre, l’espressione di geni infiammatori come Il1, Tnf e Ifn-β era significativamente aumentata. Tutto questo conferma che l’IIR è una vera e propria battaglia a livello cellulare e tissutale. Ma qual è l’interruttore che accende questa infiammazione così dannosa?
DNA Mitocondriale Fuori Posto: L’Innesco dell’Infiammazione
Qui le cose si fanno interessanti. Abbiamo notato che parallelamente al danno mitocondriale, si attivava una specifica via di segnalazione infiammatoria chiamata via cGAS-STING. Questa via è normalmente deputata a riconoscere DNA “fuori posto” nel citoplasma della cellula, come quello virale o batterico, e a scatenare una risposta immunitaria. La nostra ipotesi? Che il DNA contenuto nei mitocondri danneggiati (il cosiddetto mtDNA) potesse fuoriuscire nel citoplasma e attivare proprio questa via cGAS-STING, come un falso allarme che però provoca danni reali.
Per verificare questa idea, abbiamo fatto diversi esperimenti.
- Abbiamo visto che nelle cellule HT-29 sottoposte a ipossia/riossigenazione (HR, il modello in vitro dell’IIR), la via cGAS-STING si attivava e il sensore cGAS si avvicinava ai mitocondri.
- Introducendo mtDNA purificato direttamente nelle cellule, abbiamo visto che questo era sufficiente ad attivare la via STING e a peggiorare il danno cellulare indotto da HR.
- Al contrario, usando un inibitore specifico di cGAS (RU.521), siamo riusciti a bloccare l’attivazione della via e a ridurre il danno cellulare.
- Ancora più interessante: abbiamo creato delle cellule HT-29 “svuotate” del loro mtDNA (chiamate cellule P0) usando etidio bromuro. Ebbene, in queste cellule prive di mtDNA, l’HR non riusciva più ad attivare la via cGAS-STING e il danno cellulare era ridotto!
Questi risultati ci dicono in modo abbastanza convincente che la fuoriuscita di mtDNA dai mitocondri danneggiati è un evento chiave che innesca l’attivazione della via cGAS-STING e contribuisce al danno infiammatorio nell’IIR. Abbiamo anche provato a iniettare mtDNA direttamente nei topi durante l’IIR: questo ha peggiorato ulteriormente il danno intestinale e aumentato i livelli di infiammazione, confermando il ruolo dannoso del mtDNA “libero”.
TFAM: Il Guardiano Perduto del DNA Mitocondriale
Ma perché il mtDNA fuoriesce durante l’IIR? C’è un colpevole? Analizzando i dati di espressione genica (RNA sequencing), abbiamo notato che l’IIR era associato a una disregolazione dei geni legati al mtDNA e, in particolare, a una significativa riduzione dell’espressione di una proteina chiamata TFAM (Fattore di Trascrizione Mitocondriale A). TFAM è fondamentale: non solo regola la trascrizione del mtDNA, ma agisce anche come una sorta di “impacchettatore” e protettore, mantenendo stabile la struttura del DNA mitocondriale.
La nostra ipotesi successiva è stata: la riduzione di TFAM durante l’IIR rende il mtDNA instabile e più incline a fuoriuscire? Per testarlo, abbiamo fatto l’opposto: abbiamo aumentato artificialmente i livelli di TFAM nelle cellule HT-29 prima di sottoporle a HR. I risultati sono stati incoraggianti:
- La sovraespressione di TFAM ha ridotto l’accumulo di mtDNA nel citoplasma.
- Ha inibito l’attivazione della via cGAS-STING.
- Ha diminuito i livelli di lattato e MDA (indicatori di danno).
- Ha aumentato la vitalità cellulare dopo HR.
Questo ci suggerisce fortemente che la downregulation di TFAM durante l’IIR è un evento cruciale che favorisce la fuoriuscita di mtDNA e l’attivazione della cascata infiammatoria cGAS-STING. TFAM emerge quindi come un potenziale protettore la cui perdita contribuisce attivamente al danno.
Bloccare STING: Una Strategia Vincente?
Se la via cGAS-STING è così centrale nel causare il danno, bloccarla potrebbe essere una buona strategia terapeutica? Per rispondere a questa domanda, abbiamo utilizzato topi geneticamente modificati privi della proteina STING (topi STING knockout, STING−/−).
I risultati sono stati notevoli:
- I topi STING−/− sottoposti a IIR mostravano una significativa riduzione dell’infiammazione (minore attivazione di TBK1, un partner di STING, e minori livelli di citochine infiammatorie).
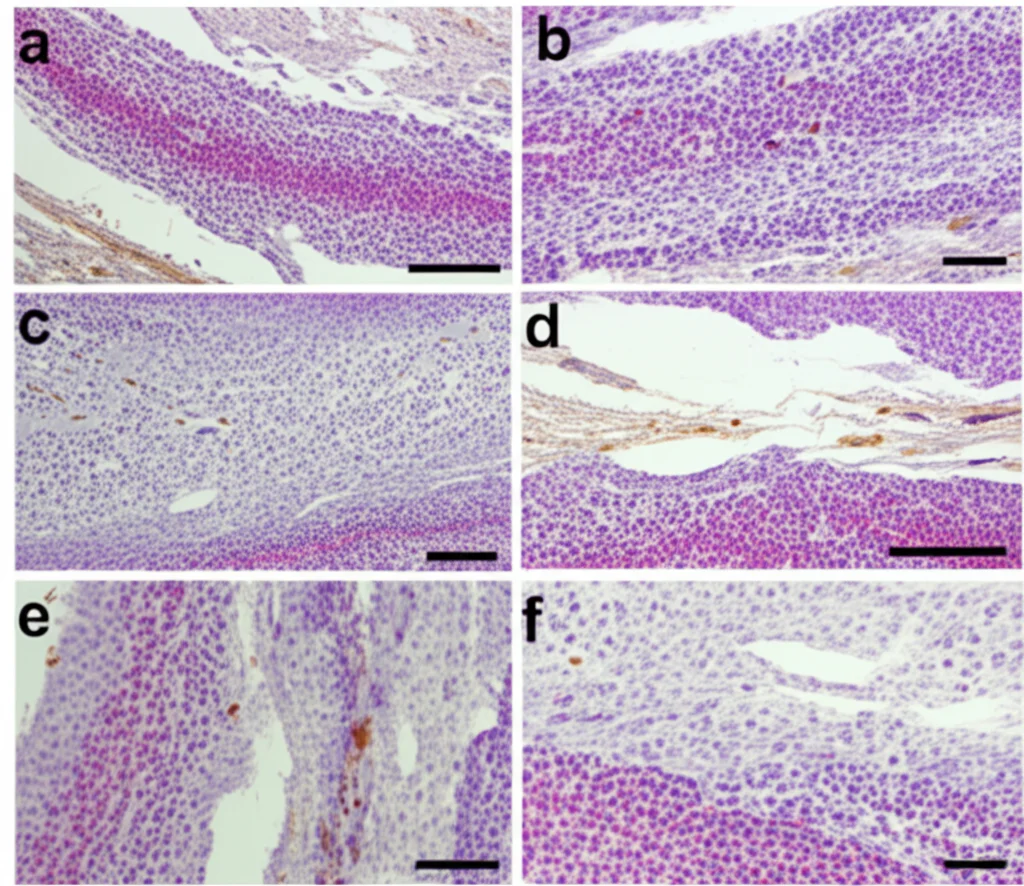
- Presentavano meno danno tissutale all’intestino (punteggi Chiu più bassi, meno cellule apoptotiche rilevate con il test TUNEL).
- Avevano livelli più bassi di stress ossidativo (LDH e MDA).
- Soprattutto, avevano un tasso di sopravvivenza a 72 ore dall’IIR significativamente più alto rispetto ai topi normali!
Abbiamo confermato questi risultati anche negli organoidi intestinali: quelli derivati da topi STING−/− crescevano meglio e mostravano meno danno dopo HR rispetto a quelli normali. Questo dimostra che bloccare STING ha un effetto protettivo concreto, non solo a livello molecolare ma anche funzionale e sulla sopravvivenza.
Un Nuovo Bersaglio Terapeutico all’Orizzonte?
Mettendo insieme tutti i pezzi, il nostro studio dipinge un quadro più chiaro di cosa succede durante l’ischemia-riperfusione intestinale. Sembra proprio che ci sia un asse cruciale: IIR → Riduzione di TFAM → Instabilità e fuoriuscita di mtDNA → Attivazione di cGAS-STING → Infiammazione e Danno Tissutale.
Questa scoperta è importante non solo perché ci aiuta a capire meglio la malattia, ma soprattutto perché apre nuove prospettive terapeutiche. Se riusciamo a trovare modi per:
- Mantenere alti i livelli di TFAM durante l’IIR.
- Impedire la fuoriuscita di mtDNA.
- Inibire specificamente cGAS o STING.
potremmo avere nuove armi per combattere il danno da IIR e migliorare l’esito per i pazienti. Certo, c’è ancora strada da fare, soprattutto per tradurre queste scoperte dai modelli di laboratorio alla clinica (ad esempio, i nostri esperimenti in vitro potrebbero non catturare tutta la complessità dell’ambiente in vivo), ma la direzione sembra promettente.
Capire questi meccanismi molecolari è fondamentale. È come smontare un orologio complicato per vedere come funzionano gli ingranaggi: solo così possiamo sperare di ripararlo quando si rompe. E nel caso dell’IIR, ripararlo potrebbe significare salvare vite.
Fonte: Springer