Svelati i Segreti Molecolari dello Sviluppo Cerebrale Umano: Un Viaggio nei Meta-Moduli
Ciao a tutti! Oggi voglio portarvi con me in un viaggio affascinante nel cuore di uno dei misteri più grandi: come si sviluppa il cervello umano, in particolare la nostra complessa corteccia cerebrale. Sapete, quella parte espansa che ci distingue da altri mammiferi e ci regala capacità come il giudizio, la percezione e il linguaggio. È un processo di una complessità sbalorditiva, e capire come funziona non è solo pura curiosità scientifica, ma è cruciale per comprendere anche cosa va storto in disturbi del neurosviluppo e psichiatrici.
Negli ultimi anni, grazie alle tecnologie di trascrittomica a singola cellula, abbiamo iniziato a “mappare” i diversi tipi di cellule presenti nel cervello in sviluppo. È come creare un atlante cellulare. Fantastico, vero? Però, ogni singolo studio, per quanto prezioso, ha i suoi limiti. Spesso si basa su pochi campioni, magari non copre tutte le regioni corticali o tutte le fasi dello sviluppo. Come fare, allora, per avere un quadro più completo e robusto?
L’Unione Fa la Forza: Nascono i Meta-Atlanti
Qui entra in gioco la nostra idea. E se unissimo le forze? Se prendessimo tutti questi “atlanti” individuali, pubblicati da diversi laboratori (un grazie enorme a tutti loro!), e li integrassimo in un unico, gigantesco **meta-atlante**? È quello che abbiamo fatto! Abbiamo messo insieme ben sette dataset sullo sviluppo della corteccia umana (parliamo di quasi 600.000 cellule!) e, parallelamente, sedici dataset sulla corteccia adulta (oltre 2,6 milioni di cellule!). Un lavoro immane, ma ne è valsa la pena.
Integrare dati così diversi non è banale, ci sono variazioni tecniche tra studi che possono “sporcare” il segnale biologico. Per superare questo ostacolo, non ci siamo limitati a classificare le cellule basandoci sui soliti geni “marcatore”. Abbiamo sviluppato una strategia più sofisticata, basata sulla **co-espressione genica**, per identificare gruppi di geni che lavorano insieme, come piccole squadre operative all’interno delle cellule. Li abbiamo chiamati **meta-moduli**.
Immaginate di analizzare ogni singolo campione individuale, identificare i gruppi di geni più caratteristici al suo interno, e poi cercare quali di questi gruppi si ritrovano costantemente anche negli altri campioni, attraverso diversi studi ed età. Questi sono i nostri meta-moduli: reti di geni la cui associazione è così forte da resistere al “rumore” tecnico. Ne abbiamo identificati 225 nello sviluppo e 299 nell’adulto. Ognuno racconta una storia, un processo biologico specifico: dalla funzione delle sinapsi alla risposta immunitaria, dalla divisione cellulare al destino stesso delle cellule.
Dallo Sviluppo all’Età Adulta: Un Cambiamento di Strategia
Una delle scoperte più intriganti è stata osservare come questi meta-moduli caratterizzano le cellule nelle diverse fasi della vita. Durante lo sviluppo, le cellule, specialmente i progenitori che daranno origine ai vari tipi neuronali, sono caratterizzate da *combinazioni* uniche di diversi meta-moduli. È come se stessero “esplorando” diverse possibilità prima di prendere una decisione definitiva sul loro destino.
Nell’adulto, invece, il quadro cambia. I tipi cellulari maturi sono spesso definiti da uno o due meta-moduli estremamente specifici. È come se, una volta presa la decisione, la cellula si concentrasse su un programma genetico ben definito. Questo conferma osservazioni precedenti: c’è un’enorme “rifinitura” trascrizionale tra lo sviluppo e l’età adulta. Le sottili differenze tra le cellule in sviluppo si “affilano” e diventano più marcate nel cervello maturo. Questo ci dice una cosa fondamentale: per capire davvero come si specifica il destino di una cellula, dobbiamo guardare allo sviluppo con lenti “evolutive”, non partire dall’adulto dove il paesaggio è già molto diverso.
Validazione: Dai Dati alla Realtà Biologica
Bello avere tanti dati e moduli, ma funzionano? Rappresentano processi reali? Per verificarlo, siamo andati a “vedere” nel tessuto cerebrale umano in sviluppo. Abbiamo usato tecniche di immunostaining per colorare specifiche proteine codificate dai geni dei nostri meta-moduli e vedere se si trovavano nei tipi cellulari e nelle regioni previste dai nostri dati.
Ad esempio, abbiamo identificato il **Meta-Modulo 156**, attivo soprattutto nelle cellule progenitrici radiali (le “mamme” di molti neuroni e cellule gliali) e la cui attività aumenta man mano che lo sviluppo procede verso la produzione di cellule gliali (gliogenesi). Contiene geni come QKI, noto marcatore pan-gliale, ma anche altri meno scontati come PDLIM5 e SALL1. Ebbene, colorando sezioni di corteccia fetale, abbiamo visto proprio QKI, PDLIM5 e SALL1 co-espressi nelle zone ricche di progenitori, confermando le previsioni del modulo! Questo modulo potrebbe rappresentare un segnale chiave per il passaggio dalla neurogenesi alla gliogenesi.
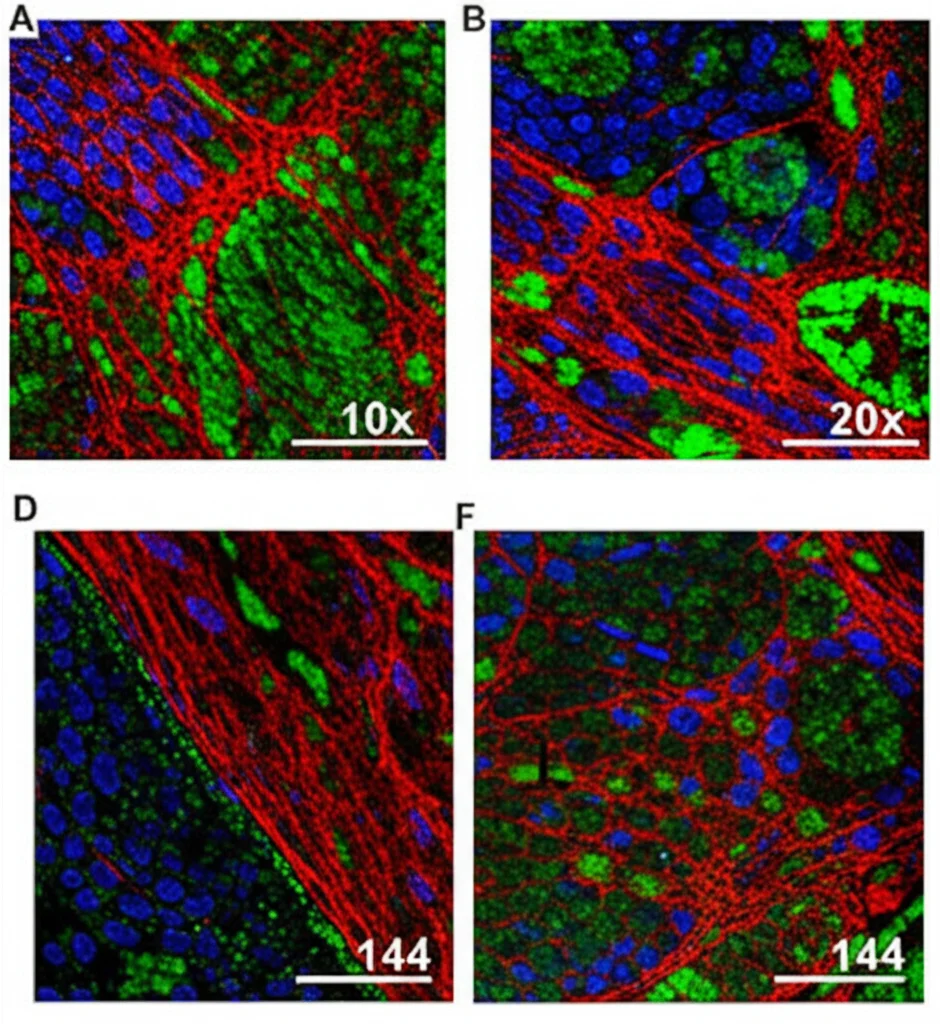
Abbiamo fatto lo stesso per altri moduli legati a specifici sottotipi neuronali. Il **Modulo 134**, ad esempio, attivo in neuroni eccitatori destinati allo strato IV della corteccia adulta, mostrava co-espressione dei suoi membri (come ADAM33 e HS6ST2) proprio nelle zone superiori della placca corticale in sviluppo. Il **Modulo 144**, invece, legato a interneuroni (i neuroni inibitori) che esprimono CCK e destinati allo strato I, vedeva i suoi membri (come VGAT e ZBTB16) co-localizzati proprio nello strato più superficiale della corteccia fetale. È incredibile come questi moduli, raggruppando geni magari mai connessi prima, ci rivelino pattern spazio-temporali così precisi!
Un Caso Studio Approfondito: Il Mistero del Modulo 20 e dei Neuroni Profondi
Voglio soffermarmi su un modulo che ci ha particolarmente affascinato: il **Meta-Modulo 20**. La sua attività aumenta costantemente durante lo sviluppo, ma in modo specifico nei neuroni eccitatori degli strati profondi della corteccia (quelli che si formano per primi). Nell’adulto, la sua attività è quasi esclusiva di questi neuroni profondi, in particolare quelli legati a un fattore di trascrizione “maestro” per questo destino cellulare: FEZF2.
La cosa curiosa è che FEZF2 stesso *non* fa parte del Modulo 20! Eppure, l’attività del modulo sembra strettamente legata alla presenza, almeno storica, di FEZF2. La nostra ipotesi? Che FEZF2, agendo precocemente, inneschi l’attivazione del Modulo 20, che poi porta a compimento la specificazione di quel particolare tipo di neurone profondo.
Andando a spulciare tra i geni del Modulo 20, abbiamo notato che quasi la metà sono potenziali bersagli diretti di FEZF2 (studiati nel topo, ma è un indizio importante). E tra questi bersagli, c’è un altro fattore di trascrizione: TSHZ3, recentemente implicato nell’autismo. Analizzando i dati temporali, abbiamo visto uno schema intrigante: prima si attiva FEZF2, poi c’è un picco transitorio di TSHZ3, e infine aumenta l’attività del Modulo 20. Sembra una staffetta molecolare! Abbiamo confermato con l’immunostaining che FEZF2 e TSHZ3 sono co-espressi nelle cellule giuste al momento giusto nella corteccia umana in sviluppo.
Esperimenti Funzionali: I Chimeroidi Corticali
Per testare questa “staffetta” molecolare, siamo passati all’azione in laboratorio. Abbiamo usato un modello avanzato: i **chimeroidi corticali**. Si tratta di organoidi cerebrali (mini-cervelli in provetta) creati combinando cellule staminali provenienti da diversi donatori. Questo aumenta la robustezza dei risultati. In questi chimeroidi, abbiamo usato delle tecniche per “spegnere” (knockdown) specificamente FEZF2, TSHZ3, o entrambi contemporaneamente.
I risultati sono stati netti. Spegnere entrambi i geni ha causato una riduzione significativa dei neuroni degli strati profondi e anche dei loro progenitori immediati (IPC), mentre aumentavano le cellule progenitrici radiali “indifferenziate”. È come se avessimo bloccato il processo di differenziamento. Analizzando il trascrittoma di queste cellule a livello di singola cellula (con una tecnica chiamata PIP-seq), abbiamo visto che l’attività del Modulo 20 diminuiva drasticamente, confermando il suo legame con FEZF2 e TSHZ3.
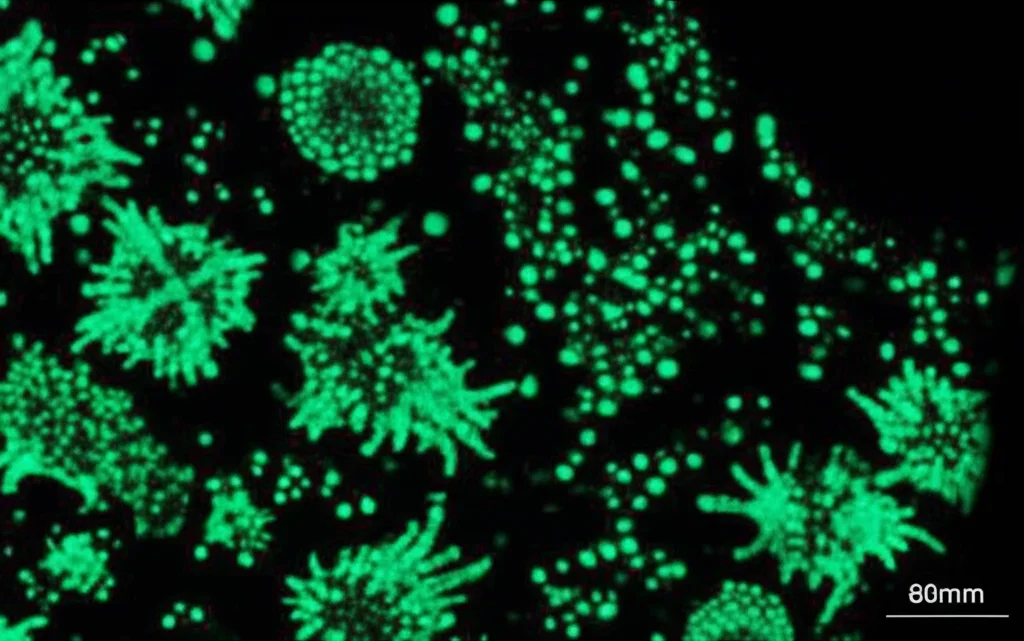
Ma non è finita qui. Volevamo capire *come* FEZF2 e TSHZ3 collaborano. Abbiamo quindi usato una tecnica multi-omica che guarda sia all’espressione genica (RNA) sia all’accessibilità della cromatina (ATAC-seq) nelle stesse cellule dei nostri chimeroidi. È emerso un quadro affascinante: sembra che FEZF2 agisca principalmente come attivatore trascrizionale, dando l’impulso iniziale. TSHZ3, invece, sembra cruciale per “aprire” la cromatina, rendendo fisicamente accessibili i geni del Modulo 20 (e persino FEZF2 stesso, anche se poi altri fattori ne causano il declino) affinché possano essere trascritti. Una collaborazione finemente regolata!
Conclusioni e Prospettive
Questo lavoro dimostra la potenza dell’integrazione di dati su larga scala. I nostri meta-atlanti e i meta-moduli che ne derivano sono una risorsa preziosa (e accessibile a tutti tramite specifici browser online!) per esplorare la complessità dello sviluppo corticale umano. Ci hanno permesso di:
- Identificare reti geniche robuste che definiscono tipi cellulari e processi di sviluppo.
- Capire meglio le differenze tra lo stato “fluido” dello sviluppo e quello “definito” dell’adulto.
- Validare previsioni computazionali con esperimenti mirati su tessuto umano e modelli in vitro avanzati.
- Svelare meccanismi molecolari specifici, come la collaborazione tra FEZF2 e TSHZ3 nella specificazione dei neuroni profondi, con potenziali implicazioni per la comprensione di disturbi come l’autismo.
È solo l’inizio, ovviamente. Questi meta-moduli aprono la porta a innumerevoli altre domande e indagini funzionali. La nostra speranza è che questo approccio e questa risorsa aiutino la comunità scientifica a fare passi avanti nella comprensione di come si costruisce il nostro incredibile cervello e cosa succede quando questo processo delicato incontra degli ostacoli.
Fonte: Springer