Stress Cellulare: La Chiave Inaspettata per Potenziare il Trapianto di Cellule Staminali?
Ciao a tutti! Oggi voglio parlarvi di qualcosa di veramente affascinante che sta emergendo nel campo della medicina rigenerativa, in particolare riguardo ai trapianti di cellule staminali ematopoietiche (CSE). Sapete, quelle cellule potentissime che danno origine a tutte le cellule del nostro sangue e che sono una speranza concreta per curare leucemie, linfomi e altre malattie gravi.
Il punto cruciale per un trapianto di successo è raccogliere abbastanza di queste preziose cellule. Tradizionalmente, si prelevano dal midollo osseo, ma oggi si preferisce raccoglierle dal sangue periferico. Perché? È più semplice, meno invasivo per il donatore e spesso porta a risultati migliori per il paziente. C’è solo un “piccolo” problema: in condizioni normali, le CSE se ne stanno belle tranquille nel loro “nido”, il midollo osseo, e solo pochissime circolano nel sangue. Troppo poche per un trapianto efficace.
La Sfida della Mobilizzazione: Far Uscire le Staminali dal Nido
Per farle uscire dal midollo e farle riversare nel sangue periferico – un processo chiamato mobilizzazione – si usano farmaci specifici. Il più comune è il G-CSF (fattore di crescita granulocitario), a volte combinato con un altro farmaco chiamato Plerixafor. Funzionano, certo, ma non sempre alla perfezione. Pensate che una percentuale non trascurabile di pazienti (dal 10% fino al 60% in alcuni casi!) non riesce a mobilizzare abbastanza cellule, anche dopo giorni di trattamento e procedure multiple. Questo significa più stress per il donatore o il paziente, costi maggiori e, a volte, l’impossibilità di procedere con il trapianto. C’è un bisogno disperato di strategie più rapide, efficaci e con meno effetti collaterali.
Ed è qui che entra in gioco la nostra ricerca, con un protagonista un po’ inaspettato: lo stress cellulare. Sì, avete capito bene. Di solito pensiamo allo stress come a qualcosa di negativo, ma recenti studi suggeriscono che un *lieve* stress a livello del reticolo endoplasmatico (RE) – una parte fondamentale della cellula – potrebbe addirittura avere effetti positivi sulle CSE, aiutandole a mantenersi giovani, attive e resistenti.
L’Ipotesi Sorprendente: Sfruttare lo Stress a Fin di Bene
Il reticolo endoplasmatico è un po’ la fabbrica e il magazzino della cellula, specialmente per le proteine e il calcio. Quando qualcosa non va per il verso giusto (ad esempio, proteine mal ripiegate si accumulano), la cellula entra in uno stato di “stress del RE”. Un meccanismo chiave nel controllo del calcio all’interno del RE è una pompa chiamata SERCA (Sarco/endoplasmic reticulum Ca²⁺-ATPase). Questa pompa lavora incessantemente per riportare il calcio dal citoplasma all’interno del RE, mantenendo l’equilibrio.
Ci siamo chiesti: cosa succederebbe se interferissimo con questa pompa SERCA? Potremmo indurre un lieve stress del RE e, magari, influenzare la capacità delle CSE di restare ancorate al midollo osseo? L’idea era che bloccando SERCA, avremmo alterato i livelli di calcio e innescato una serie di segnali che, alla fine, avrebbero potuto “sganciare” le cellule staminali.
Cosa Abbiamo Scoperto: La Prova sul Campo (anzi, in Laboratorio e nei Topi)
Per testare la nostra ipotesi, abbiamo usato diversi strumenti:
- Abbiamo trattato cellule in laboratorio (linee cellulari come le Jurkat e cellule staminali primarie isolate da topi) con sostanze note per indurre stress del RE, tra cui un inibitore specifico di SERCA chiamato BHQ.
- Abbiamo misurato cosa succedeva a un recettore chiave sulla superficie delle CSE, chiamato CXCR4. Questo recettore è fondamentale: legandosi alla sua molecola partner (SDF-1) presente nel midollo osseo, tiene le CSE ancorate al loro posto. Se l’espressione di CXCR4 diminuisce, le cellule sono più propense a migrare.
- Abbiamo condotto esperimenti su topi (modello C57Bl/6), iniettando BHQ e poi andando a contare quante CSE si trovavano nel loro sangue periferico.
- Abbiamo anche provato a combinare BHQ con il classico G-CSF per vedere se potevamo ottenere un effetto sinergico.
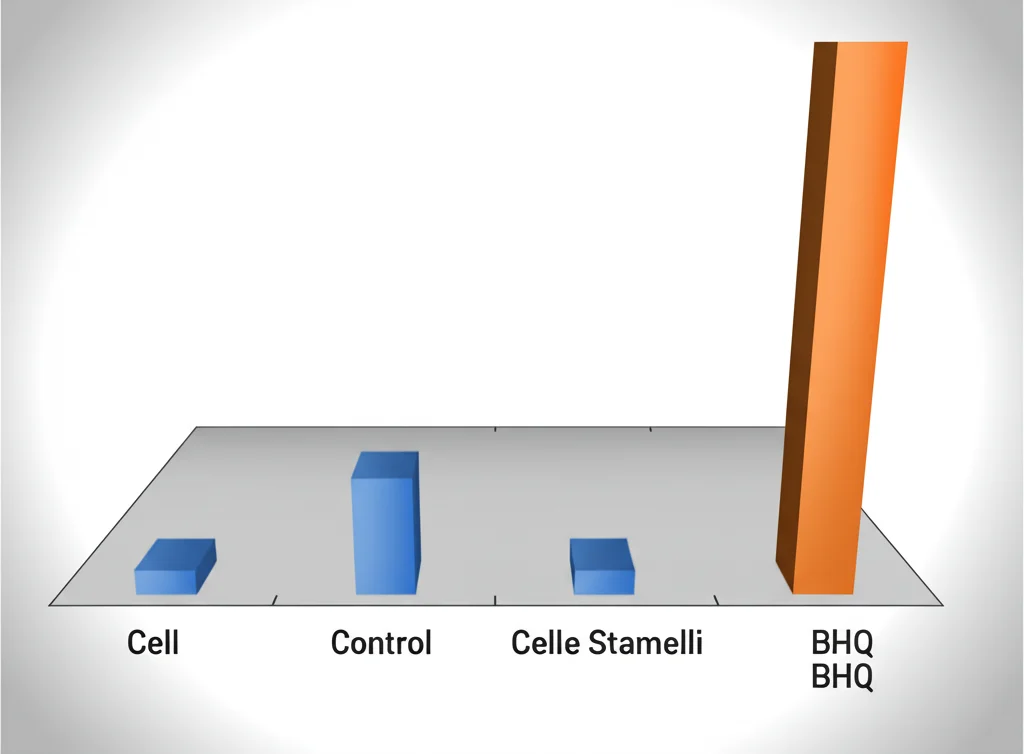
I risultati sono stati davvero incoraggianti! Abbiamo visto che trattare le cellule con BHQ (e altri induttori di stress del RE) riduceva significativamente la quantità di recettore CXCR4 sulla loro superficie. E questo non solo nelle linee cellulari, ma anche nelle preziose CSE primarie di topo.
Ma la prova del nove è arrivata dagli esperimenti in vivo: i topi trattati con una singola iniezione di BHQ mostravano un numero decisamente maggiore di CSE circolanti nel sangue rispetto ai topi di controllo! Non solo: quando abbiamo combinato BHQ con il G-CSF, l’effetto di mobilizzazione era ancora più potente rispetto al solo G-CSF. Bingo! Sembrava proprio che indurre un lieve stress del RE tramite l’inibizione di SERCA fosse una strategia efficace per promuovere la mobilizzazione delle CSE.
Il Meccanismo Svelato: Una Cascata di Segnali Innescata dal Calcio
Ok, funziona, ma come? Siamo andati più a fondo per capire la catena di eventi molecolari. Inibire SERCA con BHQ, come previsto, causa un rilascio di calcio dal reticolo endoplasmatico nel citoplasma. Questo cambiamento nei livelli di calcio intracellulare mette in moto una cascata di segnali. Abbiamo scoperto che questo porta all’inibizione di un enzima chiamato CaMKII (Calmodulin-dependent protein kinase II).
Perché è importante? Perché CaMKII, a sua volta, regola l’attività di un fattore di trascrizione chiamato STAT3. Quando CaMKII è meno attivo, anche STAT3 lo è. E indovinate un po’? STAT3 è noto per controllare l’espressione del gene CXCR4. Meno STAT3 attivo significa meno produzione della proteina CXCR4.
Ma non è tutto! Abbiamo anche osservato che lo stress indotto da BHQ portava a un aumento della fosforilazione di CXCR4 su un sito specifico (S339). Questa modifica chimica è un segnale che dice alla cellula di “internalizzare” il recettore, togliendolo dalla superficie.
Quindi, il meccanismo sembra essere duplice:
- Meno produzione di CXCR4: Inibizione di SERCA → alterazione Calcio → inibizione CaMKII → inibizione STAT3 → ridotta trascrizione di CXCR4.
- Più rimozione di CXCR4 dalla superficie: Inibizione di SERCA → … → aumento fosforilazione di CXCR4 (S339) → internalizzazione del recettore.
Entrambi questi effetti contribuiscono a ridurre la presenza di CXCR4 sulla membrana cellulare, indebolendo l’ancoraggio delle CSE al midollo osseo e facilitandone la mobilizzazione nel sangue.
Per confermare il ruolo centrale di CaMKII, abbiamo usato altri due farmaci (BD e KN93) che inibiscono specificamente questo enzima. Ebbene, anche questi farmaci hanno ridotto l’espressione di CXCR4 sulle cellule e hanno promosso la mobilizzazione delle CSE nei topi, sia da soli che in combinazione con G-CSF, proprio come faceva BHQ!

Implicazioni e Prospettive Future: Nuove Armi per il Trapianto?
Questa scoperta apre scenari davvero interessanti. L’idea di usare un inibitore di SERCA come BHQ, magari in combinazione con G-CSF, potrebbe rappresentare un nuovo protocollo di mobilizzazione più rapido ed efficiente, potenzialmente in grado di aiutare anche quei pazienti che rispondono poco ai metodi attuali.
C’è anche un altro aspetto intrigante. Abbiamo visto che fornendo calcio extra alle cellule (usando calcio gluconato), potevamo contrastare l’effetto di BHQ e ripristinare l’espressione di CXCR4. Questo suggerisce che, dopo aver mobilizzato le cellule con successo, potremmo forse usare un “boost” di calcio al momento del trapianto per aiutare le CSE a “ri-ancorarsi” efficacemente nel midollo osseo del ricevente (un processo chiamato homing).
Ovviamente, siamo ancora all’inizio. Gran parte del lavoro sul meccanismo è stato fatto su linee cellulari (Jurkat) che, pur essendo utili, non sono esattamente identiche alle CSE primarie. Abbiamo però confermato alcuni passaggi chiave anche nelle cellule di topo. Serviranno ulteriori studi, soprattutto in vivo e preclinici, per validare pienamente questa strategia e valutarne la sicurezza prima di poter pensare a un’applicazione clinica.
Tuttavia, i risultati sono promettenti. Aver capito che modulare lo stress del reticolo endoplasmatico attraverso SERCA influenza la via CaMKII-STAT3-CXCR4 ci fornisce non solo una comprensione più profonda di come le CSE si muovono nel corpo, ma anche un potenziale bersaglio terapeutico per migliorare una procedura medica salvavita come il trapianto di cellule staminali. Insomma, a volte, un po’ di stress (controllato) può fare davvero bene!
Fonte: Springer