Mal di Testa Post-Puntura Lombare? Una Scintilla di Speranza dalla Stimolazione Cerebrale!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che tocca molti pazienti che devono sottoporsi a una puntura lombare (LP), magari per una diagnosi neurologica: quel fastidiosissimo mal di testa che può comparire dopo, noto come cefalea post-puntura lombare o PDPH (Post-Dural Puncture Headache).
Chi ci è passato lo sa: non è un semplice mal di testa. Spesso peggiora drasticamente quando ci si alza in piedi e migliora da sdraiati (si chiama ortostatico), e può essere accompagnato da nausea, fastidio alla luce o ai rumori, e rigidità al collo. La causa? Una piccola perdita di liquido cerebrospinale (CSF) dal punto della puntura, che riduce la pressione attorno al cervello e al midollo spinale, mettendo in tensione strutture sensibili al dolore.
Questo problema non è raro e, oltre al disagio, può significare degenze ospedaliere più lunghe e la necessità di farmaci antidolorifici. Le misure preventive classiche, come usare aghi specifici (atraumatici), sono le più efficaci, ma altre raccomandazioni come il riposo a letto o l’idratazione extra hanno un’efficacia discutibile.
E se ci fosse un modo diverso per affrontare questo problema?
Qui entro in gioco io, o meglio, la ricerca che voglio raccontarvi. Da tempo, nel campo delle neuroscienze, esploriamo tecniche di stimolazione cerebrale non invasiva (NIBS). Una di queste è la stimolazione transcranica a corrente diretta (tDCS). Sembra complicato, ma immaginate una corrente elettrica debolissima, applicata tramite elettrodi posti sullo scalpo, che può “incoraggiare” o “calmare” l’attività dei neuroni sottostanti.
In particolare, la stimolazione anodale (a-tDCS), che tende ad aumentare l’eccitabilità neuronale, si è dimostrata promettente nel trattamento di varie forme di dolore, inclusa l’emicrania. Studi clinici hanno mostrato che applicare la a-tDCS su una specifica area del cervello, la corteccia motoria primaria (M1), può ridurre frequenza e intensità degli attacchi di emicrania.
La domanda è sorta spontanea: se funziona per l’emicrania, potrebbe funzionare anche per la PDPH? Dopotutto, entrambi coinvolgono meccanismi complessi legati al dolore nel cervello.
La nostra indagine: due studi in uno
Per scoprirlo, abbiamo messo in piedi non uno, ma due studi clinici randomizzati e controllati con placebo (sham) presso l’IRCCS Neuromed. Abbiamo coinvolto 97 pazienti che dovevano sottoporsi a una puntura lombare diagnostica.
Abbiamo diviso la nostra ricerca in due protocolli:
- Studio Terapeutico (Th-tDCS): Qui abbiamo reclutato pazienti che avevano già sviluppato la PDPH dopo la puntura lombare. Li abbiamo divisi casualmente in due gruppi: uno riceveva la stimolazione a-tDCS reale per 3 giorni consecutivi, l’altro una stimolazione “finta” (sham), dove la corrente veniva interrotta dopo pochi secondi (abbastanza per sentire un leggero pizzicore iniziale, ma senza effetti reali sul cervello). Né i pazienti né noi ricercatori che valutavamo i sintomi sapevamo chi riceveva cosa (studio in doppio cieco).
- Studio Preventivo (Pr-tDCS): In questo caso, abbiamo agito d’anticipo. I pazienti venivano assegnati casualmente al gruppo a-tDCS reale o sham subito dopo la puntura lombare, prima che potesse insorgere il mal di testa. Anche qui, il trattamento durava 3 giorni consecutivi.
L’elettrodo attivo (anodo) veniva posizionato sopra la corteccia motoria M1 dell’emisfero dominante, un’area chiave nella modulazione del dolore. L’altro elettrodo (catodo) veniva messo sulla regione sopraorbitale controlaterale. La stimolazione reale durava 20 minuti a 2 mA, una corrente molto bassa e sicura.

Come abbiamo misurato il dolore?
L’obiettivo principale era vedere se la a-tDCS riduceva l’intensità della PDPH. Abbiamo usato la Scala Visuo-Analogica (VAS), una semplice linea da 0 a 100 mm dove i pazienti segnavano il livello del loro dolore in quel momento (da “nessun dolore” a “il peggior dolore immaginabile”).
Come obiettivi secondari, abbiamo usato il Brief Pain Inventory (BPI), un questionario più dettagliato che valuta non solo l’intensità del dolore nelle ultime 24 ore, ma anche quanto questo interferisce con le attività quotidiane, l’umore, il sonno, ecc. Abbiamo anche raccolto dati su ansia, depressione, qualità del sonno e qualità della vita generale all’inizio dello studio.
Cosa abbiamo scoperto? Risultati Emozionanti!
I risultati sono stati davvero incoraggianti, in entrambi gli studi!
Nello studio Terapeutico (Th-tDCS):
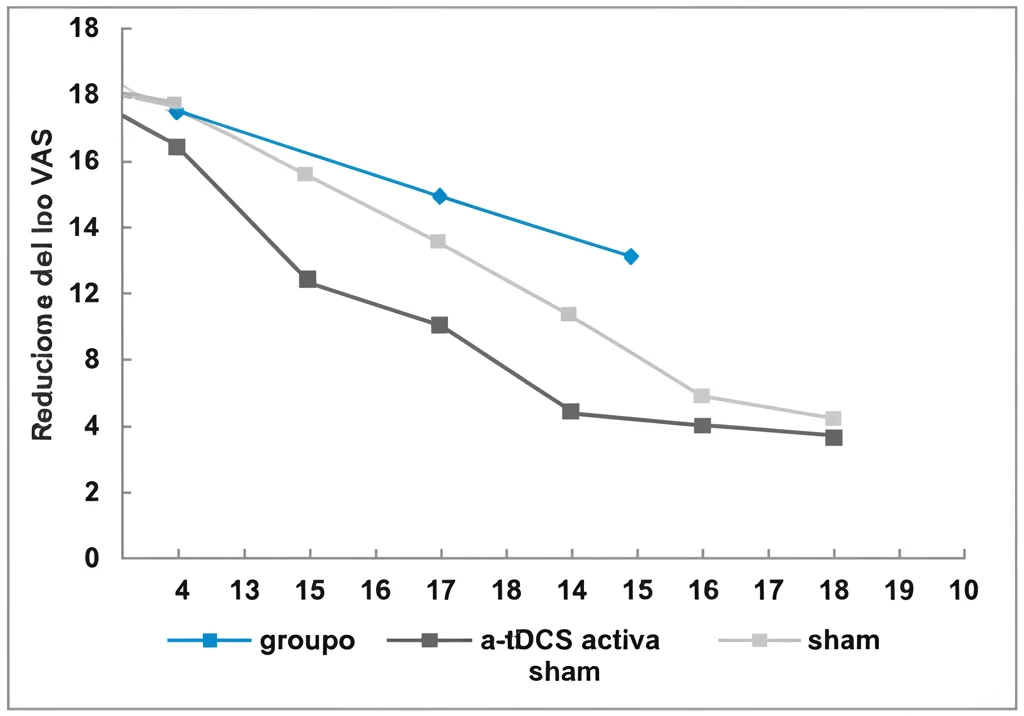
I pazienti che hanno ricevuto la stimolazione a-tDCS reale hanno mostrato una riduzione significativamente maggiore del dolore sulla scala VAS rispetto a quelli che hanno ricevuto la stimolazione sham. Già dopo il secondo giorno di trattamento (T3), la differenza era evidente e si è mantenuta fino alla fine (T5). Non solo l’intensità del dolore (VAS) è diminuita, ma anche l’impatto del dolore sulla vita quotidiana, misurato dal BPI (sia intensità che interferenza), è migliorato notevolmente nel gruppo con a-tDCS attiva.
Nello studio Preventivo (Pr-tDCS):
Qui i risultati sono stati forse ancora più interessanti. Innanzitutto, l’incidenza della PDPH è stata significativamente più bassa nel gruppo che ha ricevuto la a-tDCS preventiva: solo il 20% dei pazienti ha sviluppato il mal di testa, contro il 40% nel gruppo sham! E anche per quanto riguarda l’intensità del dolore misurata con la VAS nei giorni successivi alla LP, il gruppo a-tDCS ha riportato punteggi significativamente più bassi rispetto al gruppo sham. Lo stesso vale per il BPI: intensità e interferenza del dolore erano nettamente inferiori nel gruppo trattato preventivamente con a-tDCS.
È importante sottolineare che non ci sono stati effetti collaterali significativi in nessuno dei due gruppi e che l’uso di farmaci sintomatici (come paracetamolo o antiemetici) non era statisticamente differente tra i gruppi, suggerendo che l’effetto benefico fosse proprio dovuto alla stimolazione.
Ma come funziona questa “magia”?
Anche se i meccanismi esatti sono ancora oggetto di studio, pensiamo che stimolare la corteccia motoria M1 con a-tDCS possa influenzare positivamente la “matrice del dolore” nel cervello. Quest’area è connessa con altre regioni chiave nella percezione e modulazione del dolore, come il talamo, la corteccia cingolata, l’insula e il grigio periacqueduttale nel tronco encefalico.
La stimolazione potrebbe:
- Rinforzare i sistemi naturali del cervello che inibiscono i segnali dolorosi (il cosiddetto sistema discendente di modulazione del dolore).
- Promuovere il rilascio di oppioidi endogeni (le “morfine” naturali del nostro corpo) in aree cerebrali cruciali per il controllo del dolore.
- Modulare la connettività tra diverse aree cerebrali coinvolte nell’esperienza dolorosa, riportandola verso un funzionamento più normale.
In pratica, è come se la a-tDCS aiutasse il cervello a “riaccordare” i suoi circuiti per gestire meglio il dolore derivante dalla puntura lombare.
Un passo avanti, ma la strada è ancora lunga
Siamo molto soddisfatti di questi risultati. È la prima volta, a nostra conoscenza, che si dimostra l’efficacia della a-tDCS su M1 sia nel trattamento che nella prevenzione della PDPH. Questo apre scenari interessanti per gestire una complicanza comune e fastidiosa in modo non invasivo.
Ovviamente, come ogni studio, anche il nostro ha dei limiti. Il numero di pazienti non è enorme, provenivano da contesti clinici diversi (anche se tutti necessitavano di LP diagnostica) e non abbiamo potuto seguirli a lungo termine dopo la dimissione.
Serviranno studi più ampi per confermare questi dati e magari esplorare protocolli diversi (ad esempio, applicare la stimolazione anche prima della puntura lombare?).

In conclusione: una nuova frontiera?
Nonostante i limiti, i nostri risultati suggeriscono fortemente che la a-tDCS applicata sulla corteccia motoria M1 possa essere uno strumento efficace e sicuro per ridurre l’intensità, la durata e persino l’insorgenza della cefalea post-puntura lombare e dei sintomi dolorosi associati.
È affascinante pensare che una tecnica non invasiva come la tDCS possa avere un impatto così positivo. Potrebbe rappresentare un’opzione terapeutica e preventiva preziosa per i tanti pazienti che ogni anno affrontano una puntura lombare. La ricerca continua, ma la speranza di offrire un sollievo migliore è decisamente… elettrizzante!
Fonte: Springer