STC2: Abbiamo Trovato la Chiave Nascosta della Resistenza alla Radioterapia nel Tumore al Polmone?
Ciao a tutti! Oggi voglio portarvi con me in un viaggio affascinante nel cuore della ricerca oncologica, un campo dove ogni piccola scoperta può accendere una grande speranza. Parleremo di tumore al polmone, in particolare dell’adenocarcinoma polmonare (LUAD), che purtroppo è una delle forme più comuni e insidiose. E ci concentreremo su una sfida enorme: la radioresistenza.
Avete presente la radioterapia? È una delle armi principali che abbiamo contro il cancro, usa radiazioni ad alta energia per distruggere le cellule tumorali. Funziona, spesso molto bene, ma a volte le cellule tumorali sono più furbe, o meglio, più resistenti. Sviluppano meccanismi per sopravvivere alle radiazioni, rendendo la terapia meno efficace. Questa è la radioresistenza, una vera gatta da pelare che limita il successo delle cure e peggiora la prognosi per molti pazienti.
Il punto è che non capiamo ancora *completamente* perché alcune cellule tumorali diventano resistenti e altre no. Quali sono i fattori molecolari, i geni specifici, che orchestrano questa resistenza? È come cercare un interruttore nascosto in una stanza buia. Trovarlo potrebbe permetterci di “spegnerlo” e rendere le cellule tumorali di nuovo vulnerabili alla radioterapia.
La Nostra Caccia ai Geni della Resistenza
Ed è proprio qui che entra in gioco la nostra ricerca. Ci siamo messi alla caccia di questi “geni della radioresistenza” (li abbiamo chiamati RRRGs, per *Radioresistance-Related Genes*) nell’adenocarcinoma polmonare. Come abbiamo fatto? Beh, abbiamo usato un mix di tecniche avanzate.
Innanzitutto, abbiamo preso delle cellule di adenocarcinoma polmonare in laboratorio (la linea cellulare A549, molto usata in ricerca) e le abbiamo “allenate” a resistere alle radiazioni, sottoponendole a dosi ripetute, un po’ come avviene nella radioterapia frazionata in clinica. Poi, abbiamo usato il sequenziamento dell’RNA (RNA-seq) per vedere quali geni erano più “accesi” o “spenti” in queste cellule rese resistenti rispetto a quelle normali non irradiate. È come leggere il libretto di istruzioni delle cellule per capire cosa è cambiato.
Ma non ci siamo fermati al laboratorio. Abbiamo anche analizzato dati provenienti da pazienti reali, scaricando informazioni genetiche e cliniche da grandi database pubblici come The Cancer Genome Atlas (TCGA) e Gene Expression Omnibus (GEO). Abbiamo confrontato i profili genetici dei pazienti che avevano risposto bene alla radioterapia (Responders, Res) con quelli che non avevano risposto (Non-Responders, N-Res).
Incrociando i dati del laboratorio con quelli dei pazienti, abbiamo identificato un gruppo di geni che sembravano essere costantemente associati alla radioresistenza. Erano i nostri RRRGs! Tra questi, abbiamo usato un metodo statistico chiamato LASSO-Cox per selezionare i più “pesanti”, quelli con il maggior impatto sulla prognosi dopo la radioterapia.
Un Modello Predittivo e un Protagonista Inatteso: STC2
Siamo riusciti a costruire un modello predittivo basato su 6 di questi geni (FCGBP, SLCO4A1, ALDH3A1, STC2, TERT, CYP24A1). Questo modello, in pratica, calcola un “punteggio di rischio” per ogni paziente basato sull’espressione di questi geni. E indovinate un po’? I pazienti con un punteggio di rischio alto avevano una sopravvivenza generale (OS) significativamente più breve dopo la radioterapia, sia nel set di dati TCGA che in quello di validazione GEO. Il nostro modello sembrava funzionare bene nel predire chi avrebbe risposto meno alla terapia! L’area sotto la curva ROC (AUC), una misura di quanto è bravo un modello a distinguere tra gruppi, era promettente, specialmente per la previsione a 3 e 4 anni.
Tra questi 6 geni, uno in particolare ha attirato la nostra attenzione: STC2 (Stanniocalcina 2). Perché? Perché la sua espressione era non solo associata a una prognosi peggiore, ma mostrava anche la correlazione più forte. Sembrava essere un attore chiave in questa complessa vicenda della radioresistenza.
STC2 è una proteina che il nostro corpo produce, specialmente in condizioni di stress cellulare (come ipossia o mancanza di nutrienti). Già si sapeva che è sovraespressa in diversi tipi di cancro e che può aiutare le cellule tumorali a sopravvivere, proliferare e persino a invadere altri tessuti. Era stata collegata alla radioresistenza in altri tumori, ma il suo ruolo specifico nell’adenocarcinoma polmonare era ancora nebuloso.
STC2 Sotto la Lente: Conferme e Nuove Scoperte
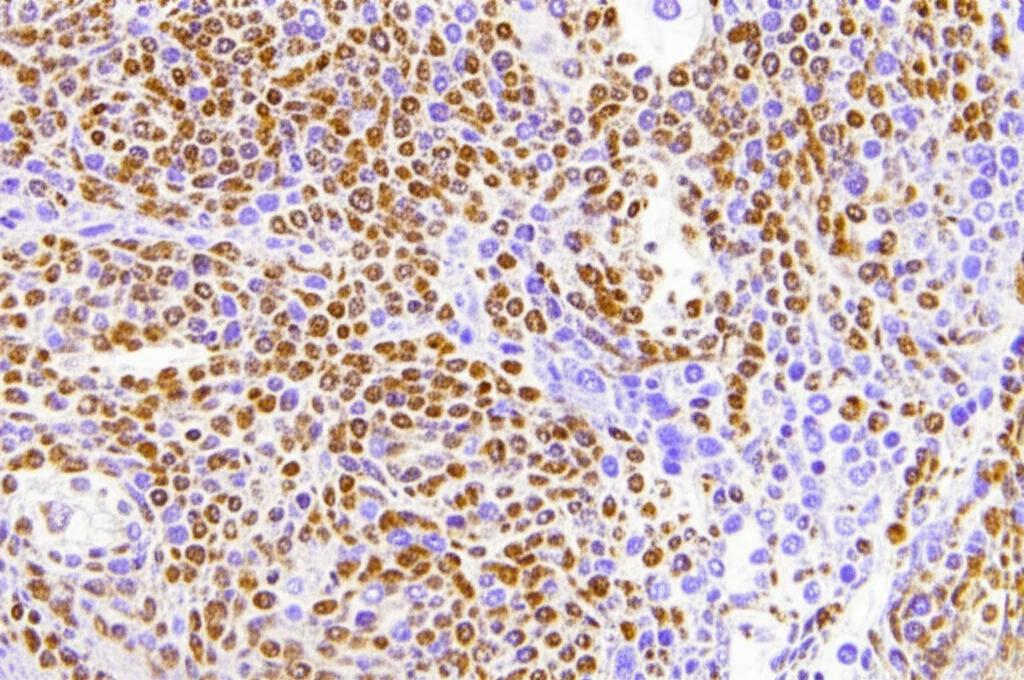
Dovevamo vederci chiaro. Siamo andati a verificare l’espressione di STC2 direttamente nei tessuti tumorali di 74 pazienti con LUAD che avevamo seguito nel nostro ospedale (First Affiliated Hospital of Xi’an Jiaotong University). Usando l’immunoistochimica (IHC), una tecnica che colora le proteine nei tessuti, abbiamo visto nero su bianco (o meglio, marrone su viola!):
- L’espressione di STC2 era significativamente più alta nei pazienti che non avevano risposto alla radioterapia (N-Res) rispetto a quelli che avevano risposto (Res).
- Era anche più alta nei tessuti tumorali rispetto ai tessuti normali adiacenti.
- E, cosa cruciale, i pazienti con alta espressione di STC2 avevano una sopravvivenza generale (OS) e una sopravvivenza libera da progressione (PFS) significativamente più brevi.
Questi dati clinici rafforzavano potentemente l’idea che STC2 fosse un marcatore di prognosi infausta e di resistenza alla radioterapia nel LUAD.
Ma non basta osservare, volevamo capire il meccanismo. Siamo tornati alle nostre cellule A549 in laboratorio. Prima di tutto, abbiamo confermato con un’altra tecnica (Western blotting) che le cellule rese radioresistenti esprimevano effettivamente più proteina STC2 rispetto alle cellule normali. Bingo!
Poi abbiamo fatto l’esperimento chiave: cosa succede se “spegniamo” il gene STC2 in queste cellule tumorali? Abbiamo usato una tecnica chiamata siRNA knockdown per silenziare specificamente STC2 nelle cellule A549. E abbiamo osservato gli effetti:
- Maggiore sensibilità alle radiazioni: Abbiamo sottoposto le cellule con STC2 silenziato (siSTC2) e le cellule di controllo (NC) a dosi crescenti di radiazioni. Risultato? Le cellule siSTC2 formavano molte meno colonie (gruppi di cellule sopravvissute) rispetto alle controllo. Silenziare STC2 le rendeva significativamente più vulnerabili alle radiazioni!
- Ridotta capacità di proliferazione: Abbiamo anche misurato quanto velocemente crescevano le cellule usando il test CCK8. Le cellule siSTC2 proliferavano molto più lentamente rispetto alle cellule di controllo, specialmente dopo le prime 24 ore.
Questi esperimenti ci hanno detto chiaramente che STC2 non è solo un marcatore passivo, ma gioca un ruolo attivo nel promuovere la radioresistenza e la proliferazione delle cellule di adenocarcinoma polmonare.
Abbiamo anche fatto un’analisi più fine usando dati di sequenziamento a singola cellula (single-cell RNA sequencing), che ci permette di vedere l’espressione genica cellula per cellula. Questo ha rivelato che STC2 è espresso in particolari tipi di cellule polmonari (come le cellule AT1 e AT2) e, cosa interessante, sembra essere particolarmente elevato nelle cellule AT2 presenti nei tessuti tumorali rispetto a quelle nei tessuti normali. Questo potrebbe suggerire un legame specifico tra STC2, questo tipo cellulare (spesso considerato cellula di origine per alcuni LUAD) e lo sviluppo del tumore e della sua resistenza.
Cosa Significa Tutto Questo per il Futuro?
Ok, tiriamo le somme. Il nostro studio ha identificato STC2 come un gene cruciale nella radioresistenza dell’adenocarcinoma polmonare. La sua alta espressione è un campanello d’allarme: predice una risposta peggiore alla radioterapia e una prognosi meno favorevole per i pazienti. Ma la notizia più eccitante è che abbiamo dimostrato, in laboratorio, che silenziare STC2 rende le cellule tumorali più sensibili alle radiazioni e ne rallenta la crescita.
Questo apre scenari davvero promettenti. STC2 potrebbe diventare:
- Un biomarcatore predittivo: Misurare i livelli di STC2 nei pazienti prima della radioterapia potrebbe aiutarci a personalizzare il trattamento, magari intensificandolo per chi ha alti livelli di STC2 o scegliendo terapie alternative.
- Un nuovo bersaglio terapeutico: Sviluppare farmaci che bloccano specificamente STC2 o la sua funzione potrebbe essere una strategia per superare la radioresistenza. Immaginate di poter somministrare un farmaco anti-STC2 insieme alla radioterapia per renderla più efficace!
Il nostro modello predittivo a 6 geni, che include STC2, si è dimostrato abbastanza accurato e potrebbe essere un ulteriore strumento per stratificare i pazienti e guidare le decisioni cliniche, anche se necessita di validazione su coorti più ampie.

Certo, la strada è ancora lunga. Dobbiamo capire più a fondo *come* esattamente STC2 conferisce radioresistenza (quali vie molecolari attiva o disattiva? Interagisce con la riparazione del DNA? Con il ciclo cellulare? Con lo stress ossidativo?). E poi, ovviamente, bisognerà sviluppare e testare potenziali farmaci anti-STC2 in modelli preclinici e, speriamo, in studi clinici.
Ma aver identificato un attore così importante come STC2 in un problema così critico come la radioresistenza nel tumore al polmone è un passo avanti significativo. È una nuova luce che si accende nella stanza buia, una nuova speranza per migliorare le cure e la vita dei pazienti che affrontano questa difficile malattia. E noi siamo entusiasti di continuare a esplorare questa pista!
Fonte: Springer