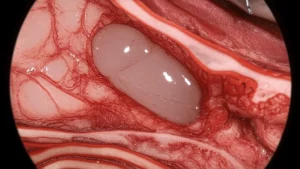
Cancro Ovarico: Perché Rimuovere Tutto il Tumore Fa Davvero la Differenza (Studio Norvegese)
Ciao a tutti! Oggi voglio parlarvi di un argomento tosto ma fondamentale: il cancro ovarico e cosa succede dopo l’intervento chirurgico. Sapete, quando si affronta questa malattia, uno degli obiettivi principali della chirurgia, chiamata citoriduttiva, è rimuovere quanto più tumore possibile. Ma cosa succede se rimane qualche traccia? Quanto impatta sulla sopravvivenza? Bene, ho sottomano uno studio norvegese molto interessante, pubblicato su Springer, che ha cercato di rispondere proprio a queste domande, analizzando i dati di un intero paese. E i risultati, ve lo dico subito, sono piuttosto netti.
Lo Studio Norvegese: Numeri che Parlano Chiaro
Immaginate un po’: i ricercatori hanno preso in esame i dati di ben 2608 donne a cui è stato diagnosticato un cancro epiteliale ovarico (EOC) invasivo in stadio III-IV tra il 2013 e il 2022, grazie al Registro Tumori Norvegese. Di queste, 1849 sono state operate. L’obiettivo era capire come la presenza di malattia residua (RD) – cioè tessuto tumorale rimasto dopo l’intervento – influenzasse la sopravvivenza rispetto a chi non aveva più malattia macroscopicamente visibile (NMRD, No Macroscopic Residual Disease).
Hanno usato modelli statistici sofisticati (i flexible parametric models, per i più tecnici) per confrontare la mortalità “in eccesso” (quella dovuta specificamente al tumore, al netto di altre cause) tra i due gruppi. E indovinate un po’?
Il Verdetto: Nessuna Malattia Residua è Sempre Meglio
I risultati sono stati cristallini: le donne con malattia residua (RD) avevano un rischio di mortalità 2,62 volte maggiore rispetto a quelle con NMRD. Un dato potente, non trovate? E la cosa interessante è che questa differenza significativa è stata osservata indipendentemente dal tipo istologico del tumore (cioè dal tipo specifico di cellule tumorali, come sieroso ad alto grado, endometrioide, mucinoso, etc.). Il test per l’eterogeneità tra i tipi istologici non ha mostrato differenze statisticamente significative (p=0.21), suggerendo che l’obiettivo di non lasciare malattia residua è cruciale per tutti i sottotipi principali.
Ma Quanto Conta la Dimensione del Tumore Residuo?
Qui arriva un altro punto affascinante. I ricercatori si sono chiesti: ok, avere malattia residua è peggio, ma fa differenza se ne rimane pochissima (pochi millimetri) o di più (diversi centimetri)? Hanno diviso le pazienti con RD in categorie basate sul diametro del tumore residuo.
Ebbene, anche le donne con una quantità minima di malattia residua, tra 0.1 e 0.4 cm, avevano già un rischio di morte quasi raddoppiato (EHR = 2.09) rispetto a chi aveva NMRD. Per le categorie con diametri maggiori (da 0.5-0.9 cm fino a 3.0-20 cm), il rischio era circa triplicato (EHR intorno a 2.75-2.97) rispetto all’assenza di malattia residua.
La vera sorpresa, però, è emersa analizzando la sopravvivenza *all’interno* del gruppo di pazienti con malattia residua (RD > 0 cm). Modellando il diametro come una variabile continua (usando tecniche come le restricted cubic splines), non è emersa una differenza statisticamente significativa nella sopravvivenza a tre anni al variare del diametro del tumore residuo (p ≥ 0.17). Questo vale sia considerando tutti i tumori insieme, sia focalizzandosi sul tipo più comune, il sieroso ad alto grado. Sembra quasi dire: una volta che c’è malattia residua, anche poca, la prognosi peggiora significativamente, e la quantità esatta (sopra lo zero) potrebbe non essere il fattore più determinante per la sopravvivenza successiva, almeno per i tipi più comuni. C’era un leggero segnale (p=0.04) che per i tipi istologici *non* sierosi ad alto grado, dimensioni minori di RD (≤0.4 cm) potessero associarsi a una sopravvivenza leggermente migliore rispetto a RD di 1 cm, ma sono dati da prendere con cautela vista la numerosità campionaria ridotta per questi sottotipi.
Chemioterapia Prima o Dopo la Chirurgia? L’Importanza di NMRD Rimane
Un’altra analisi interessante ha riguardato l’uso della chemioterapia. Alcune pazienti ricevono la chirurgia come primo trattamento (Primary Cytoreductive Surgery, PCS), seguita da chemio adiuvante. Altre, invece, fanno prima alcuni cicli di chemioterapia (Neoadjuvant Chemotherapy, NACT) per ridurre il tumore, e poi vengono operate (Interval Cytoreductive Surgery, ICS).
Lo studio ha analizzato un sottogruppo di pazienti diagnosticate dal 2019 in poi, per cui erano disponibili dati dettagliati sulle terapie sistemiche (chemioterapia, bevacizumab, PARP inibitori – PARPi). Cosa hanno scoperto? Che l’obiettivo di raggiungere NMRD è associato a una migliore sopravvivenza indipendentemente dal fatto che si faccia PCS o NACT+ICS. Certo, le pazienti che ottengono NMRD dopo PCS sembrano avere una prognosi leggermente migliore rispetto a quelle che ottengono NMRD dopo NACT+ICS, ma in entrambi i casi, non avere malattia residua è la condizione migliore.

Un dato particolare è emerso nel gruppo PCS (senza NACT): le pazienti con malattia residua piccola (0.1-0.9 cm) avevano un rischio di morte sorprendentemente alto (EHR = 8.72), addirittura superiore a quelle con RD più grande (1.1-20 cm, EHR = 3.64). Questo pattern non si vedeva nel gruppo NACT+ICS. Gli autori ipotizzano che questo possa legarsi alle indicazioni per terapie aggiuntive come il bevacizumab, che in Norvegia erano previste per pazienti considerate “ad alto rischio” (stadio IV, RD > 1 cm dopo PCS, o NACT). Le pazienti con PCS e RD < 1 cm potrebbero essere state considerate a "basso rischio", non ricevendo bevacizumab, ma mostrando comunque una prognosi sfavorevole. Questo solleva interrogativi sulla definizione stessa di "basso rischio" nel cancro ovarico avanzato.
L’Impatto delle Terapie Mirate
L’analisi ha anche confermato che l’uso dei PARP inibitori (PARPi), terapie mirate per pazienti con specifiche caratteristiche molecolari (es. mutazioni BRCA o deficit della ricombinazione omologa), è associato a una migliore sopravvivenza, soprattutto nei tumori sierosi ad alto grado. Questo sottolinea l’importanza crescente della personalizzazione delle cure.
Cosa Portiamo a Casa?
Questo studio norvegese, basato su dati “real-world” di un’intera nazione, rafforza un messaggio chiave: nella chirurgia del cancro ovarico avanzato, l’obiettivo primario deve essere la rimozione completa di tutta la malattia macroscopicamente visibile (NMRD). Questo offre le migliori possibilità di sopravvivenza, indipendentemente dal tipo istologico e dal timing della chirurgia rispetto alla chemio.
La scoperta che, una volta presente, la quantità esatta di malattia residua potrebbe non influenzare drasticamente la sopravvivenza (specialmente per i tumori sierosi ad alto grado) è intrigante e merita ulteriori studi. Potrebbe significare che anche quantità minime di tumore residuo hanno un impatto biologico significativo o che la capacità di raggiungere NMRD riflette una biologia tumorale intrinsecamente meno aggressiva o più chemio-sensibile.
Infine, i dati sull’interazione tra RD e NACT, e l’osservazione sulla prognosi inaspettatamente sfavorevole per pazienti PCS con piccola RD, suggeriscono che forse dobbiamo riconsiderare come definiamo i gruppi di rischio e chi potrebbe beneficiare di terapie adiuvanti più aggressive come il bevacizumab.
Insomma, la battaglia contro il cancro ovarico è complessa, ma studi come questo ci aiutano a capire meglio quali fattori contano davvero e dove concentrare gli sforzi per migliorare le cure e la sopravvivenza delle pazienti. La chirurgia ottimale rimane un pilastro fondamentale.
Fonte: Springer