Rinite Allergica e Morte Cellulare ‘Infuocata’: Ho Scoperto il Legame Nascosto con GZMA!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che affligge milioni di persone nel mondo, me compreso a volte: la rinite allergica (AR). Quel fastidioso naso che cola, gli starnuti a raffica, il prurito… un vero incubo, vero? Colpisce circa 400 milioni di persone a livello globale e i numeri sono in continua crescita. Pensate che solo negli Stati Uniti ne soffre il 15% della popolazione, con costi annuali che superano i 20 miliardi di dollari! Ma la cosa frustrante è che, nonostante sia così comune, i meccanismi precisi che la scatenano sono ancora un po’ un mistero.
Un Nuovo Indiziato: La Piroptosi
Recentemente, però, la ricerca ha iniziato a puntare i riflettori su un processo cellulare affascinante e un po’ inquietante: la piroptosi. Non è la solita morte cellulare programmata (apoptosi) né una morte accidentale (necrosi). Immaginate una cellula che decide di “autodistruggersi” ma facendolo in modo… esplosivo! La piroptosi è una forma di morte cellulare programmata che scatena una forte risposta infiammatoria. La cellula si gonfia, la sua membrana si rompe formando piccoli pori e rilascia all’esterno citochine pro-infiammatorie come IL-1β e IL-18, richiamando altre cellule immunitarie sul posto. È come se la cellula suonasse un allarme antincendio potentissimo prima di soccombere.
Studi recenti hanno suggerito che questa “morte infuocata” potrebbe giocare un ruolo chiave proprio nella rinite allergica. In modelli animali di AR, si è osservata un’aumentata piroptosi nelle cellule della mucosa nasale. Ma quale fosse il legame molecolare preciso, quali geni fossero coinvolti in entrambi i processi… beh, questo non era ancora chiaro. Ed è qui che entra in gioco la mia ricerca (o meglio, l’analisi che ho condotto su dati esistenti!).
La Caccia ai Geni: Detective nel Mondo della Bioinformatica
Come svelare questo mistero? Ho deciso di usare la potenza della bioinformatica. Immaginate di avere accesso a enormi archivi di dati genetici (come il database GEO – Gene Expression Omnibus) provenienti da persone con rinite allergica e persone sane. Il mio obiettivo era trovare i geni che fossero contemporaneamente legati alla rinite allergica E alla piroptosi.
Per farlo, ho “setacciato” diversi set di dati (GSE51392, GSE43523, GSE44037) usando tecniche computazionali avanzate come:
- WGCNA (Weighted Gene Co-expression Network Analysis): Per identificare gruppi di geni che lavorano insieme.
- LASSO (Least Absolute Shrinkage and Selection Operator): Un metodo statistico per selezionare i geni più importanti.
- Random Forest (RF): Un algoritmo di machine learning per identificare i geni “predittivi”.
Ho incrociato i geni identificati come rilevanti per la AR da queste analisi con un elenco di geni noti per essere coinvolti nella piroptosi (ottenuti dal database GeneCards). L’obiettivo era trovare i “geni comuni”, quelli all’intersezione tra AR e piroptosi.

Il Protagonista Inatteso: GZMA
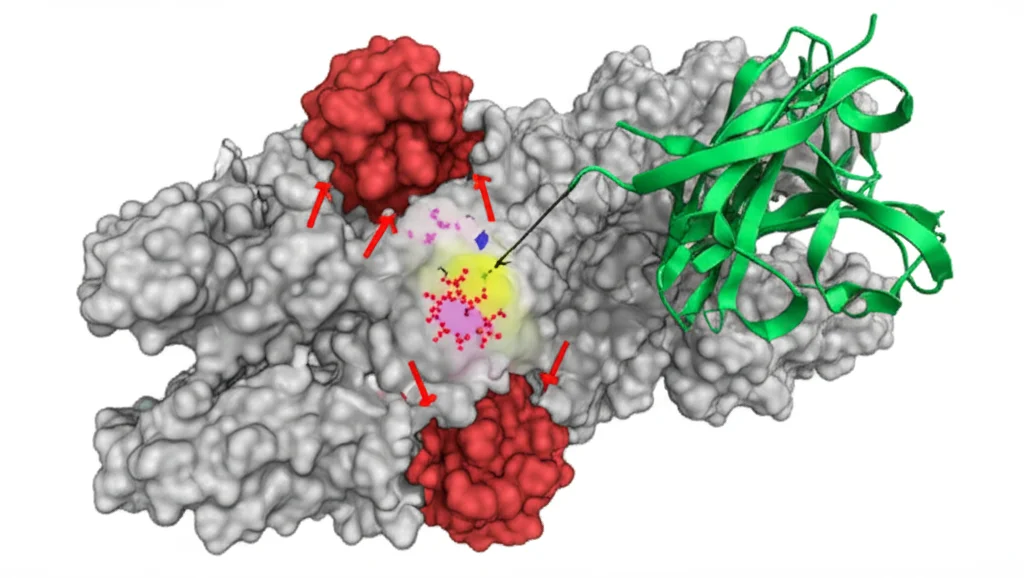
E sapete cosa è emerso da questa complessa analisi incrociata? Un gene in particolare si è distinto: GZMA (Granzyme A). Questo gene codifica per un enzima, una proteasi serinica, secreta principalmente da cellule immunitarie citotossiche come le cellule Natural Killer (NK) e i linfociti T citotossici (CTLs CD8+). Sembrava proprio essere il pezzo mancante del puzzle!
Per essere sicuri, ho verificato questo risultato su un altro set di dati indipendente (GSE101720) e l’analisi della curva ROC (uno strumento statistico per valutare la capacità diagnostica) ha confermato che GZMA ha un buon potenziale predittivo per la rinite allergica. L’AUC (Area Under the Curve) era promettente sia nel set di dati di training (0.779) che in quello di validazione (0.667).
Dalla Teoria alla Pratica: La Conferma nel Modello Animale
Ma i dati digitali non bastano. Serviva una prova “sul campo”. Per questo, abbiamo utilizzato un modello murino (topi) di rinite allergica indotta da ovalbumina (OVA). Abbiamo prelevato campioni di tessuto della mucosa nasale dai topi con AR e dai topi di controllo sani. Ebbene, l’analisi tramite Western Blot (una tecnica per misurare la quantità di specifiche proteine) ha confermato i nostri sospetti: i livelli della proteina GZMA erano significativamente più alti nei topi con rinite allergica rispetto ai controlli! Non solo, anche i livelli di NLRP3 e GSDMD (altre proteine chiave nella via della piroptosi, in particolare l’inflammasoma NLRP3 e la gasdermina D che esegue la rottura della membrana) erano aumentati. Questo suggerisce che la via NLRP3/GSDMD/GZMA è effettivamente attiva e contribuisce alla patogenesi della AR.
Il Contesto Immunitario: Cosa Succede alle Cellule di Difesa?
Ma GZMA non agisce nel vuoto. Fa parte di un complesso scenario immunitario. Analizzando l’infiltrazione di cellule immunitarie nei campioni (usando un algoritmo chiamato CIBERSORT), abbiamo notato delle differenze interessanti tra i pazienti con AR e i controlli sani:
- Una riduzione significativa dei Linfociti T regolatori (Tregs) nei pazienti con AR. I Tregs sono fondamentali per “spegnere” le risposte immunitarie eccessive e mantenere la tolleranza. La loro diminuzione potrebbe favorire l’infiammazione allergica.
- Un aumento delle cellule NK attivate e una diminuzione di quelle a riposo.
- Una correlazione positiva tra l’espressione di GZMA e i livelli di Linfociti T CD8+. Questo è logico, dato che le cellule CD8+ sono una delle principali fonti di GZMA.
Quindi, l’ipotesi che emerge è che nella rinite allergica ci sia uno squilibrio immunitario: meno “pompieri” (Tregs) e forse più “soldati” (CD8+ T cells, NK attivate) che secernono GZMA. E GZMA, a sua volta, potrebbe promuovere la piroptosi, magari tagliando proteine come la Gasdermina B (GSDMB), come suggerito da studi recenti sul cancro e l’asma, creando un circolo vizioso infiammatorio.

GZMA: Un Nuovo Bersaglio Terapeutico?
Tutto questo ci porta a una conclusione entusiasmante: GZMA potrebbe essere un nuovo bersaglio molecolare per prevenire e trattare la rinite allergica. Se GZMA gioca un ruolo così centrale nel promuovere l’infiammazione e la piroptosi innescate dalla risposta allergica, allora bloccare la sua azione potrebbe essere una strategia terapeutica efficace.
Interessante notare che, analizzando la sensibilità ai farmaci nel database CellMiner, abbiamo trovato una correlazione tra l’espressione di GZMA e la sensibilità al metilprednisolone, un corticosteroide comunemente usato per trattare l’infiammazione, suggerendo un possibile legame funzionale.
Cosa Ci Riserva il Futuro?
Certo, siamo ancora all’inizio. Questa è un’analisi bioinformatica integrata con una validazione preliminare in vivo. Serviranno ulteriori studi sperimentali per confermare questi meccanismi nel dettaglio e per capire come GZMA interagisca esattamente con la via della piroptosi nella rinite allergica (ad esempio, il suo ruolo su GSDMB). Bisognerà anche validare questi risultati su campioni umani più ampi.
Tuttavia, aver identificato GZMA come un gene chiave all’incrocio tra rinite allergica, piroptosi e risposta immunitaria (in particolare cellule CD8+ e Tregs) apre strade davvero promettenti. Potrebbe portare allo sviluppo di terapie più mirate e personalizzate per chi, come tanti di noi, combatte ogni giorno contro starnuti e naso che cola. La battaglia contro la rinite allergica ha forse trovato un nuovo, importante, punto debole da colpire!
Fonte: Springer