Ansia: Svelato il Ruolo Nascosto dell’Ormone della Fame nel Cervello!
Ciao a tutti, appassionati di scienza e misteri del cervello! Oggi voglio portarvi con me in un viaggio affascinante nel cuore delle nostre emozioni, in particolare dell’ansia. Sappiamo tutti cos’è, quella sensazione sgradevole di preoccupazione o paura che a volte ci attanaglia. Ma vi siete mai chiesti cosa succede *davvero* nel nostro cervello quando siamo ansiosi, specialmente dopo periodi di forte stress? Beh, tenetevi forte, perché una recente ricerca ha gettato nuova luce su meccanismi sorprendenti, coinvolgendo un attore inaspettato: un recettore legato all’ormone della fame!
Capire l’Ansia: Un Puzzle Complesso
L’ansia, di per sé, non è una nemica. È una risposta fisiologica adattativa, un campanello d’allarme che ci aiuta a reagire a stimoli stressanti e a sopravvivere. Il problema sorge quando questa risposta diventa eccessiva, sproporzionata o cronica, trasformandosi in un vero e proprio disturbo che limita la nostra vita quotidiana. Lo stress cronico, come quello che molti hanno sperimentato durante e dopo la pandemia di COVID-19 (che ha fatto impennare i casi di disturbi d’ansia del 25.6%!), è uno dei principali fattori di rischio. Ma quali sono i circuiti neurali, le “strade” nel nostro cervello, che vanno in tilt? E quali molecole sono coinvolte? La verità è che ne sappiamo ancora troppo poco.
L’Ipotalamo Ventromediale: Un Crocevia di Emozioni e Metabolismo
Entra in scena una piccola ma potentissima area del cervello: il nucleo ventromediale dell’ipotalamo (VMH). Questa regione, conservata nel corso dell’evoluzione, è un vero centro di controllo per funzioni vitali come l’alimentazione, il metabolismo energetico e persino comportamenti innati come quelli sociali e difensivi. Recenti studi hanno iniziato a collegare specifiche parti del VMH, in particolare le zone dorsomediale e centrale (VMHdm/c), alle risposte allo stress e ai comportamenti di difesa. In particolare, si è visto che attivare certi neuroni in quest’area, quelli che esprimono una proteina chiamata αCaMKII+ (un nome un po’ tecnico, ma pensatela come un marcatore per un tipo specifico di neuroni eccitatori), può indurre comportamenti simili all’ansia. Ma come funzionano esattamente questi neuroni?
Neuroni Sotto Stress: Cosa Succede nel VMH?
I ricercatori hanno usato tecniche pazzesche, come la fotometria a fibra ottica, per “spiare” l’attività di questi neuroni αCaMKII+ nel VMH di topolini mentre esploravano un labirinto chiamato “Elevated Plus Maze” (EPM), un test classico per misurare l’ansia. Immaginate un labirinto a forma di più (+), sospeso in aria, con due bracci aperti (spaventosi per un topo!) e due chiusi (più sicuri). Ebbene, hanno scoperto che in condizioni normali, l’attività di questi neuroni aumentava quando i topi entravano nei bracci aperti (quelli che inducono ansia) e diminuiva nei bracci chiusi. Sembra quasi che questi neuroni “sentano” lo stress ambientale.
Ma la cosa ancora più sorprendente è venuta dopo. Usando tecniche come la chemogenetica (attivare o disattivare neuroni con farmaci specifici) e l’optogenetica (usare la luce per controllare i neuroni!), hanno scoperto che attivare artificialmente questi neuroni αCaMKII+ nel VMH… riduceva i comportamenti ansiosi! Sì, avete letto bene. Sembra controintuitivo: neuroni che si attivano in situazioni ansiogene, se stimolati ulteriormente, alleviano l’ansia. Questo suggerisce che forse l’attivazione di questi neuroni è in realtà un meccanismo di coping, un modo per affrontare lo stress e mantenere l’ansia a livelli gestibili. Inattivarli, al contrario, aumentava l’ansia. Quindi, l’attività di questi neuroni sembra essere necessaria e sufficiente per sopprimere l’ansia in condizioni normali.
Lo Stress Ripetuto Cambia le Carte in Tavola
Ok, ma cosa succede quando lo stress non è un evento isolato, ma diventa cronico? I ricercatori hanno sottoposto i topi a uno stress da immobilizzazione ripetuto (Repeated Restraint Stress, RRS) per 4 giorni. Hanno poi osservato il comportamento dei topi in diversi momenti dopo lo stress. Curiosamente, l’aumento significativo dell’ansia non era immediato, ma si manifestava in modo ritardato, circa 6 giorni dopo la fine dello stress. I topi diventavano più ansiosi nell’EPM, meno socievoli e mostravano più segni di “disperazione” in altri test come il test di sospensione per la coda (TS) e il test di nuoto forzato (FS).
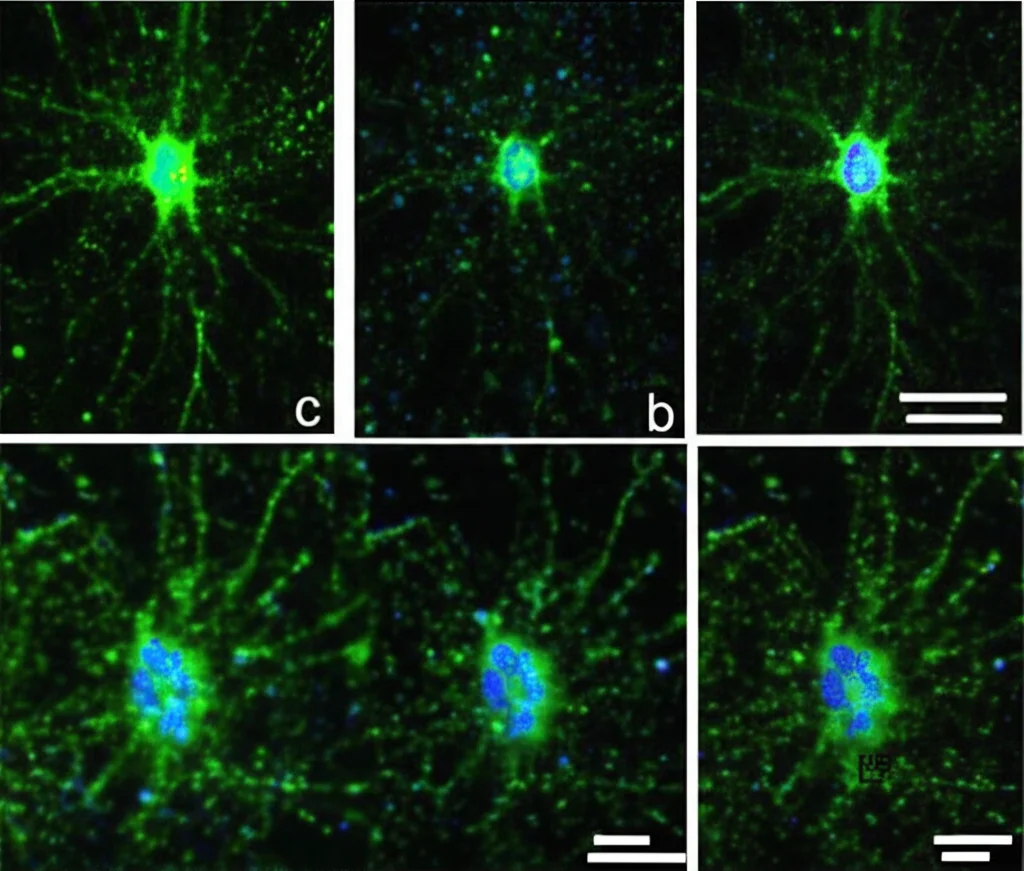
A questo punto, ci si aspetterebbe forse che i famosi neuroni αCaMKII+ nel VMH fossero meno attivi, dato che la loro attivazione riduce l’ansia. Invece, misurando un marcatore di attività neuronale (la proteina c-Fos), hanno visto che questi neuroni erano persistentemente attivati sia subito dopo lo stress (90 minuti) sia 6 giorni dopo, quando l’ansia era ormai manifesta. Tuttavia, andando a misurare l’attività elettrica *direttamente* da questi neuroni attivati dallo stress (usando una tecnica sofisticata chiamata RAM system combinata con l’elettrofisiologia), hanno scoperto che la loro frequenza di scarica (quanto spesso “sparano” segnali) era significativamente ridotta a 6 giorni rispetto a 90 minuti dopo lo stress. Anche le registrazioni in vivo (fotometria) nei topi stressati mostravano una risposta attenuata nei bracci aperti del labirinto rispetto ai topi non stressati.
Quindi, riassumendo: lo stress cronico porta a un’ansia ritardata, e anche se i neuroni αCaMKII+ sembrano “accendersi” in risposta allo stress (c-Fos), la loro capacità effettiva di comunicare (frequenza di scarica) diminuisce proprio quando l’ansia aumenta. C’è qualcosa che sta frenando questi neuroni “anti-ansia”?
Il Colpevole Inatteso: GHS-R1a, il Recettore della Grelina
Ed è qui che entra in gioco il nostro protagonista molecolare: il recettore GHS-R1a. Questo è il recettore a cui si lega la grelina, un ormone prodotto principalmente dallo stomaco, noto come “l’ormone della fame”. Ma la grelina e il suo recettore non si occupano solo di appetito; sono coinvolti anche nella risposta allo stress e nella regolazione delle emozioni, anche se i meccanismi sono sempre stati poco chiari.
I ricercatori hanno misurato l’espressione del gene GHS-R1a nel VMH dei topi stressati. E cosa hanno trovato? Un aumento significativo dell’espressione di GHS-R1a proprio a 6 giorni dopo lo stress, in perfetta coincidenza con l’aumento dell’ansia e la diminuzione dell’eccitabilità dei neuroni αCaMKII+! Questo aumento avveniva specificamente nei neuroni αCaMKII+ del VMHdm/c. Non si osservava un aumento simile subito dopo lo stress (90 minuti), né in altre aree cerebrali coinvolte nell’ansia come il nucleo accumbens (NAc) nello stesso modo. Anche nell’ippocampo ventrale (vHPC) c’era un aumento a 6 giorni, ma vedremo che non sembrava avere lo stesso effetto comportamentale.

La Prova del Nove: Manipolare GHS-R1a
Avere una correlazione è interessante, ma per dimostrare una causa ed effetto bisogna intervenire! E i ricercatori l’hanno fatto, in modo brillante.
- Hanno ridotto l’espressione di GHS-R1a specificamente nei neuroni αCaMKII+ del VMH (usando tecniche come l’RNA interference o topi geneticamente modificati). Risultato? I topi mostravano meno ansia, sia in condizioni normali sia dopo lo stress RRS!
- Hanno aumentato l’espressione di GHS-R1a in questi stessi neuroni. Risultato? I topi mostravano più ansia, sia in condizioni normali sia dopo lo stress!
Questi esperimenti dimostrano in modo causale che l’aumento di GHS-R1a nei neuroni αCaMKII+ del VMH è direttamente responsabile dell’aumento dell’ansia indotta dallo stress. Hanno anche verificato che aumentare GHS-R1a in altri tipi di neuroni (inibitori) nel VMH o nei neuroni αCaMKII+ dell’ippocampo ventrale non aveva lo stesso effetto ansiogeno, sottolineando la specificità del meccanismo nel VMHdm/c.
Come Agisce GHS-R1a? Frenando i Neuroni Anti-Ansia
Ma come fa GHS-R1a a promuovere l’ansia? Ricordate che l’aumento di GHS-R1a coincideva con una ridotta frequenza di scarica dei neuroni αCaMKII+? Ebbene, hanno confermato che aumentare artificialmente GHS-R1a in questi neuroni ne riduceva l’eccitabilità spontanea (li faceva “sparare” meno). Inoltre, usando un farmaco antagonista di GHS-R1a (YIL781), somministrato localmente nel VMH, riuscivano a bloccare l’effetto ansiogeno causato dall’eccesso di GHS-R1a.
Infine, hanno fatto un esperimento combinato: hanno aumentato GHS-R1a nei neuroni αCaMKII+ (cosa che li rende più ansiosi e meno eccitabili) e *contemporaneamente* li hanno attivati con la chemogenetica (usando hM3Dq). Risultato? L’attivazione forzata riusciva a “bypassare” l’effetto inibitorio di GHS-R1a e a ridurre l’ansia, sia nei topi normali che in quelli stressati. Questo conferma che GHS-R1a promuove l’ansia proprio perché “frena” l’attività di questi neuroni αCaMKII+ che, quando attivi, ci aiutano a gestire lo stress.
Implicazioni e Prospettive Future
Questa ricerca è davvero affascinante perché svela un meccanismo molecolare e cellulare specifico attraverso cui lo stress cronico può portare a un aumento patologico dell’ansia. Identifica il recettore GHS-R1a nei neuroni αCaMKII+ del VMHdm/c come un interruttore cruciale. Inizialmente, questi neuroni si attivano per aiutarci ad affrontare lo stress, ma l’esposizione prolungata porta a un aumento ritardato di GHS-R1a, che ne sopprime l’attività e fa pendere la bilancia verso uno stato di ansia eccessiva.

La scoperta che GHS-R1a gioca questo ruolo apre nuove, intriganti possibilità terapeutiche. Potremmo immaginare farmaci che bloccano selettivamente GHS-R1a nel VMH (come l’antagonista YIL781 usato nello studio) per trattare disturbi d’ansia indotti da stress, come il disturbo da stress post-traumatico (PTSD)? Certo, la strada è ancora lunga. Bisogna capire meglio come lo stress regola l’espressione di GHS-R1a, se la grelina circolante è direttamente coinvolta in questo processo nel VMH, e quali sono i circuiti a valle di questi neuroni. Ma è un passo avanti importantissimo nella comprensione di un’emozione così complessa e diffusa come l’ansia. Il nostro cervello non smette mai di sorprenderci!
Fonte: Springer