Puntini di Carbonio dal Paclitaxel: Una Nuova Speranza Contro il Tumore al Cervello?
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona profondamente: la lotta contro uno dei tumori cerebrali più aggressivi e temuti, il glioblastoma. Sapete, il glioblastoma è davvero un osso duro, rappresenta la forma più comune e letale di cancro al cervello, con una prognosi spesso infausta nonostante le terapie attuali come chirurgia, radioterapia e chemioterapia. Uno dei problemi principali? La famigerata barriera emato-encefalica (BBB), una sorta di “muro difensivo” che protegge il nostro cervello ma, ahimè, impedisce alla maggior parte dei farmaci di raggiungere efficacemente il tumore.
La Sfida del Glioblastoma e la Barriera Emato-Encefalica
Pensate che la sopravvivenza media dopo la diagnosi è di soli 14 mesi, anche con le cure standard. E anche quando si aggiungono terapie più recenti, il guadagno è limitato. La recidiva è quasi una certezza, colpendo il 90% dei pazienti. È chiaro che c’è un bisogno disperato di nuove strategie terapeutiche, di farmaci che possano superare quella dannata barriera e colpire il tumore dove fa più male.
Ed è qui che entra in gioco la nanomedicina, un campo incredibilmente promettente. Le nanoparticelle, grazie alle loro dimensioni infinitesimali e alle loro proprietà uniche, offrono nuove speranze. Tra queste, i punti di carbonio (Carbon Dots o CDs) stanno emergendo come candidati particolarmente interessanti. Sono biocompatibili, stabili, economici da produrre e, cosa fondamentale, alcuni studi suggeriscono che possano attraversare la BBB.
La Nostra Idea: Sfruttare un “Vecchio” Farmaco in Modo Nuovo
Allora ci siamo chiesti: e se potessimo prendere un farmaco chemioterapico conosciuto ed efficace contro molti tumori, ma limitato nel trattamento del glioblastoma proprio a causa della BBB e della sua scarsa solubilità in acqua, e trasformarlo in qualcosa di nuovo grazie ai punti di carbonio? Il farmaco in questione è il Paclitaxel (PTX). È potentissimo contro le cellule tumorali (pensate, potenzialmente 1400 volte più potente del temozolomide, il farmaco standard per il glioblastoma, almeno in laboratorio!), ma da solo non ce la fa a raggiungere il cervello in quantità sufficienti.
Così, abbiamo sviluppato un metodo innovativo: usando il Paclitaxel stesso come precursore, attraverso un processo chiamato “metodo idrotermale one-step” (sembra complicato, ma è relativamente semplice!), abbiamo creato dei nuovissimi punti di carbonio, che abbiamo chiamato PTX-CDs.
PTX-CDs: Piccoli, Solubili e Capaci di Superare la Barriera
La prima cosa sorprendente è stata la solubilità: i nostri PTX-CDs sono risultati circa 1000 volte più solubili in acqua rispetto al PTX originale! Un vantaggio enorme. Analizzandoli al microscopio elettronico (TEM), abbiamo visto che sono particelle piccolissime, con un diametro medio di circa 20 nanometri, e ben disperse. Hanno anche mostrato proprietà fluorescenti, emettendo una luce blu-verde sotto raggi UV, il che è utile per seguirne il percorso nelle cellule.
Ma la domanda cruciale era: riescono a superare la BBB? Abbiamo costruito un modello di barriera emato-encefalica in vitro e… sì! I PTX-CDs hanno mostrato una capacità di attraversamento significativa, circa il 19.8%. Sembra che lo facciano principalmente attraverso un meccanismo chiamato macropinocitosi, una sorta di “ingestione” da parte delle cellule della barriera. Questo è un passo avanti gigantesco!

Come Colpiscono le Cellule Tumorali? Il Meccanismo d’Azione
Una volta superata la barriera, come agiscono questi PTX-CDs sulle cellule di glioblastoma? Abbiamo osservato che vengono rapidamente assorbiti dalle cellule tumorali (in meno di 30 minuti!) e, cosa molto interessante, si accumulano preferenzialmente nei mitocondri. I mitocondri sono le “centrali energetiche” della cellula, ma sono anche un punto debole.
I PTX-CDs, una volta nei mitocondri, sembrano danneggiarli. Abbiamo visto alterazioni nella loro struttura e una perdita del potenziale di membrana mitocondriale. Questo danno porta a un aumento massiccio di specie reattive dell’ossigeno (ROS), molecole che causano forte stress ossidativo all’interno della cellula. È come sovraccaricare la cellula di “rifiuti tossici” che non riesce a smaltire. E questo stress ossidativo è la causa principale della morte cellulare (apoptosi) indotta dai nostri PTX-CDs. Abbiamo confermato questo meccanismo vedendo che, se trattavamo le cellule anche con antiossidanti, la tossicità dei PTX-CDs diminuiva.
Non Solo Morte Cellulare: Stop alla Proliferazione e all’Invasione
Ma non è tutto. Volevamo capire più a fondo cosa succedesse a livello genetico. Analizzando l’espressione genica (RNA-sequencing) delle cellule trattate, abbiamo scoperto che i PTX-CDs mandano letteralmente in tilt il ciclo cellulare. In particolare, bloccano le cellule nella fase G2/M, impedendo loro di dividersi e quindi di proliferare. Abbiamo confermato questo blocco vedendo una diminuzione delle proteine chiave che regolano questa fase (come CDC25C, Ciclina B1 e CDK1). E infatti, i test di proliferazione e formazione di colonie hanno mostrato una drastica riduzione della crescita delle cellule tumorali trattate con PTX-CDs.
Un’altra caratteristica terribile del glioblastoma è la sua capacità di invadere il tessuto cerebrale circostante. Questo processo è spesso legato alla cosiddetta transizione epitelio-mesenchimale (EMT), un meccanismo che rende le cellule più mobili e invasive. Ebbene, abbiamo scoperto che i PTX-CDs riescono a inibire significativamente anche il processo di EMT! Le cellule trattate perdevano la loro forma “aggressiva” e diventavano più simili a cellule normali, meno capaci di migrare e invadere. Questo è stato confermato dalla diminuzione di marcatori EMT come N-caderina e Vimentina e dall’aumento di E-caderina (un marcatore “buono”, associato a minore invasività).

I Risultati Sugli Animali Sono Promettenti
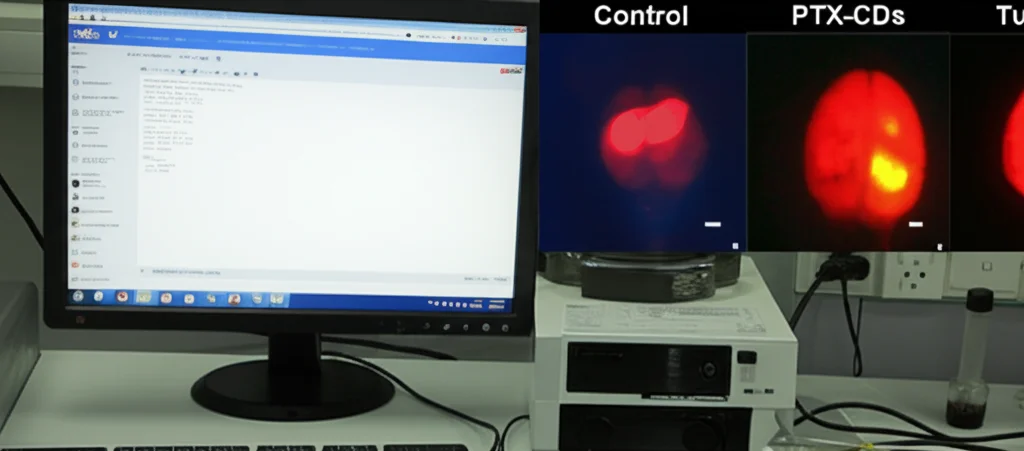
Ovviamente, i test in provetta sono importanti, ma la vera prova del nove è vedere se funziona in un organismo vivente. Abbiamo quindi testato i PTX-CDs su topi in cui avevamo indotto un glioblastoma (modello ortotopico, cioè il tumore cresce nel cervello, proprio come negli umani). Abbiamo somministrato i PTX-CDs per via endovenosa e li abbiamo confrontati con un gruppo di controllo (soluzione salina) e un gruppo trattato con temozolomide (TMZ), il farmaco standard.
I risultati sono stati davvero incoraggianti! I topi trattati con PTX-CDs hanno mostrato una riduzione significativa della crescita tumorale, visibile tramite imaging a bioluminescenza, paragonabile e forse anche leggermente superiore a quella ottenuta con TMZ. Cosa ancora più importante, i topi trattati con PTX-CDs hanno avuto una sopravvivenza significativamente più lunga rispetto ai controlli. L’analisi dei tessuti cerebrali ha confermato la riduzione del tumore e una minore proliferazione cellulare (meno Ki67, un marcatore di proliferazione) nei topi trattati con i nostri punti di carbonio.
Sicurezza Prima di Tutto
Quando si sviluppa un nuovo farmaco, la sicurezza è fondamentale. Abbiamo condotto test preliminari di biocompatibilità. I PTX-CDs si sono dimostrati meno tossici per le cellule sane (fibroblasti) rispetto alle cellule tumorali, a parità di concentrazione (anche se ad alte dosi mostrano tossicità anche per le cellule normali, come molti chemioterapici). Non hanno causato emolisi (rottura dei globuli rossi), indicando una buona compatibilità con il sangue. Nei topi sani, la somministrazione endovenosa non ha causato perdita di peso né danni evidenti agli organi principali (cuore, fegato, milza, polmoni, reni, cervello), come confermato dalle analisi del sangue e dall’esame istologico. Sembra anche che vengano eliminati efficacemente dall’organismo, principalmente attraverso fegato e reni.
Guardando al Futuro: Una Strategia Promettente
Quindi, cosa significa tutto questo? Abbiamo sviluppato un nuovo tipo di punto di carbonio, i PTX-CDs, partendo da un farmaco chemioterapico esistente, il Paclitaxel. Questi PTX-CDs sono molto più solubili, riescono ad attraversare la barriera emato-encefalica, si accumulano nei mitocondri delle cellule tumorali inducendo stress ossidativo e morte cellulare, bloccano la proliferazione e inibiscono l’invasività legata all’EMT. Hanno mostrato un’efficacia antitumorale significativa in modelli animali di glioblastoma, con un profilo di sicurezza preliminare favorevole.
Questa strategia di “riciclare” farmaci noti trasformandoli in nanomateriali con proprietà migliorate è, secondo me, estremamente affascinante. Potrebbe aprire nuove strade per lo sviluppo di terapie contro il glioblastoma (e forse altri tumori cerebrali), potenzialmente accorciando i tempi lunghissimi della ricerca farmaceutica. Certo, la strada è ancora lunga, dobbiamo capire meglio come esattamente attraversano la BBB e ottimizzare ulteriormente questi nanomateriali, ma i risultati iniziali ci danno davvero una grande speranza. È un piccolo passo, ma potrebbe essere l’inizio di qualcosa di importante nella lotta contro questo terribile nemico.
Fonte: Springer