Asma: E se la Chiave Fosse Nascosta in una Proteina? La Sorprendente ITGB3!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona tantissimo: la ricerca sull’asma e le nuove frontiere che stiamo esplorando. Sapete, l’asma è una di quelle condizioni croniche che toccano tantissime persone, bambini e adulti, rendendo a volte difficile anche solo respirare profondamente. È una battaglia costante contro infiammazione, iperreattività delle vie aeree e quel fastidioso rimodellamento strutturale che le rende più strette.
Noi ricercatori siamo sempre alla caccia di nuovi modi per capire meglio questa malattia e, soprattutto, per trovare strategie terapeutiche più efficaci, specialmente per prevenire le crisi e migliorare la qualità della vita anche quando i sintomi sembrano sotto controllo. E se vi dicessi che forse abbiamo trovato un nuovo, inaspettato alleato in questa lotta? Si chiama Integrina β3 (ITGB3).
Cos’è l’Asma e Perché è Così Complicata?
Prima di tuffarci nella nostra scoperta, facciamo un piccolo ripasso. L’asma è caratterizzata principalmente da tre cose:
- Infiammazione cronica delle vie aeree.
- Iperreattività bronchiale (i bronchi reagiscono in modo esagerato agli stimoli).
- Rimodellamento delle vie aeree (cambiamenti strutturali che le ispessiscono e restringono).
Quest’ultimo punto, il rimodellamento, è particolarmente insidioso perché contribuisce alla persistenza della malattia e al rischio di attacchi futuri. Una parte cruciale di questo processo è la cosiddetta Transizione Epitelio-Mesenchimale (EMT). Immaginate le cellule che rivestono le nostre vie aeree (epiteliali) che, sotto stress (come l’esposizione ad allergeni), si trasformano, diventando più simili a cellule del tessuto connettivo (mesenchimali), più mobili e capaci di produrre matrice extracellulare in eccesso. Questo contribuisce all’ispessimento e alla rigidità delle pareti bronchiali. È un meccanismo complesso, spesso attivato da segnali come il TGF-β, e capire come fermarlo è una delle grandi sfide.
Entra in Scena ITGB3: Un Nome da Ricordare?
Qui entra in gioco la nostra protagonista: l’Integrina β3 (ITGB3). Le integrine sono recettori sulla superficie delle cellule che fanno da ponte tra l’interno e l’esterno, fondamentali per l’adesione cellulare e la comunicazione. ITGB3 era già stata “sospettata” in passato: alcuni studi genetici l’avevano identificata come un possibile gene associato alla suscettibilità all’asma, suggerendo addirittura un ruolo protettivo. Ma come esattamente agisse, era un mistero. Ecco dove siamo intervenuti noi! Ci siamo chiesti: può ITGB3 influenzare direttamente quel processo chiave di EMT nell’asma? E se sì, come?
Il Nostro Detective Lavoro: Modelli In Vitro e In Vivo
Per rispondere a queste domande, abbiamo messo in piedi dei modelli sperimentali. Abbiamo usato un allergene comunissimo, l’estratto di acaro della polvere (HDM), per simulare l’asma sia in vitro, su cellule epiteliali delle vie aeree umane (la linea cellulare A549), sia in vivo, in topolini da laboratorio.
L’idea era semplice:
- Esporre le cellule e i topi all’HDM per scatenare una risposta simile all’asma.
- Vedere cosa succedeva ai livelli di ITGB3.
- Manipolare questi livelli: aumentare l’espressione di ITGB3 (sovraespressione) o diminuirla (knockdown) per vedere l’effetto sulla risposta all’HDM.
Abbiamo misurato un sacco di parametri: la vitalità delle cellule, la loro morte programmata (apoptosi), i livelli di citochine infiammatorie tipiche dell’asma (come IL-4, IL-5, IL-13) e, ovviamente, i marcatori della EMT (come E-caderina, N-caderina e vimentina).

Risultati Sorprendenti: ITGB3 Come Scudo Protettivo!
E qui le cose si sono fatte davvero interessanti! Innanzitutto, abbiamo confermato che l’esposizione all’HDM fa parecchi danni: riduce la vitalità delle cellule, aumenta l’apoptosi, scatena l’infiammazione e promuove chiaramente la EMT (meno E-caderina, più N-caderina e vimentina). Abbiamo anche notato che, sia nei pazienti asmatici che nelle cellule trattate con HDM, i livelli di ITGB3 erano più bassi del normale.
Ma la vera svolta è arrivata quando abbiamo giocato con i livelli di ITGB3:
- Diminuire ITGB3 (knockdown): peggiorava tutti gli effetti negativi dell’HDM. Più morte cellulare, più infiammazione, EMT più accentuata. Un disastro!
- Aumentare ITGB3 (sovraespressione): voilà! Gli effetti dannosi dell’HDM venivano contrastati. Le cellule sopravvivevano meglio, l’apoptosi e l’infiammazione diminuivano, e soprattutto, la transizione EMT veniva inibita (più E-caderina, meno N-caderina e vimentina). Era come se ITGB3 agisse da scudo protettivo!
Questi risultati ci dicevano che ITGB3 non solo è associata all’asma, ma gioca un ruolo attivo nel contrastarla, in particolare bloccando quella pericolosa trasformazione cellulare (EMT).
Il Meccanismo Segreto: Smascherare la Via NF-κB
Ok, ITGB3 protegge. Ma come fa? Dovevamo scavare più a fondo nel meccanismo molecolare. I nostri sospetti si sono concentrati su una via di segnalazione cellulare famosissima per il suo ruolo nell’infiammazione: la via del NF-κB. Questo percorso è come un interruttore generale che, quando attivato, accende la produzione di molte molecole infiammatorie.
Abbiamo analizzato lo stato di attivazione di NF-κB nelle nostre cellule. E bingo! L’HDM attivava potentemente la via NF-κB. Ma la cosa più eccitante è stata scoprire che la sovraespressione di ITGB3 riusciva a spegnere questa attivazione indotta dall’HDM! Al contrario, quando abbiamo “forzato” l’attivazione di NF-κB (usando un attivatore specifico), abbiamo visto che questo annullava gli effetti benefici della sovraespressione di ITGB3. In pratica, anche con tanta ITGB3, se NF-κB era acceso artificialmente, le cellule tornavano a soffrire di apoptosi, infiammazione ed EMT.
Questa è stata la prova chiave: ITGB3 esercita i suoi effetti protettivi, almeno in parte significativa, tenendo a bada la via infiammatoria NF-κB, e così facendo blocca anche la EMT.

Dalla Provetta ai Topolini: La Conferma In Vivo
Bello scoprire tutto questo in provetta, ma funziona anche in un organismo complesso? Per verificarlo, siamo passati al nostro modello animale. Abbiamo indotto l’asma nei topolini con HDM e poi abbiamo aumentato i livelli di ITGB3 in alcuni di loro tramite vettori lentivirali (una tecnica per modificare geneticamente le cellule).
I risultati sono stati entusiasmanti e hanno confermato quanto visto in vitro! I topi con più ITGB3 mostravano:
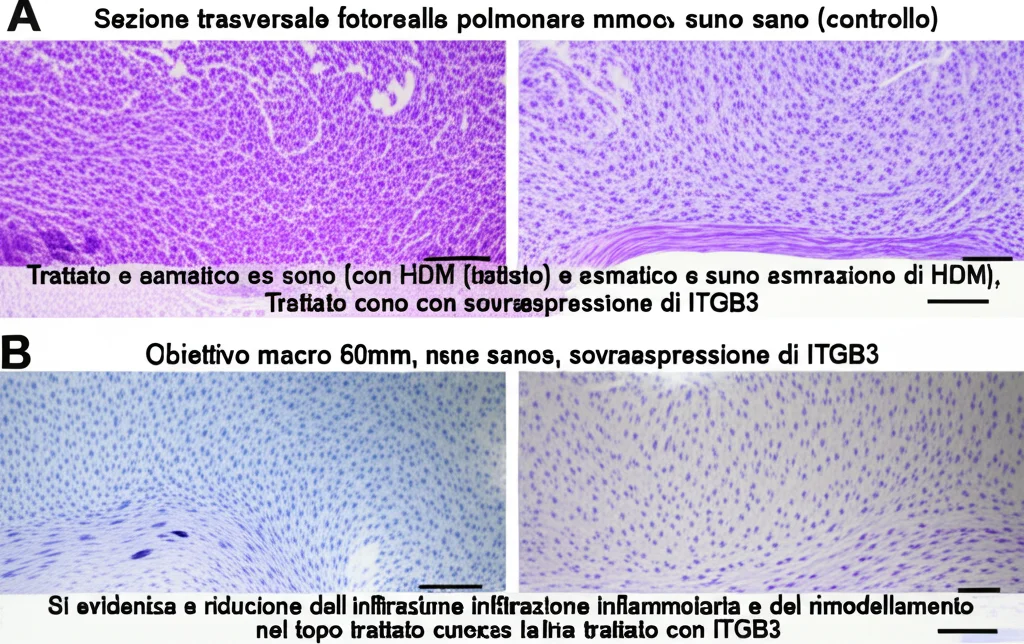
- Meno infiammazione nei polmoni (misurata dalle citochine nel liquido di lavaggio broncoalveolare e dall’infiltrazione di cellule infiammatorie nel tessuto).
- Meno danni strutturali ai polmoni (valutati con l’analisi istologica).
- Minore attivazione della via NF-κB nei tessuti polmonari.
Era la conferma che cercavamo: aumentare ITGB3 proteggeva i polmoni dall’attacco asmatico indotto dall’allergene, riducendo infiammazione e rimodellamento, proprio attraverso il blocco della via NF-κB.
Cosa Significa Tutto Questo per il Futuro?
Beh, questa scoperta è davvero promettente! Abbiamo dimostrato per la prima volta in modo dettagliato che l’Integrina β3 non è solo un marcatore, ma un vero e proprio regolatore negativo dell’asma. Agisce come un freno molecolare, contrastando l’infiammazione e, cosa cruciale, la trasformazione epitelio-mesenchimale (EMT) che contribuisce al rimodellamento cronico delle vie aeree. E lo fa “calmando” la via di segnalazione NF-κB.
Questo apre scenari terapeutici molto interessanti. Immaginate farmaci capaci di aumentare l’espressione o l’attività di ITGB3 specificamente nelle vie aeree dei pazienti asmatici. Potrebbe essere un modo nuovo per affrontare non solo i sintomi, ma anche le cause strutturali della malattia, offrendo una protezione a lungo termine.
Certo, la strada è ancora lunga. Questi sono studi preclinici, fatti su cellule e modelli animali. Serviranno ulteriori ricerche, magari su cellule primarie umane e poi, speriamo, studi clinici per confermare questi risultati nell’uomo e valutare la sicurezza e l’efficacia di un approccio basato su ITGB3. Ma aver identificato questo meccanismo è un passo avanti importantissimo.
È affascinante come il nostro corpo nasconda meccanismi di difesa così sofisticati. Continuare a esplorarli è la nostra missione, nella speranza di trovare, un giorno, soluzioni sempre migliori per chi convive con l’asma. Incrociamo le dita!
Fonte: Springer







