Poloxamer 188: Non Solo un Cerotto per le Cellule Cardiache, Ma un Booster di Ossido Nitrico!
Ragazzi, parliamoci chiaro. Quando il cuore subisce un “colpo”, come un infarto seguito da un intervento per ripristinare il flusso sanguigno (quello che noi scienziati chiamiamo danno da ischemia/riperfusione o I/R), le conseguenze possono essere davvero pesanti. Parliamo di danni seri, a volte permanenti. Da tempo, nel mondo della ricerca, siamo alla caccia di molecole “eroiche” che possano dare una mano al nostro muscolo più importante in questi momenti critici. Una di queste molecole, che ha attirato la nostra attenzione, è il Poloxamer 188, o P188 per gli amici.
Un Eroe Inaspettato: Cos’è il Poloxamer 188?
Il P188 è un tipo particolare di molecola, un copolimero a tre blocchi non ionico. Immaginatelo un po’ come un cerotto molecolare super avanzato. È composto da parti che amano l’acqua (idrofile) e parti che la “odiano” (idrofobe). Questa sua doppia natura gli permette di fare cose incredibili a livello cellulare.
La Vecchia Storia: P188 Come Riparatore di Membrane
Per anni, l’idea prevalente è stata che il P188 agisse principalmente stabilizzando le membrane delle cellule. Pensate alle membrane cellulari come alle mura di una città. Durante un attacco (l’ischemia), queste mura possono danneggiarsi, creando delle brecce. Il P188 sembrava capace di “tappare” questi buchi, impedendo la fuoriuscita di componenti vitali e l’ingresso incontrollato di ioni dannosi, come il calcio, che può mandare in tilt la cellula e portarla alla morte (apoptosi). Funzionava, o almeno così pensavamo, come un sigillante, proteggendo muscoli, neuroni e persino la barriera che protegge il nostro cervello. Studi precedenti, sia in provetta che su cuori isolati, avevano già mostrato che P188 riduceva la morte delle cellule cardiache (i cardiomiociti) se somministrato al momento giusto. Sembrava una storia semplice: P188 ripara le membrane, le cellule sopravvivono meglio. Ma sarà davvero tutto qui?
La Svolta: E Se Ci Fosse di Più? L’Indizio dell’Ossido Nitrico
Qui entriamo in gioco noi e la nostra curiosità. Ci siamo chiesti: e se il P188 facesse qualcosa di più che tappare buchi? Sappiamo che nel danno da I/R un ruolo cruciale lo giocano anche le cellule che rivestono l’interno dei vasi sanguigni, le cellule endoteliali (ECs). Queste cellule sono delle vere e proprie fabbriche di una molecola importantissima per la salute cardiovascolare: l’ossido nitrico (NO). L’NO è un vasodilatatore, aiuta a mantenere il sangue fluido, ha effetti anti-infiammatori… insomma, è un vero toccasana per il cuore e i vasi. E se P188, oltre a proteggere le cellule muscolari del cuore (i cardiomiociti, CMs), desse una mano anche alle cellule endoteliali, magari proprio stimolando la produzione di NO? Questa è stata la nostra ipotesi, una pista nuova e affascinante.
Dentro il Laboratorio: Come Abbiamo Scoperto il Segreto
Per vederci chiaro, abbiamo messo in piedi un disegno sperimentale bello tosto. Abbiamo usato una tecnologia pazzesca: cellule derivate da cellule staminali pluripotenti indotte (iPSC). In pratica, siamo partiti da cellule adulte riprogrammate per tornare “bambine” e poi le abbiamo fatte diventare cellule cardiache (iPSC-CMs) e cellule endoteliali (iPSC-ECs) umane, perfettamente funzionanti in laboratorio. Il vantaggio? Avere cellule umane illimitate, senza le variabilità tra donatori e i problemi delle cellule primarie.
Abbiamo simulato l’attacco cardiaco in una piastra di coltura: abbiamo tolto ossigeno e glucosio alle cellule (ipossia) e poi glieli abbiamo ridati (riossigenazione), aggiungendo diverse concentrazioni di P188. Volevamo vedere cosa succedeva alla sopravvivenza, alla funzione delle cellule e, soprattutto, alla produzione di NO.
Non ci siamo fermati qui. Siamo passati a un modello più complesso: cuori isolati di ratto (modello ex-vivo di Langendorff). Abbiamo indotto un danno da I/R anche in questi cuori e abbiamo somministrato P188 durante la fase di riperfusione, misurando la funzione cardiaca e la produzione di NO. E per essere sicuri del ruolo dell’NO, abbiamo fatto lo stesso esperimento bloccando la produzione di NO con un inibitore specifico (L-NAME).
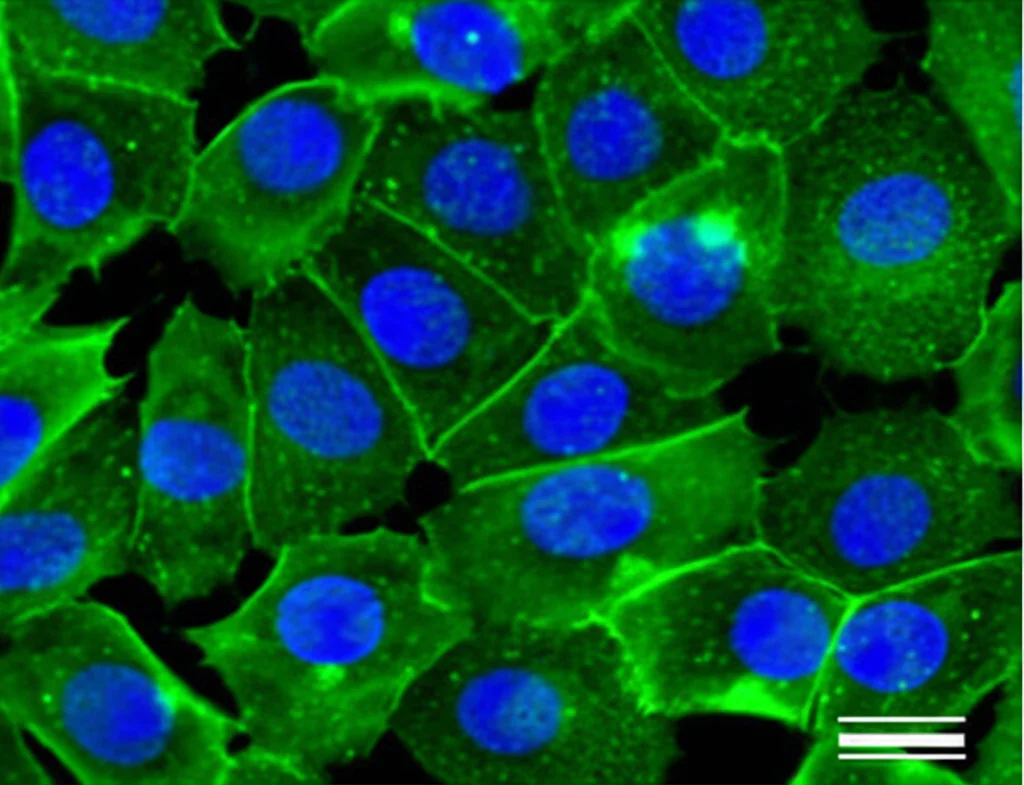
I Risultati Parlano Chiaro: Dalle Cellule ai Cuori
I risultati sono stati elettrizzanti!
- Nelle cellule iPSC: Il P188 ha protetto i cardiomiociti (iPSC-CMs) dal danno da ipossia/riossigenazione in modo dose-dipendente, migliorando la loro sopravvivenza (quasi il 90% contro il 50% senza P188!) e la loro capacità di contrarsi e rilassarsi. Ha anche ridotto l’apoptosi (la morte cellulare programmata). Ma la vera sorpresa è arrivata dalle cellule endoteliali (iPSC-ECs): il P188 non solo le ha protette, ma ha aumentato significativamente la produzione intracellulare di NO (circa il 50% in più rispetto al controllo!). Questo effetto sull’NO era particolarmente evidente dopo 8 ore di riossigenazione, suggerendo che P188 aiuta le cellule a riprendersi e a riattivare meccanismi protettivi.
- Nei cuori di ratto isolati: I risultati ex-vivo hanno confermato tutto. La somministrazione di P188 durante la riperfusione ha migliorato notevolmente la funzione cardiaca (miglior contrazione, miglior rilassamento) e ha ridotto l’area dell’infarto. E la prova del nove? Quando abbiamo bloccato la produzione di NO con L-NAME, tutti gli effetti benefici del P188 sono svaniti! Questo ci ha dato la conferma definitiva: l’NO è un mediatore chiave dell’azione cardioprotettiva del P188. Addirittura, abbiamo visto che P188 aumentava la produzione di NO in modo dose-dipendente anche in cuori sani, non ischemici.
Perché l’Ossido Nitrico è Così Importante?
L’NO prodotto dalle cellule endoteliali è fondamentale. Agisce sulle cellule muscolari lisce dei vasi facendole rilassare (vasodilatazione), migliorando il flusso sanguigno. Ma fa molto di più: protegge le stesse cellule endoteliali, riduce l’infiammazione, previene l’aggregazione piastrinica e combatte lo stress ossidativo. Nel contesto dell’I/R, un aumento di NO può:
- Stabilizzare l’equilibrio del calcio nei cardiomiociti, prevenendo la contrattura e la morte cellulare.
- Attivare vie di segnalazione che proteggono i mitocondri (le centrali energetiche della cellula).
- Contrastare i radicali liberi dell’ossigeno (ROS), molecole dannose prodotte in abbondanza durante la riperfusione.
- Ottimizzare il metabolismo energetico delle cellule cardiache.
Il fatto che P188 potenzi la produzione di NO aggiunge quindi un potentissimo strumento al suo arsenale protettivo.
Un Meccanismo a Doppio Filo: Membrana e NO
Quindi, la nostra ricerca svela un quadro più complesso e affascinante. Il Poloxamer 188 non è solo un “riparatore” passivo di membrane danneggiate. Sì, probabilmente la sua capacità di stabilizzare le membrane aiuta anche le cellule endoteliali a funzionare meglio, magari migliorando l’efficienza dell’enzima che produce NO (l’eNOS), che si trova proprio sulla membrana. Ma l’effetto sull’NO sembra andare oltre. P188 agisce attivamente potenziando questa via di segnalazione cruciale. È un meccanismo a doppio filo: stabilizzazione della membrana E aumento della produzione di NO. Una combinazione potentissima contro il danno da I/R.
Cosa Ci Riserva il Futuro?
Certo, come in ogni ricerca, ci sono dei limiti. Abbiamo usato solo ratti maschi, per esempio, e dovremo approfondire l’interazione tra P188, NO e lo stress ossidativo (ROS), che è un gioco complesso di equilibri. Sarà fondamentale studiare meglio la comunicazione diretta tra cellule endoteliali e cardiomiociti (il cosiddetto crosstalk) usando colture miste.
Ma i risultati sono estremamente promettenti. Aver dimostrato questo nuovo meccanismo d’azione basato sull’NO, sia in modelli cellulari umani avanzati che in cuori interi, apre strade importanti. Il Poloxamer 188, e forse anche suoi derivati più recenti, si conferma un candidato terapeutico molto interessante per mitigare i danni cardiaci legati all’ischemia e riperfusione. La nostra scoperta aggiunge un tassello fondamentale alla comprensione di come funziona e rafforza la speranza di poterlo, un giorno, usare clinicamente per proteggere il cuore dei pazienti. La ricerca continua!
Fonte: Springer