PKM2 Extracellulare: Il Regista Nascosto che Manipola l’Immunità Tumorale e Cambia le Regole del Gioco
Amici della scienza, preparatevi per un viaggio affascinante nel microscopico mondo del cancro e del nostro sistema immunitario. Oggi voglio parlarvi di una scoperta che mi ha letteralmente lasciato a bocca aperta, una di quelle che potrebbe davvero cambiare le carte in tavola nelle terapie oncologiche. Sto parlando di una proteina chiamata PKM2, ma non nella sua veste “classica” all’interno della cellula, bensì quando se ne va a spasso fuori, nello spazio extracellulare. E cosa combina lì? Beh, sembra che giochi un ruolo da protagonista nel modulare come il nostro sistema immunitario risponde al tumore, in particolare influenzando dei soldati speciali chiamati macrofagi.
Il Tumore: Un Abile Manipolatore dell’Immunità
Una delle domande che da sempre ci assilla è: “Come fanno le cellule tumorali a sfuggire alla distruzione da parte del nostro sistema immunitario?” Sembra quasi una beffa, no? Il nostro corpo ha un esercito pronto a difenderci, eppure il cancro riesce spesso a farla franca. La verità, un po’ scomoda, è che il tumore è un maestro della manipolazione. Non solo elude le difese, ma riesce persino a “corrompere” le cellule immunitarie presenti nel suo microambiente, trasformandole da nemiche ad alleate che ne favoriscono la crescita e la diffusione. Pensate un po’!
Tra queste cellule “educate” dal tumore, i macrofagi associati al tumore (TAM) sono tra i più abbondanti e significativi. I macrofagi sono cellule incredibilmente versatili; possono assumere diverse “personalità” o polarità. Le due principali sono:
- M1 (classicamente attivati): i “guerrieri”, pro-infiammatori, che combattono attivamente il tumore.
- M2 (alternativamente attivati): i “riparatori”, anti-infiammatori o pro-rigenerazione, che in contesti tumorali, purtroppo, finiscono per favorire la crescita del cancro, la sua capacità di dare metastasi e la resistenza alle terapie.
La cosa interessante è che questa polarizzazione non è fissa; i macrofagi possono passare da M1 a M2 e viceversa, a seconda dei segnali che ricevono dall’ambiente circostante. Nelle fasi iniziali del cancro, i TAM tendono ad essere M1, ma con il progredire della malattia, il tumore li “rieduca” prevalentemente verso il fenotipo M2. Ed è qui che entra in gioco la nostra protagonista.
PKM2: Non Solo un Enzima Metabolico
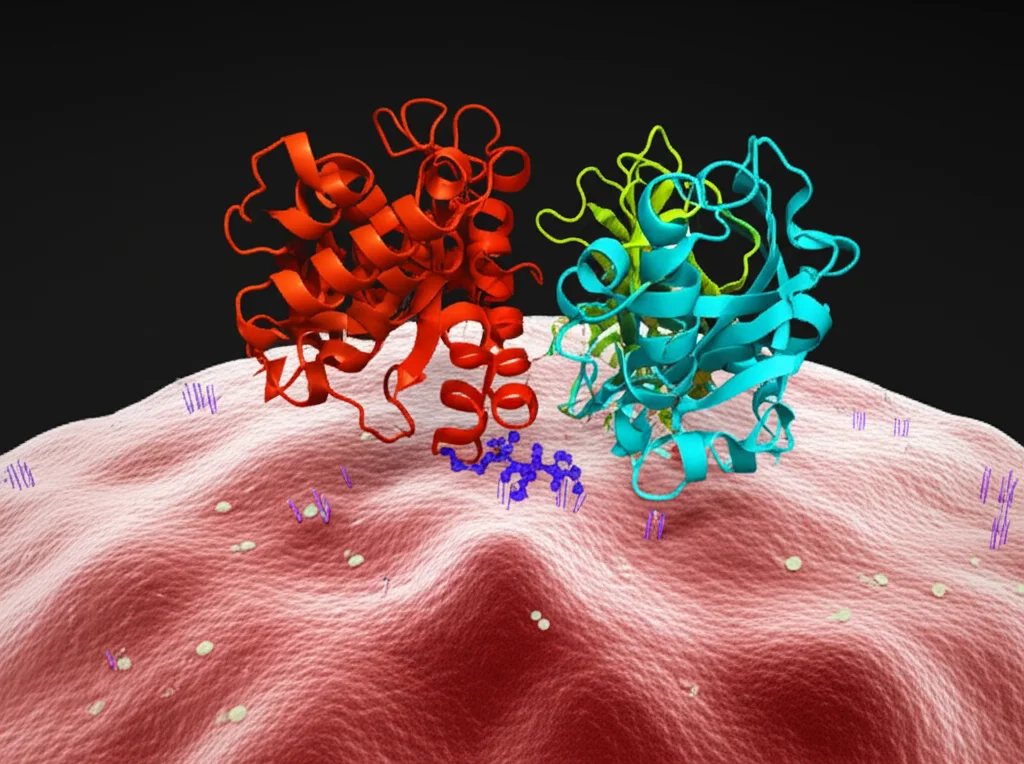
La Piruvato Kinasi M2 (PKM2) è un enzima ben noto per il suo ruolo nel metabolismo del glucosio, l’ultimo step della glicolisi. Ma negli ultimi anni, abbiamo scoperto che la PKM2 è molto più di un semplice operaio metabolico. Può esistere in forma di dimero o tetramero, con funzioni diverse, e può trovarsi in varie parti della cellula, regolando processi che vanno dal metabolismo alla trascrizione genica, fino all’organizzazione della cromatina. Insomma, una vera e propria proteina multitasking!
Da tempo si osserva che pazienti con tumori solidi o con varie malattie infiammatorie presentano alti livelli di PKM2 nel sangue. Questo ha fatto sorgere un sospetto: e se la PKM2 rilasciata dalle cellule, la cosiddetta PKM2 extracellulare (EcPKM2), avesse un ruolo attivo in questi processi patologici? Studi precedenti del nostro gruppo avevano già dimostrato che l’EcPKM2 facilita la crescita tumorale promuovendo l’angiogenesi (la formazione di nuovi vasi sanguigni che nutrono il tumore) e che viene rilasciata anche durante la riparazione delle ferite, aiutando il processo. Recentemente, abbiamo anche visto che i miofibroblasti, cellule coinvolte nella fibrosi e presenti anche nel microambiente tumorale, aumentano la produzione e secrezione di PKM2 quando attivati.
Ora, la nuova, entusiasmante scoperta è che l’EcPKM2 ha un altro asso nella manica: modula l’immunità tumorale spingendo i macrofagi verso la polarità M2, quella pro-tumorale. E come fa? Andiamo a scoprirlo.
La Danza Molecolare: EcPKM2 e i Macrofagi
Abbiamo scoperto che l’EcPKM2, una volta fuori dalla cellula tumorale, non vaga a caso. Cerca un partner specifico sulla superficie dei macrofagi: una proteina chiamata integrina αvβ3. Le integrine sono recettori che permettono alle cellule di interagire con l’ambiente esterno e con altre cellule. Abbiamo confermato che i macrofagi esprimono abbondantemente questa integrina.
Attraverso una serie di esperimenti, abbiamo dimostrato che:
- Le cellule di macrofago (sia linee cellulari come Raw264.7 sia macrofagi derivati da midollo osseo di topo, BMMφ) si “attaccano” preferenzialmente a piastre rivestite con PKM2 ricombinante (rPKM2), e questo attacco dipende proprio dall’integrina αvβ3.
- L’EcPKM2 e l’integrina β3 possono essere “pescate” insieme dagli estratti cellulari, confermando la loro interazione fisica.
- Nei tumori di modelli animali, la rPKM2 marcata si lega in modo significativo ai macrofagi tumorali.
Ma qual è la conseguenza di questo legame? Abbiamo osservato che i macrofagi trattati con rPKM2 cambiano morfologia, diventando simili a quelli trattati con IL-4 (un noto induttore di M2). E non solo: iniziano a secernere alti livelli di IL-10 (una citochina tipica degli M2) e ad esprimere sulla loro superficie il marcatore CD206 (anch’esso caratteristico degli M2). Al contrario, i marcatori M1 come CD86 e iNOS (ossido nitrico sintasi inducibile) diminuiscono. Addirittura, l’EcPKM2 sembra capace di “convertire” macrofagi M1 (precedentemente attivati con LPS, un induttore M1) verso un fenotipo M2, riducendo la secrezione di TNFα (una citochina pro-infiammatoria M1).
Dalle Provette ai Modelli Viventi: La Conferma Sperimentale
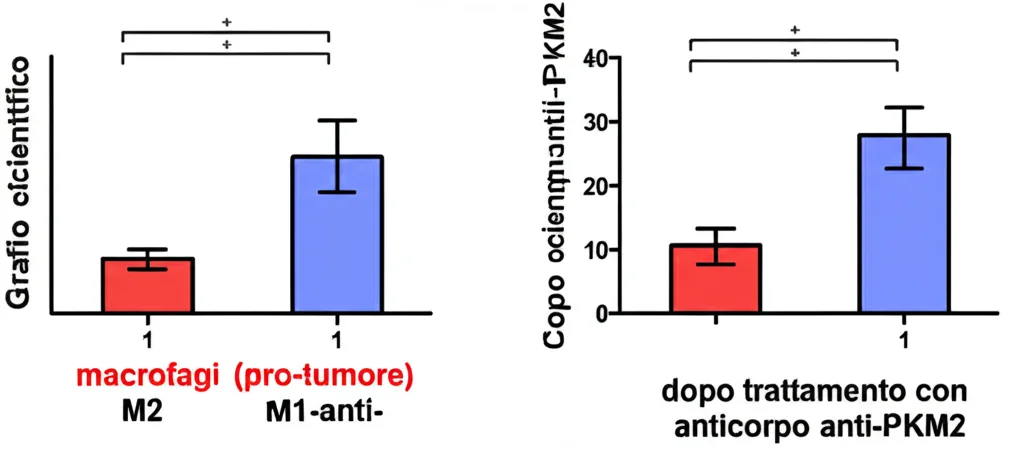
Per vedere se questi effetti si verificavano anche in vivo, abbiamo utilizzato diversi modelli murini di cancro: un modello di cancro al seno (4T1), un melanoma (B16) e un modello di cancro al polmone geneticamente ingegnerizzato (GEM-NSCLC). Trattando i topi portatori di tumore con una forma mutante di PKM2 (G415R, più solubile e dimerica) abbiamo osservato un aumento della crescita tumorale, del peso e delle dimensioni dei tumori. Ma la cosa più importante è che, analizzando le cellule immunitarie all’interno di questi tumori, abbiamo visto un aumento della percentuale di macrofagi M2 e una diminuzione degli M1. Di conseguenza, aumentavano anche le cellule T regolatorie (Treg), che sopprimono la risposta immunitaria anti-tumorale, e diminuivano le cellule T citotossiche CD8+, i veri killer del cancro. Questo si traduceva anche in un aumento delle metastasi polmonari, anch’esse ricche di macrofagi M2 e Treg.
A questo punto, la domanda sorge spontanea: se l’EcPKM2 fa tutto questo “danno”, possiamo bloccarla? Abbiamo sviluppato un anticorpo monoclonale anti-PKM2 (chiamato PKAb) che è in grado di disturbare l’interazione tra EcPKM2 e l’integrina αvβ3. Ebbene, trattando i topi con questo anticorpo, abbiamo ottenuto l’effetto opposto! La crescita tumorale è stata inibita, le metastasi ridotte, e, cosa cruciale, nei tumori c’era una maggiore popolazione di macrofagi M1 e una minore di M2 e Treg. Questi risultati sono stati consistenti in tutti i modelli tumorali testati, suggerendo che questo meccanismo è abbastanza generalizzato.
Svelare il Meccanismo: Come EcPKM2 Tira le Fila
Ma come fa esattamente l’interazione EcPKM2-integrina αvβ3 a cambiare la polarità dei macrofagi? Sospettavamo che venisse attivata una via di segnalazione intracellulare a valle dell’integrina. E infatti, abbiamo scoperto che l’EcPKM2 attiva una cascata di segnali nota come asse integrina-FAK-PI3K.
Ecco i passaggi chiave che abbiamo identificato:
- L’EcPKM2 si lega all’integrina αvβ3.
- Questo legame attiva la proteina FAK (Focal Adhesion Kinase).
- FAK attivata, a sua volta, attiva PI3K (Phosphoinositide 3-kinase).
- L’attivazione di PI3K porta alla soppressione di un’altra proteina chiamata PTEN. PTEN è un noto soppressore tumorale che, tra le altre cose, contrasta l’attività di PI3K.
- La soppressione di PTEN causa un aumento dell’espressione e dell’attività di Arginasi-1 (Arg1). Arg1 è un enzima chiave per la funzione dei macrofagi M2, poiché consuma arginina, sottraendola alla produzione di ossido nitrico (tipico degli M1) e favorendo invece la produzione di molecole che promuovono la riparazione tissutale e la crescita cellulare (che nel cancro, significa crescita tumorale).
Abbiamo confermato questi passaggi utilizzando inibitori specifici per FAK e PI3K, che bloccavano gli effetti dell’EcPKM2 sull’attivazione di Arg1. Inoltre, “spegnendo” l’integrina β3 o sovraesprimendo PTEN nei macrofagi, siamo riusciti ad annullare l’effetto pro-M2 dell’EcPKM2. Questo ci ha dato la prova che l’EcPKM2 orchestra la polarizzazione M2 proprio attraverso questa via di segnalazione integrina-FAK-PI3K-PTEN-Arg1. È un meccanismo elegante e, devo dire, piuttosto astuto da parte del tumore!
Una Nuova Speranza Terapeutica: L’Anticorpo Anti-PKM2
La parte più entusiasmante di questa ricerca, per me, è il potenziale terapeutico. Se il nostro anticorpo PKAb può “riprogrammare” i macrofagi da M2 (pro-tumore) a M1 (anti-tumore), potrebbe rappresentare una nuova strategia per combattere il cancro. E cosa succede se lo combiniamo con le terapie immunitarie già esistenti, come gli inibitori dei checkpoint immunitari (ad esempio, anti-PD-1)?
Abbiamo testato questa combinazione nel modello di melanoma B16. Da soli, sia l’anticorpo PKAb sia l’anti-PD-1 avevano effetti modesti sulla sopravvivenza degli animali e sulla crescita tumorale. Ma la combinazione dei due ha mostrato effetti anti-cancro significativamente potenziati! Questo suggerisce che colpire l’EcPKM2 potrebbe rendere i tumori più sensibili all’immunoterapia, un risultato davvero promettente.
Un vantaggio di prendere di mira l’EcPKM2 è che questa proteina sembra agire su più fronti per promuovere il cancro: non solo sui macrofagi, ma anche, come avevamo visto in precedenza, sull’angiogenesi e forse anche sui fibroblasti associati al cancro (CAF), che sono simili ai miofibroblasti. Quindi, un singolo agente terapeutico potrebbe colpire simultaneamente diverse vie che il tumore usa per crescere e diffondersi. Inoltre, i livelli di PKM2 circolante sono generalmente bassi o non rilevabili negli individui sani, il che fa ben sperare per la sicurezza di una terapia mirata a neutralizzarla. E, non da ultimo, i livelli di PKM2 nel siero dei pazienti potrebbero persino servire come biomarcatore per predire la risposta al trattamento.

Implicazioni Più Ampie e Prospettive Future
Questa scoperta ci porta a riflettere sul ruolo dell’EcPKM2 in un contesto più ampio. Sembra che l’EcPKM2 possa agire come un “ponte” tra la risposta infiammatoria iniziale e una fase successiva di proliferazione/rigenerazione, sia nella riparazione delle ferite (dove è benefica) sia nella progressione del cancro (dove è dannosa). Nei tumori in stadio avanzato, dove le cellule tumorali e i CAF rilasciano abbondante EcPKM2, questa proteina orchestra una sorta di “finta rigenerazione” che in realtà favorisce la crescita tumorale, la sopravvivenza delle cellule cancerose e la metastasi, in parte proprio “educando” i macrofagi verso il fenotipo M2.
C’è ancora molto da esplorare. Ad esempio, la via FAK-PI3K attivata dall’EcPKM2 potrebbe influenzare anche altri attori molecolari importanti per la polarità dei macrofagi, come l’asse AKT-mTOR. Capire appieno tutti i dettagli di questa complessa rete di interazioni sarà fondamentale.
In conclusione, credo che abbiamo scoperchiato un meccanismo nuovo e importante attraverso cui il tumore manipola il sistema immunitario. L’EcPKM2 emerge come un bersaglio terapeutico incredibilmente interessante, con il potenziale non solo di inibire direttamente la crescita tumorale, ma anche di “risvegliare” il sistema immunitario contro il cancro. La strada è ancora lunga, ma scoperte come questa ci danno la speranza e la motivazione per continuare a lottare. E chissà, forse un giorno potremo dire di aver aggiunto un’altra potente freccia al nostro arco contro questa terribile malattia.
Fonte: Springer