Osteonecrosi e Denti: La Luce Laser PBM è la Svolta per Pazienti a Rischio?
Ciao a tutti! Oggi voglio parlarvi di un argomento che sta molto a cuore a noi professionisti del settore dentale e, soprattutto, ai nostri pazienti più fragili: l’osteonecrosi della mandibola legata ai farmaci, o MRONJ (Medication-Related Osteonecrosis of the Jaw). È una condizione seria, un po’ un incubo, che può colpire chi assume determinati farmaci per l’osteoporosi o per trattamenti oncologici. E la domanda che ci tormenta è: come possiamo aiutare questi pazienti quando hanno bisogno, ad esempio, di un’estrazione dentale, senza scatenare questo mostro?
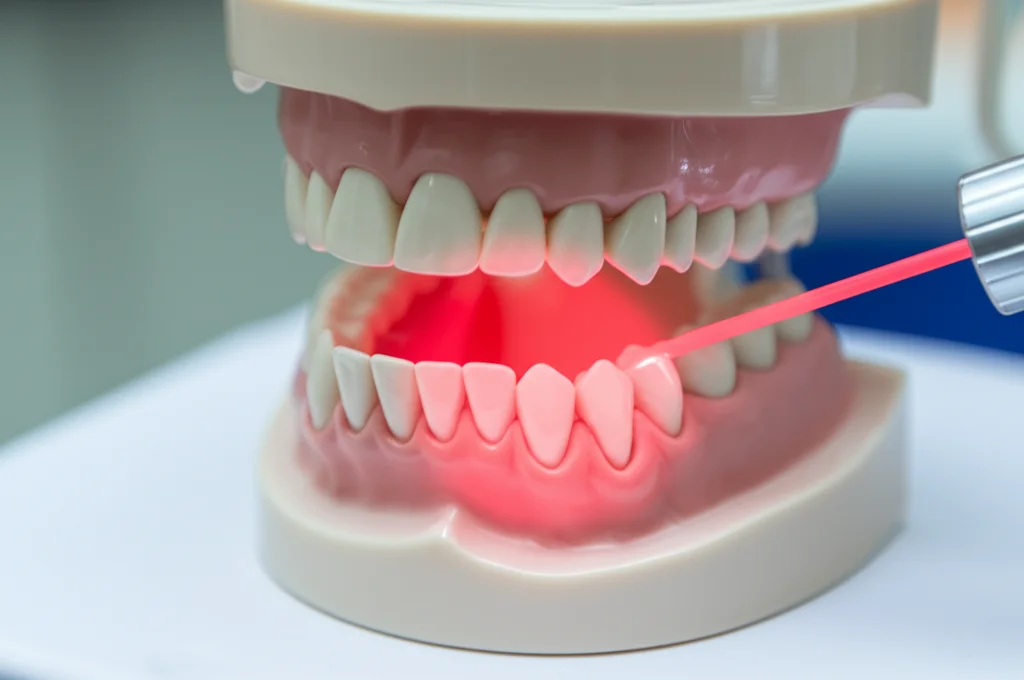
Beh, sembra che un raggio di luce – letteralmente – possa venire in nostro soccorso. Sto parlando della fotobiomodulazione (PBM), una terapia che usa la luce a bassa potenza per stimolare i processi biologici. Recentemente, abbiamo condotto uno studio retrospettivo, un po’ come guardare indietro nei nostri archivi, per vedere se la PBM potesse davvero fare la differenza come supporto alle estrazioni chirurgiche in pazienti a rischio di MRONJ. E i risultati sono… beh, continuate a leggere!
Cos’è l’Osteonecrosi della Mandibola Farmaco-Correlata (MRONJ)?
Prima di tuffarci nello studio, facciamo un passo indietro. La MRONJ è definita come una reazione avversa a farmaci che porta alla distruzione progressiva dell’osso mascellare o mandibolare, in pazienti che assumono (o hanno assunto) farmaci noti per aumentare questo rischio, e che non hanno subito radioterapia recente in testa o collo. Chi sono questi pazienti? Principalmente persone in cura per patologie oncologiche o osteometaboliche (come l’osteoporosi severa).
I farmaci “incriminati” sono soprattutto gli anti-riassorbitivi (come i famosi bisfosfonati o il denosumab) e/o gli anti-angiogenici (farmaci che bloccano la formazione di nuovi vasi sanguigni, usati in oncologia).
Storicamente, si è sempre puntato il dito contro le estrazioni dentali e le procedure chirurgiche invasive come principale fattore scatenante (circa il 73% dei casi!). Ma la ricerca recente sta un po’ cambiando le carte in tavola. Si inizia a pensare che forse non è tanto l’estrazione in sé, quanto la presenza di un’infezione preesistente (come parodontiti gravi o perimplantiti) a giocare un ruolo chiave. Estrarre un dente già compromesso da un’infezione potrebbe addirittura ridurre il rischio, eliminando il focolaio! Insomma, l’infezione ossea sembra essere il vero “cattivo” della storia, più che la chirurgia in sé. Ovviamente, ci sono anche altri fattori da considerare: il tipo di farmaco, la durata della terapia, fattori sistemici (come il diabete o l’uso di corticosteroidi) e fattori locali.
La Sfida della Prevenzione e l’Intrigo della Fotobiomodulazione (PBM)
Le linee guida attuali (sia americane che italiane) mettono ancora la prevenzione al primo posto. Questo significa igiene orale impeccabile e, quando un intervento è inevitabile, procedure il meno traumatiche possibili, spesso accompagnate da una profilassi antibiotica. L’idea è prevenire l’infezione ossea post-intervento.
Il problema? Non c’è un protocollo standardizzato per gli antibiotici (quale tipo? quando? per quanto tempo?), e c’è sempre il rischio crescente dell’antibiotico-resistenza. Inoltre, questi pazienti sono spesso già debilitati, e bombardarli di antibiotici non è mai l’ideale.
Ecco perché si cercano alternative, terapie aggiuntive che possano aiutare la guarigione e ridurre la necessità di antibiotici. Si è parlato di ossigenoterapia iperbarica, ozonoterapia, concentrati piastrinici autologhi (come il PRF) e, appunto, della fotobiomodulazione (PBM).
La PBM usa luce non ionizzante (laser a bassa potenza o LED) per “parlare” con le cellule. Non si sa ancora *tutto* sul suo meccanismo d’azione, ma sappiamo che può innescare effetti anti-infiammatori, analgesici e bio-modulatori, aiutando i tessuti a ripararsi. L’abbiamo già vista all’opera con successo per trattare mucositi orali, lichen planus, disturbi dell’articolazione temporo-mandibolare e persino per ridurre dolore e gonfiore dopo l’estrazione dei denti del giudizio. Alcuni studi l’hanno proposta anche per *trattare* la MRONJ già conclamata, a volte come palliativo, altre volte come supporto alla chirurgia. Ma l’idea di usarla *prima* che la MRONJ si sviluppi, come prevenzione durante le estrazioni in pazienti a rischio… beh, quella è relativamente nuova e super interessante!
Il Nostro Studio Retrospettivo: Cosa Abbiamo Fatto?
Presso il Dipartimento di Scienze Odontostomatologiche e Maxillo Facciali della Sapienza Università di Roma, all’interno del progetto “MoMax” che si occupa proprio di pazienti fragili e oncologici, abbiamo analizzato le cartelle cliniche dei pazienti trattati tra il 2016 e il 2023.
I criteri erano chiari:
- Pazienti a rischio di MRONJ (in terapia attuale o passata con farmaci modificanti l’osso, con o senza anti-angiogenici).
- Sottoposti a una o più estrazioni dentali.
- Sottoposti al nostro protocollo preventivo con PBM.
- Senza una diagnosi pregressa o attuale di MRONJ.
Abbiamo escluso chi aveva già la MRONJ, chi aveva fatto radioterapia testa-collo, chi prendeva solo anti-angiogenici e i minori di 18 anni.
Abbiamo raccolto un sacco di dati: età, sesso, abitudini (fumo, alcol), dettagli sui farmaci (tipo, durata, via di somministrazione), fattori di rischio sistemici (patologia di base – oncologica, osteoporosi, ecc. -, chemioterapia, corticosteroidi, diabete, patologie tiroidee, ipertensione) e il numero e la sede delle estrazioni.
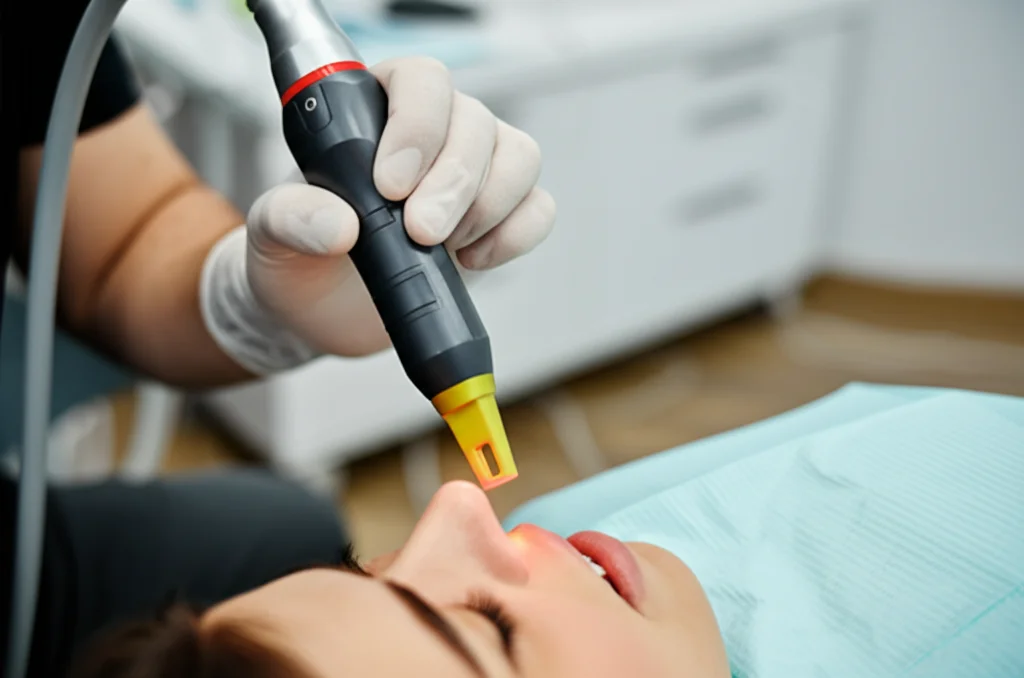
Il nostro protocollo PBM prevedeva quattro sedute: due prima dell’intervento (6 e 2 giorni prima) e due dopo (2 e 6 giorni dopo). Abbiamo usato un laser multi-diodico (con lunghezze d’onda di 650 nm, 810 nm e 910 nm simultaneamente), irradiando l’area dell’estrazione senza contatto (~1 cm di distanza) per 15 minuti a sessione, con una potenza totale di 0.6 W e una frequenza di 30 kHz, per un’energia totale di 577.4 J per seduta. Se c’erano più estrazioni distanti tra loro, ripetevamo l’applicazione nella stessa seduta.
Tutti i pazienti, inoltre, seguivano una profilassi antibiotica standard (amoxicillina/acido clavulanico + metronidazolo da 3 giorni prima a 7 giorni dopo l’intervento) e usavano un collutorio alla clorexidina. La “vacanza terapeutica” dai farmaci a rischio veniva valutata caso per caso con il medico prescrittore.
I Risultati: Cosa Abbiamo Scoperto?
Alla fine, abbiamo incluso nello studio 62 pazienti (58 donne e 4 uomini), con un’età media di circa 67 anni e mezzo. La maggior parte (71%) assumeva farmaci a basso dosaggio (LD-BMAs), tipicamente per osteoporosi o perdita ossea indotta da trattamenti oncologici (CTIBL), mentre il 29% assumeva farmaci ad alto dosaggio (HD-BMAs), prevalentemente pazienti oncologici. La durata media della terapia con questi farmaci era di quasi 54 mesi. In media, abbiamo estratto 2.3 denti per paziente.
E ora, il dato clou: 50 pazienti (l’80.65%) hanno avuto una guarigione completa senza sviluppare MRONJ! Fantastico, no? Purtroppo, 12 pazienti (il 19.35%) hanno invece sviluppato la MRONJ.
Analizzando i dati per capire chi avesse avuto più problemi, sono emerse alcune cose interessanti:
- Un rischio significativamente più alto di MRONJ è stato osservato nei pazienti che avevano assunto acido zoledronico (un potente bisfosfonato endovenoso) (p=0.029).
- Anche la somministrazione per via endovenosa (I.V.) in generale era associata a un rischio maggiore (p=0.029).
- Tra i fattori sistemici, l’uso concomitante di corticosteroidi aumentava significativamente il rischio (p=0.039). L’Odds Ratio (OR) era addirittura 5.75, significa che chi prendeva cortisone aveva quasi 6 volte più probabilità di sviluppare MRONJ nel nostro campione!
- Curiosamente, i pazienti in trattamento per patologie tiroidee sembravano avere un rischio leggermente inferiore, anche se la significatività statistica era al limite (p=0.055).
Questi risultati confermano un po’ quello che già si sospettava: l’acido zoledronico e i corticosteroidi sono “clienti” tosti quando si parla di rischio MRONJ.
Interpretazione e Discussione: Perché la PBM Potrebbe Funzionare (e Perché Non Sempre)?
Quel tasso di successo dell’80.65% è incoraggiante. Potrebbe essere dovuto proprio agli effetti positivi della PBM: stimolazione del metabolismo cellulare, miglioramento della microcircolazione grazie al rilascio di ossido nitrico (NO), attivazione di geni che promuovono la produzione di fattori di crescita, effetti anti-infiammatori e forse anche analgesici. La luce laser sembra “risvegliare” le cellule, specialmente quelle che soffrono in un ambiente acido post-infortunio, e stimolare anche le cellule ossee (osteoblasti) a fare il loro lavoro.
Certo, il 19.35% di insuccessi ci ricorda che la MRONJ è una bestia complessa e multifattoriale. La PBM non è una bacchetta magica. La letteratura scientifica mostra tassi di incidenza di MRONJ post-estrattiva molto variabili, specialmente nei pazienti oncologici ad alte dosi di farmaci (dal 11% fino al 50% in alcuni studi!). Il nostro risultato si colloca in questo range, ma l’idea è che la PBM possa aver contribuito a mantenerlo verso l’estremità inferiore.
Altri studi che hanno usato la PBM in prevenzione hanno riportato risultati forse anche migliori, ma spesso usavano protocolli diversi o combinavano la PBM con altre tecniche, come la terapia fotodinamica (PDT) o i concentrati piastrinici. Questo rende i confronti difficili.
Una delle grandi sfide con la PBM è proprio la mancanza di protocolli standardizzati. I parametri del laser (lunghezza d’onda, potenza, tempo, energia, frequenza) sono tantissimi e una dose inadeguata potrebbe non funzionare o addirittura essere controproducente. C’è un grande bisogno di studi che riportino i protocolli in modo dettagliato e standardizzato.
L’altra sfida è la complessità del paziente. Non basta dire “paziente a rischio”. Bisogna considerare la dose del farmaco (alta o bassa?), la durata della terapia, la presenza di altri fattori di rischio sistemici (corticosteroidi, diabete…) e locali (stato parodontale del dente da estrarre, presenza di protesi incongrue, infezioni…). Analizzare il “profilo di rischio” individuale è fondamentale per capire perché un trattamento funziona in un paziente e non in un altro.
Limiti e Prospettive Future
Dobbiamo essere onesti sui limiti del nostro studio:
- È retrospettivo: abbiamo guardato dati già esistenti, il che è meno potente di uno studio prospettico (dove si pianifica tutto prima).
- È monocentrico: i risultati vengono da un solo ospedale. Servirebbero studi multicentrici.
- Manca un gruppo di controllo: non abbiamo potuto confrontare direttamente i pazienti trattati con PBM con un gruppo simile non trattato (per ovvi motivi etici, dato che la PBM è considerata benefica).
- Alcuni dati mancavano (come la dose accumulata esatta dei farmaci) e non abbiamo potuto valutare a fondo tutti i fattori di rischio locali per la natura retrospettiva.
Nonostante ciò, crediamo che questo studio aggiunga un tassello importante. La maggior parte dei nostri pazienti a rischio ha beneficiato della PBM come supporto all’estrazione, guarendo senza problemi. Abbiamo confermato che fattori come l’acido zoledronico e i corticosteroidi sono campanelli d’allarme importanti.

Cosa ci serve per il futuro? Sicuramente studi più robusti: prospettici, randomizzati e controllati (se eticamente fattibili), multicentrici, con criteri di inclusione più specifici, protocolli PBM dettagliati e standardizzati, e un’analisi approfondita del profilo di rischio completo di ogni paziente. Solo così potremo capire davvero il potenziale della PBM nella prevenzione di questa complicanza così temuta.
In conclusione, la fotobiomodulazione si conferma una strada promettente e affascinante per aiutare i nostri pazienti più vulnerabili ad affrontare le cure dentali necessarie con maggiore sicurezza. Non è ancora la soluzione definitiva per tutti, ma è un’arma in più nel nostro arsenale, un raggio di speranza supportato da dati incoraggianti. Continueremo a studiare e a cercare le strategie migliori per proteggere il sorriso e la salute dei nostri pazienti!
Fonte: Springer