Parodontite: Ho Scoperto Come un Batterio Scatena il Caos nella Tua Bocca (e Come Fermarlo!)
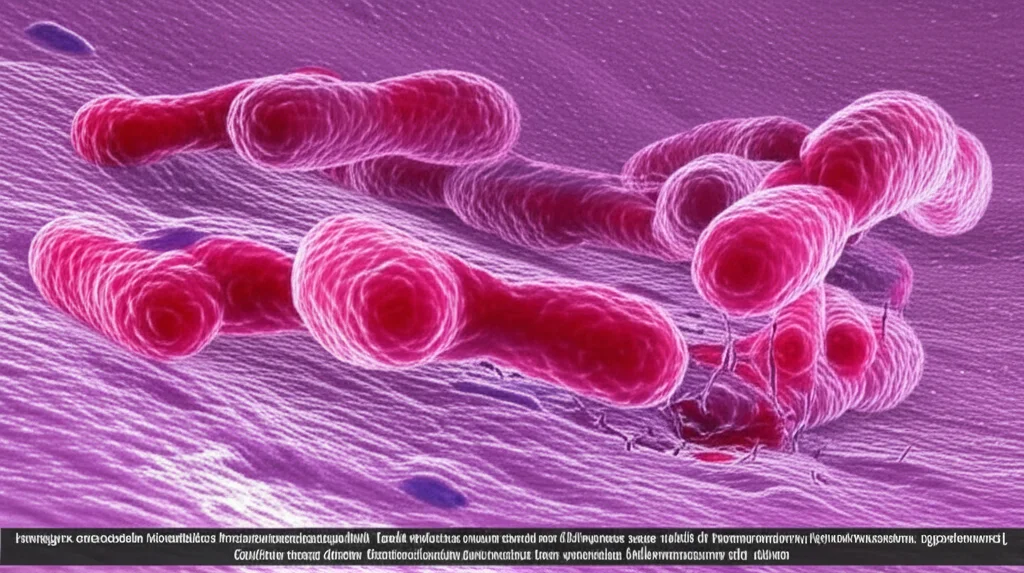
Ciao a tutti! Oggi voglio parlarvi di qualcosa che riguarda molti di noi, anche se spesso non ce ne rendiamo conto finché non è troppo tardi: la parodontite. Non è una semplice gengivite, ma una vera e propria malattia infiammatoria che può portare alla perdita dei denti. E sapete chi è uno dei principali colpevoli? Un batterio dal nome un po’ complicato: Porphyromonas gingivalis. Sembra uscito da un film di fantascienza, vero? Eppure, questo microrganismo anaerobico (cioè che vive senza ossigeno) è un attore chiave nel dramma che si svolge sotto le nostre gengive.
Ma come fa esattamente questo batterio a causare così tanti danni? Beh, la storia è più complessa e affascinante di quanto si possa pensare. Non si limita a “mangiare” i tessuti, ma orchestra una risposta immunitaria distruttiva. Immaginate il nostro sistema immunitario come un esercito. Di solito ci difende, ma a volte, manipolato dal nemico, finisce per danneggiare il nostro stesso territorio.
I Macofagi: Guardiani che Possono Diventare un Problema
Nel nostro esercito immunitario ci sono soldati specializzati chiamati macrofagi. Sono cellule fantastiche: arrivano sul luogo dell’infezione, inglobano i batteri e i detriti cellulari (un processo chiamato fagocitosi) e rilasciano segnali (citochine) per coordinare la difesa. Il problema è che, a volte, la morte di questi stessi macrofagi durante la battaglia può peggiorare le cose. È un paradosso: i nostri difensori, morendo, possono amplificare l’infiammazione e contribuire alla distruzione dei tessuti parodontali e dell’osso alveolare che sostiene i denti. Capire perché e come muoiono questi macrofagi è fondamentale per trovare nuove cure.
PANoptosi: Quando la Morte Cellulare Diventa Esplosiva
Recentemente, noi ricercatori abbiamo iniziato a capire che la morte cellulare non è un evento unico, ma può avvenire in modi diversi: apoptosi (una sorta di suicidio cellulare programmato e “pulito”), piroptosi (una morte infiammatoria esplosiva) e necroptosi (un’altra forma di morte programmata ma più “sporca” e infiammatoria). La cosa ancora più interessante è che nella parodontite, questi processi sembrano avvenire contemporaneamente! Nel 2019 è stato coniato un termine per descrivere questo fenomeno: PANoptosi. È come se la cellula attivasse tutti i suoi programmi di autodistruzione insieme, amplificando enormemente i segnali infiammatori. E indovinate un po’? Sembra proprio che il nostro P. gingivalis sia un maestro nell’indurre questa PANoptosi nei macrofagi.
Il Regista Occulto: La Proteina Zbp1
Ma chi dirige questa orchestra di morte cellulare? Le nostre ricerche ci hanno portato a una proteina specifica: la Z-DNA binding protein 1 (Zbp1). Inizialmente identificata come una proteina indotta dall’interferone e associata ai tumori, Zbp1 agisce come un sensore a monte. Contiene domini che le permettono di legare acidi nucleici (come il DNA) e interagire con altre proteine. È nota per il suo ruolo nelle risposte antivirali, ma studi recenti, inclusi i nostri, l’hanno implicata anche nelle infezioni batteriche e, in particolare, nella parodontite indotta da P. gingivalis. Sembra che Zbp1 sia un interruttore chiave che può attivare la PANoptosi.

Il Meccanismo Svelato: Stress Mitocondriale e DNA Rilasciato
Come fa P. gingivalis ad attivare Zbp1 nei macrofagi? Abbiamo scoperto un meccanismo affascinante. L’infezione da P. gingivalis provoca uno stress notevole ai mitocondri, le “centrali energetiche” delle nostre cellule. Questo stress porta al rilascio del DNA mitocondriale (mtDNA) nel citoplasma, il “corpo” della cellula. Normalmente, il mtDNA dovrebbe rimanere confinato nei mitocondri. Quando fuoriesce, agisce come un segnale di pericolo. Ed è qui che entra in gioco Zbp1: riconosce e si lega a questo mtDNA “fuori posto”. Questo legame scatena una cascata di segnali a valle che portano proprio alla PANoptosi, amplificando la morte cellulare e l’infiammazione. È un meccanismo quasi diabolico: il batterio stressa la cellula, la cellula rilascia un segnale di pericolo interno (mtDNA), e una proteina della cellula stessa (Zbp1) usa quel segnale per autodistruggerla in modo infiammatorio!
Non Solo Stress: Come P. gingivalis Aumenta la Produzione di Zbp1
Ma non finisce qui. P. gingivalis non si limita a far rilasciare mtDNA per attivare Zbp1; stimola anche la cellula a produrre *più* Zbp1. Abbiamo identificato il percorso molecolare coinvolto: inizia con i recettori Toll-like 2 e 4 (Tlr2/4) sulla superficie del macrofago, che riconoscono componenti del batterio. Questo attiva una via di segnalazione intracellulare che coinvolge le proteine JNK e poi i fattori di trascrizione Stat3 e Stat5. Questi ultimi entrano nel nucleo della cellula e “accendono” il gene Zbp1, portando a una maggiore produzione della proteina. Più Zbp1 significa una risposta PANoptotica ancora più forte quando l’mtDNA viene rilasciato. Un doppio colpo micidiale!
La Prova del Nove: Esperimenti su Modelli Animali
Per confermare le nostre ipotesi, abbiamo usato modelli animali, in particolare topi. Abbiamo indotto la parodontite in topi normali usando P. gingivalis e abbiamo osservato, come previsto, un aumento dell’infiammazione, della perdita ossea e della morte cellulare nei macrofagi, insieme a livelli elevati di Zbp1. Ma la prova cruciale è arrivata quando abbiamo fatto lo stesso esperimento su topi geneticamente modificati per non avere la proteina Zbp1 (topi Zbp1 knockout). In questi topi, l’infezione da P. gingivalis causava molti meno danni! La distruzione dei tessuti parodontali era ridotta, c’erano meno segni di PANoptosi nei macrofagi e l’infiammazione era contenuta. Questo ci ha dato una forte conferma che Zbp1 è davvero un mediatore chiave del danno indotto da P. gingivalis.
Alla Ricerca di una Soluzione: Bloccare Zbp1
Se Zbp1 è così importante, bloccarla potrebbe essere una strategia terapeutica? Abbiamo iniziato a cercare composti che potessero farlo. Utilizzando database e simulazioni al computer (docking molecolare), abbiamo identificato un candidato promettente: l’acido salvianolico B (Sal B). È un composto naturale estratto dalla radice di Salvia miltiorrhiza (Danshen), una pianta usata nella medicina tradizionale cinese. Le simulazioni hanno mostrato che Sal B potrebbe legarsi bene a Zbp1, potenzialmente inibendola. Esperimenti in vitro hanno confermato che Sal B riduceva l’espressione di Zbp1 nei macrofagi infettati da P. gingivalis e diminuiva i segni di PANoptosi e infiammazione.
Una Consegna Innovativa: I Microaghi
Ok, abbiamo un potenziale farmaco (Sal B), ma come lo portiamo dove serve, cioè nei tessuti gengivali infiammati, in modo efficace? L’applicazione locale è spesso difficile nel cavo orale. Qui entra in gioco un’altra tecnologia affascinante: i microaghi (MNs). Immaginate un piccolo cerotto con centinaia di aghi minuscoli, quasi invisibili, fatti di un materiale che si dissolve. Questi aghi possono penetrare lo strato superficiale della mucosa orale senza causare dolore significativo e rilasciare il farmaco direttamente nel tessuto. Abbiamo caricato Sal B su questi microaghi fatti di PVA (alcool polivinilico) e acido ialuronico. Test di laboratorio hanno mostrato che gli aghi erano abbastanza robusti da penetrare la mucosa e si dissolvevano rapidamente (in circa 30 secondi), rilasciando efficacemente Sal B.
Test sul Campo (Anzi, in Bocca!): Sal B e Microaghi Contro la Parodontite
Abbiamo quindi testato i nostri microaghi caricati con Sal B (Sal B@MNs) nei topi con parodontite indotta da P. gingivalis. Abbiamo applicato i cerotti quotidianamente sulla mucosa vicino all’area infiammata. I risultati sono stati davvero incoraggianti! Nei topi trattati con Sal B@MNs, abbiamo osservato una significativa riduzione della perdita ossea e della distruzione dei tessuti parodontali rispetto ai topi non trattati o trattati con microaghi vuoti. Inoltre, i livelli di Zbp1 nei tessuti erano più bassi e c’erano meno segni di infiammazione. Abbiamo testato questa tecnologia anche in un modello di guarigione di ferite nel palato dei topi, sempre in presenza di P. gingivalis, e anche lì Sal B@MNs ha migliorato la guarigione e ridotto l’infiammazione e l’espressione di Zbp1.

Cosa Significa Tutto Questo?
Questa ricerca ci apre una nuova finestra sulla comprensione della parodontite. Abbiamo svelato un meccanismo dettagliato attraverso cui Porphyromonas gingivalis, un batterio chiave, manipola le nostre stesse cellule immunitarie (i macrofagi) per causare danno. Lo fa inducendo uno stato di morte cellulare infiammatoria multipla (PANoptosi) orchestrato dalla proteina Zbp1. Zbp1 viene attivata dal DNA mitocondriale rilasciato a causa dello stress indotto dal batterio, e la sua produzione è ulteriormente aumentata da una specifica via di segnalazione (Tlr2/4–JNK–Stat3/5) attivata sempre dal batterio.
La scoperta più entusiasmante è che bloccare Zbp1, sia geneticamente che farmacologicamente con l’acido salvianolico B, può proteggere dalla distruzione dei tessuti parodontali. Inoltre, l’uso dei microaghi si è dimostrato un metodo promettente per veicolare questo tipo di trattamento direttamente dove serve.
Certo, siamo ancora a livello di ricerca preclinica, ma questi risultati sono molto promettenti. Identificare Zbp1 come bersaglio terapeutico e sviluppare strategie come Sal B@MNs potrebbe portare in futuro a nuovi trattamenti più efficaci per combattere la parodontite e forse altre malattie infiammatorie. È un esempio perfetto di come capire i meccanismi molecolari più profondi di una malattia possa aprire la strada a soluzioni innovative. Continueremo a lavorare in questa direzione, sperando di poter presto offrire nuove armi contro questo nemico silenzioso che si nasconde nelle nostre bocche!
Fonte: Springer