MDSC nel Tumore al Polmone: Vi Svelo Come le Isoliamo Meglio!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona molto nel mio campo di ricerca: il microambiente tumorale, o TME (Tumor Microenvironment). Immaginatelo come un ecosistema complesso, quasi una piccola città caotica all’interno del nostro corpo dove le cellule tumorali non sono sole. Anzi, convivono e interagiscono con un sacco di altre cellule: quelle dello stroma, quelle endoteliali e, soprattutto, un’armata eterogenea di cellule del nostro sistema immunitario. Questa interazione è cruciale perché decide le sorti della malattia.
I “Buoni” e i “Cattivi” del Sistema Immunitario nel Tumore
Nel TME ci sono i “buoni”, come le cellule Natural Killer (NK) o i linfociti T CD8+ citotossici, che sono i nostri soldati scelti, pronti a combattere il tumore e a limitarne la crescita. Fantastico, no? Purtroppo, però, il tumore è subdolo. Rilascia un sacco di segnali – chemochine, fattori di crescita, citochine infiammatorie – che mandano in tilt la normale produzione di cellule immunitarie (la mielopoiesi). Questo processo, che potremmo definire “d’emergenza”, porta alla creazione di cellule mieloidi “alternative”, che invece di combattere il tumore, finiscono per aiutarlo. Tra queste, le più note sono i macrofagi associati al tumore (TAM) e, le protagoniste di oggi, le cellule mieloidi soppressorie (MDSC).
Le MDSC sono un gruppo eterogeneo di cellule mieloidi immature che hanno una pessima reputazione: sopprimono la risposta immunitaria all’interno del tumore, favorendone la progressione. Si espandono non solo nel cancro, ma anche in risposta a infezioni, infiammazioni, traumi o malattie autoimmuni.
Identikit delle MDSC: Non è Facile Riconoscerle
Generalmente, le MDSC umane si dividono in due gruppi principali:
- PMN-MDSC (polimorfonucleate): CD33+CD11b+HLA-DRlow/-CD15+CD14-
- M-MDSC (monocitiche): CD33+CD11b+HLA-DRlow/-CD15-CD14+
Il problema è che assomigliano tantissimo ai loro “cugini” pro-infiammatori, rispettivamente i neutrofili e i monociti. Hanno origine, aspetto e marcatori simili, ma biologicamente fanno cose diverse. Distinguerle è una vera sfida! Per le M-MDSC, un marcatore chiave è la bassa o assente espressione di HLA-DR (una molecola MHC di classe II). Per le PMN-MDSC, fino a poco tempo fa, l’unico modo per separarle dai neutrofili era la centrifugazione su gradiente (le PMN-MDSC sono a bassa densità, i neutrofili ad alta). Recentemente, si è scoperto che il recettore LOX-1 (Lectin-type oxidized LDL receptor 1) è espresso specificamente sulle PMN-MDSC, il che aiuta un po’.
Perché Studiare le MDSC *Dentro* il Tumore (tMDSC)?
Un punto fondamentale: le MDSC che circolano nel sangue, quelle nella milza e quelle che si infiltrano nel tumore (le tMDSC, appunto) non sono uguali. Hanno profili genetici, metabolismo e livelli di proteine chiave (come PD-L1, un importante freno immunitario) diversi. Le tMDSC, in particolare, sono delle vere alleate del cancro nel TME:
- Promuovono la formazione di nuovi vasi sanguigni (angiogenesi) tramite l’asse VEGFA/COX2.
- Aiutano le metastasi inducendo un cambiamento nelle cellule tumorali (fenotipo mesenchimale) e preparando il terreno in altri organi (nicchia pre-metastatica).
- Soprattutto, bloccano i nostri linfociti T “buoni” usando varie armi: consumano l’arginina (essenziale per i linfociti T) tramite gli enzimi ARG1 e NOS2; degradano il triptofano tramite IDO1; limitano la disponibilità di cisteina.
Capite bene, quindi, che studiare le tMDSC direttamente dal tumore è cruciale per capire davvero cosa succede nel TME e come contrastarlo.
La Sfida: Isolare le tMDSC dai Tumori Umani
Nonostante il loro ruolo critico, isolare e studiare le tMDSC dai tessuti umani, specialmente da tumori solidi come il carcinoma polmonare non a piccole cellule (NSCLC), è complicato. Esistono kit commerciali per i topi, ma non per i campioni tumorali umani. Finora, ci si è affidati principalmente a due tecniche:
- MACS (Magnetic-Activated Cell Sorting): Usa biglie magnetiche legate ad anticorpi per “pescare” le cellule desiderate (o eliminare quelle indesiderate). È relativamente semplice, ma permette di usare al massimo due marcatori e spesso la purezza non è eccelsa.
- FACS (Fluorescence-Activated Cell Sorting): Permette di separare le cellule in base a molti marcatori fluorescenti. È molto preciso, ma richiede strumentazione costosa, personale specializzato, è lungo e può stressare le cellule, riducendone la vitalità e la funzionalità.
Molti studi che usano queste tecniche, inoltre, non riportano dati sulla purezza delle cellule isolate o usano pannelli di marcatori non completi, rendendo difficile interpretare i risultati. C’era bisogno di qualcosa di meglio.

La Nostra Soluzione Innovativa: Rosette-MACS
Ed è qui che entriamo in gioco noi! Abbiamo messo a punto un nuovo flusso di lavoro, che abbiamo chiamato Rosette-MACS, combinando due tecnologie in modo intelligente per isolare le tMDSC da biopsie di tumore al polmone umano. Questo approccio era già stato usato per le MDSC circolanti nel sangue, ma adattarlo al tessuto tumorale è stata la vera novità.
Ecco come funziona, in parole povere:
- Dissociazione del Tumore: Per prima cosa, dobbiamo ottenere una sospensione di singole cellule dal pezzetto di tumore. Usiamo un kit specifico e un dispositivo meccanico (gentleMACS).
- Il Trucco dei Globuli Rossi: La tecnologia RosetteSep™ (della Stemcell Technologies) è pensata per il sangue intero. Usa anticorpi speciali che legano le cellule “indesiderate” ai globuli rossi (RBC), formando delle “rosette” dense che, dopo centrifugazione su un gradiente di densità, finiscono sul fondo. Le cellule che ci interessano (in questo caso, quelle mieloidi CD33+) rimangono all’interfaccia, belle pulite. Ma nel tessuto tumorale dissociato, i globuli rossi non ci sono! La nostra idea è stata semplice ma efficace: aggiungere globuli rossi freschi autologhi (cioè dello stesso paziente, ottenuti da un prelievo di sangue) alla sospensione cellulare del tumore in un rapporto 1:1. Et voilà, il RosetteSep funziona anche sul tessuto! Questo passaggio elimina gran parte delle cellule non mieloidi (linfociti T, B, NK…).
- Purificazione Finale con MACS: A questo punto, abbiamo una popolazione arricchita di cellule mieloidi (CD33+). Per isolare specificamente le MDSC, dobbiamo eliminare quelle che esprimono HLA-DR (che non sono soppressorie). Usiamo quindi delle biglie magnetiche anti-HLA-DR (tecnologia MACS). Le cellule che *non* si legano alle biglie (HLA-DR negative o basse) sono le nostre tMDSC!
I Risultati: Rosette-MACS Batte FACS e MACS
Abbiamo confrontato il nostro metodo Rosette-MACS con FACS e MACS tradizionali, usando campioni di tumore al polmone umano. I risultati sono stati incredibili:
- Resa (Yield): Con Rosette-MACS abbiamo recuperato un numero enormemente maggiore di tMDSC (circa 18 milioni di cellule in media, corrispondenti al 40% delle cellule iniziali!) rispetto a FACS (meno di 100.000 cellule, <1%) e MACS (circa 350.000 cellule, <1%).
- Purezza: La purezza delle tMDSC isolate con Rosette-MACS è stata quasi dell’80% (cellule CD33+CD11b+HLA-DRlow/-). Con FACS abbiamo ottenuto meno del 15% e con MACS addirittura solo lo 0.39%!
- Vitalità: Le cellule isolate con Rosette-MACS erano molto vitali (circa 89%), mentre con MACS la vitalità era inferiore al 50%. La vitalità post-FACS è notoriamente un problema a causa dello stress della procedura.
- Tempo: Rosette-MACS richiede circa 200 minuti in totale (inclusa la processazione del tumore), un po’ più di MACS (170 min) ma meno di FACS (240 min, senza contare la preparazione).
Non Solo Purezza: Le Cellule Isolate Sono Funzionali!
Ok, abbiamo tante cellule e sono pure, ma… funzionano come dovrebbero? Sono davvero immunosoppressive? Questa è una domanda cruciale, spesso trascurata. Abbiamo verificato!
1. Espressione Genica: Abbiamo analizzato l’espressione di geni chiave associati alla funzione soppressoria delle MDSC. Rispetto alle cellule immunitarie del sangue di donatori sani (PBMC), le tMDSC isolate con Rosette-MACS mostravano livelli significativamente più alti di:
- ARG1 (94 volte di più!)
- IDO1 (22 volte di più!)
- PD-L1 (22 volte di più!)
- NOS2 (38 volte di più!)
- Altri geni importanti come COX2, VEGFA, S100A8, S100A9, LOX1.
Questo conferma che mantengono il loro “programma” immunosoppressivo.
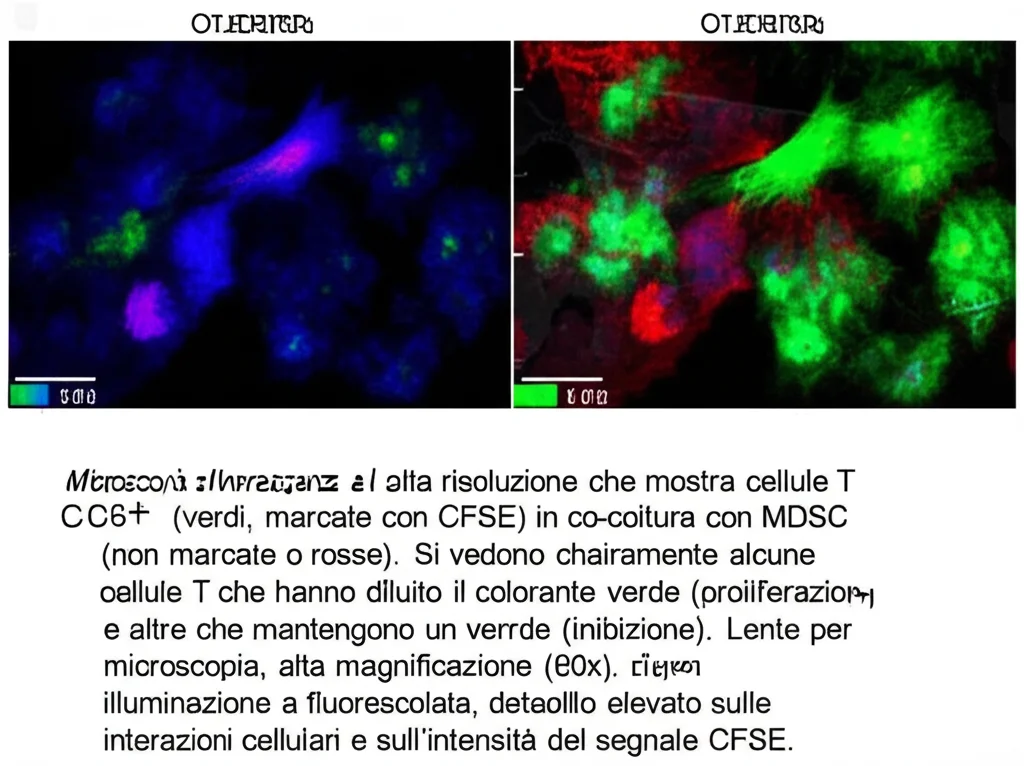
2. Test di Soppressione: Abbiamo messo le tMDSC isolate a contatto con linfociti T CD8+ (i nostri “soldati buoni”) attivati in laboratorio. Abbiamo misurato quanto i linfociti T riuscivano a proliferare (moltiplicarsi). Risultato: i linfociti T coltivati da soli proliferavano molto (57%), ma quando erano insieme alle tMDSC (in rapporto 1:2), la loro proliferazione era significativamente inibita (solo 35%). Bingo! Le cellule isolate con Rosette-MACS sono attivamente immunosoppressive.
Perché Questo Metodo è Importante?
Come dicevo prima, studiare le tMDSC è fondamentale perché si comportano diversamente dalle MDSC circolanti. Queste ultime sono più “plastiche”, possono trasformarsi in altri tipi di cellule. Le tMDSC, invece, sono più “impegnate” nel loro ruolo soppressivo all’interno del TME. Capire le loro specifiche proprietà è essenziale per sviluppare nuove immunoterapie che mirino proprio a bloccare la loro azione nefasta nel microambiente tumorale. Usare solo le MDSC del sangue potrebbe darci informazioni fuorvianti.
Il nostro metodo Rosette-MACS offre una piattaforma robusta per ottenere tMDSC umane funzionali con alta resa e purezza, superando molti limiti delle tecniche attuali. Questo apre la strada a studi più dettagliati sui meccanismi molecolari dell’immunosoppressione mediata dalle tMDSC e, speriamo, all’identificazione di nuovi bersagli terapeutici.
Qualche Limitazione (Siamo Onesti)
Nessun metodo è perfetto, e anche il nostro ha dei limiti:
- La quantità di tMDSC recuperate può variare tra pazienti, perché l’infiltrazione immunitaria nei tumori polmonari è eterogenea.
- Richiede globuli rossi freschi autologhi, il che potrebbe essere un problema in alcuni casi (difficoltà nel prelievo, disidratazione, disturbi della coagulazione). Abbiamo provato alternative (conservare il sangue, usare i globuli rossi recuperati dal RosetteSep stesso), ma non hanno funzionato bene.
- Il kit RosetteSep arricchisce solo cellule mieloidi (CD33+). Se si volessero studiare anche i linfociti dello stesso tumore, FACS o MACS potrebbero essere più versatili (anche se meno efficienti per le tMDSC).
- La conservazione del campione tumorale fresco è critica per tutti i metodi.
In Conclusione
Nonostante i limiti, crediamo fermamente che la combinazione Rosette-MACS rappresenti un passo avanti significativo per l’isolamento e lo studio delle tMDSC dal tumore al polmone umano. Ci fornisce un modello sperimentale più affidabile per mimare ciò che accade nel TME e per cercare nuove strategie terapeutiche contro il cancro al polmone, una sfida ancora enorme. È un piccolo tassello, ma speriamo importante, nella lotta contro questa malattia!
Fonte: Springer