Stop alle Metastasi? Scoperta Z1362873773, una Nuova Speranza Contro il Cancro al Colon
Ciao a tutti! Oggi voglio parlarvi di una scoperta che ci riempie di entusiasmo e che potrebbe aprire nuove strade nella lotta contro una delle malattie più temute: il cancro, in particolare quello al colon-retto. Come sapete, una delle sfide più grandi nel trattamento dei tumori non è tanto la massa tumorale primaria, quanto la sua capacità di diffondersi in altre parti del corpo, un processo chiamato metastasi. È proprio la metastasi la principale causa di morte legata al cancro a livello globale.
Il Nemico Invisibile: la Metastasi e il Ruolo della Fascina
Ma come fanno le cellule tumorali a “viaggiare” nel corpo? Immaginatele come piccole esploratrici maligne che devono muoversi e invadere nuovi territori. Per farlo, hanno bisogno di riorganizzare il loro “scheletro” interno, l’actina, creando delle specie di tentacoli o piedini (chiamati filopodi, lamellipodi, invadopodi) che le aiutano a spostarsi. Qui entra in gioco una proteina chiave: la fascina.
La fascina agisce come un “organizzatore” di questi filamenti di actina, raggruppandoli in fasci rigidi e compatti che formano proprio quelle strutture necessarie alla cellula tumorale per muoversi. La cosa interessante è che, mentre nei tessuti sani la fascina è poco presente o assente, in molti tipi di cancro, compreso quello del colon-retto (specialmente in forme aggressive come l’adenocarcinoma serrato), i suoi livelli sono notevolmente aumentati. Questa abbondanza di fascina è direttamente collegata a una maggiore crescita del tumore, invasività e, appunto, metastasi. Per questo motivo, la fascina è diventata un bersaglio terapeutico molto promettente e un indicatore di aggressività del cancro.
Negli anni, sono stati identificati alcuni inibitori della fascina, come la Migrastatina e i suoi derivati, o molecole come la G2. Questi composti hanno mostrato potenziale nel bloccare il movimento delle cellule tumorali. Tuttavia, la loro sintesi è spesso complessa e costosa, e lo spazio chimico esplorato finora è relativamente limitato. Pensate che persino alcuni farmaci già approvati per altri usi (come l’imipramina e il raltegravir) si sono rivelati inibitori della fascina, ma riutilizzare farmaci esistenti, sebbene utile, copre solo una piccola parte delle infinite possibilità molecolari là fuori e presenta difficoltà brevettuali.
Caccia al Tesoro Molecolare: Come Abbiamo Trovato Z1362873773
Ecco perché abbiamo deciso di intraprendere una vera e propria “caccia al tesoro” molecolare su larga scala. Ci siamo rivolti a una libreria chimica vastissima, la Enamine HTS, che contiene quasi 1,4 milioni di composti diversi! Un universo di molecole da esplorare.
Come abbiamo fatto a cercare un ago in un pagliaio così grande? Abbiamo usato un approccio in silico, cioè al computer, chiamato “screening virtuale basato sul ligando”. In pratica, abbiamo preso un inibitore noto ed efficace della fascina, la molecola G2, e ne abbiamo creato un modello farmacoforico. Un farmacoforo è come l’impronta digitale chimica essenziale di una molecola, definendo le caratteristiche chiave necessarie per interagire con il suo bersaglio (la fascina, in questo caso).
Armati di questo modello, abbiamo usato un software sviluppato dal nostro gruppo di ricerca (Metascreener) per confrontarlo con tutte le 1,4 milioni di molecole della libreria Enamine. Cercavamo composti che avessero un’impronta chimica molto, molto simile a quella di G2. Abbiamo impostato un filtro molto stretto: solo le molecole con una somiglianza farmacoforica superiore al 97% rispetto al modello G2 sono state prese in considerazione. Da questo screening massivo sono emersi 50 candidati promettenti. Di questi, ne abbiamo selezionati 12 che erano effettivamente disponibili per essere acquistati e testati in laboratorio.
Dalla Teoria alla Provetta: Le Prove di Laboratorio
Avere una lista di candidati dal computer è un ottimo punto di partenza, ma la vera prova del nove avviene in laboratorio. Dovevamo verificare se queste molecole selezionate fossero davvero in grado di legarsi alla fascina e di bloccarne la funzione.
Abbiamo usato due test principali:
- Differential Scanning Fluorimetry (DSF): Questo test misura se un composto si lega a una proteina osservando come cambia la sua temperatura di denaturazione (cioè la temperatura alla quale la proteina si “srotola”). Un cambiamento significativo indica un’interazione.
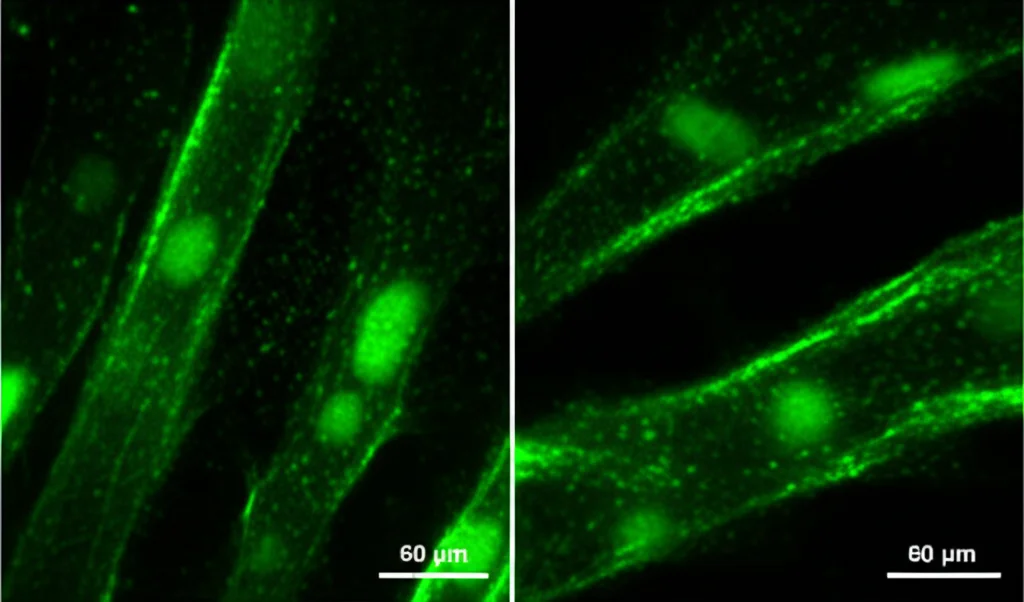
- F-actin Bundling Assay: Questo è il test funzionale chiave. Abbiamo ricreato in provetta il processo di formazione dei fasci di actina mediato dalla fascina e abbiamo aggiunto i nostri composti candidati. Se un composto inibisce la fascina, i filamenti di actina rimangono disorganizzati e non formano i fasci compatti. Abbiamo visualizzato il tutto usando un colorante fluorescente (falloidina legata ad Alexa Fluor 488) che si lega all’actina, permettendoci di vedere i fasci al microscopio.
Tra i 12 composti testati, uno in particolare ha brillato: Z1362873773. Questo composto non solo ha mostrato segni di legame con la fascina nel test DSF, ma ha anche dimostrato una chiara capacità di inibire la formazione dei fasci di F-actina nel secondo test, confermando la sua attività inibitoria sulla funzione della fascina. Le immagini al microscopio erano eloquenti: dove c’era Z1362873773, i fasci di actina non si formavano, proprio come succedeva con un inibitore noto usato come controllo positivo.
Sotto la Lente: Gli Effetti sulle Cellule Tumorali e sugli Organoidi
Avere una molecola che funziona in provetta è fantastico, ma funzionerà anche sulle cellule tumorali vere e proprie? Per scoprirlo, abbiamo testato Z1362873773 su due linee cellulari di adenocarcinoma colorettale umano: DLD-1 e HCT-116.
Prima abbiamo verificato la sua tossicità per determinare le concentrazioni giuste da usare. Poi, abbiamo condotto un “wound-healing assay” (saggio di guarigione della ferita). In pratica, si crea un “graffio” in uno strato di cellule tumorali coltivate in piastra e si osserva quanto velocemente le cellule riescono a “chiudere” il graffio migrando. I risultati sono stati molto incoraggianti: Z1362873773 ha ridotto significativamente la capacità di migrazione di entrambe le linee cellulari, con un effetto paragonabile a quello dell’inibitore G2 alla stessa concentrazione.
Ma volevamo andare oltre le semplici linee cellulari, che sono modelli semplificati. Abbiamo quindi testato Z1362873773 su organoidi tumorali derivati da pazienti con cancro al colon-retto. Gli organoidi sono come mini-tumori coltivati in laboratorio che mantengono molte delle caratteristiche del tumore originale del paziente, rappresentando un modello preclinico molto più realistico. Anche in questo caso, Z1362873773 ha mostrato un effetto citotossico significativo sugli organoidi, addirittura 2-3 volte superiore a quello di G2 in questo modello ex vivo. Questo suggerisce che Z1362873773 potrebbe essere particolarmente efficace in un contesto più vicino a quello reale del paziente.
Viaggio nel Mondo Molecolare: Come Funziona l’Inibitore?
Per capire meglio come Z1362873773 interagisce con la fascina a livello atomico, siamo tornati al computer, usando tecniche di modellazione molecolare come il docking e le simulazioni di dinamica molecolare (MD).
Il docking è come cercare di capire come una chiave (la nostra molecola Z1362873773) si inserisce in una serratura (la proteina fascina). Abbiamo usato due strutture cristallografiche della fascina (una libera e una legata a un analogo di G2, PDB: 6B0T) e diversi software (AutoDock Vina, Lead Finder) per predire il sito di legame più probabile e la “posa” di Z1362873773. I risultati hanno indicato con forza che Z1362873773 si lega preferenzialmente a un sito specifico sulla fascina, noto come sito di legame dell’actina 2, lo stesso sito dove si legano altri inibitori noti come G2 e i suoi derivati. Abbiamo anche identificato i residui amminoacidici chiave della fascina coinvolti nell’interazione (come Phe14, Ile93, Trp101, Phe216, Arg217), confermando ulteriormente la plausibilità del legame.

Le simulazioni di dinamica molecolare (MD) ci hanno permesso di fare un passo in più: abbiamo simulato il comportamento del complesso fascina-Z1362873773 per un periodo di tempo (100 nanosecondi) in un ambiente acquoso, tenendo conto della flessibilità della proteina. Queste simulazioni hanno confermato che il legame è stabile nel tempo e che Z1362873773 rimane saldamente ancorato al sito di legame dell’actina 2. L’analisi energetica (MMPBSA) ha indicato un legame forte, dominato da interazioni di van der Waals, e ha ulteriormente rafforzato la nostra fiducia nel meccanismo d’azione proposto.
Sarà un Farmaco? Potenzialità e Vantaggi di Z1362873773
Una molecola può essere efficace in laboratorio, ma per diventare un farmaco deve avere anche le giuste proprietà farmacocinetiche: deve poter essere assorbita, distribuirsi correttamente nel corpo, non essere metabolizzata troppo in fretta e non essere tossica (proprietà ADMET). Abbiamo usato software predittivi (QikProp, ALOGPS) per valutare queste caratteristiche per Z1362873773 e le abbiamo confrontate con quelle di inibitori noti.
I risultati sono stati molto promettenti:
- Assorbimento e Solubilità: Z1362873773 sembra avere una buona solubilità acquosa (logPAQS = -5.831, logS = -4.08) e un’ottima predizione di assorbimento orale (100%). Potrebbe anche essere assorbibile attraverso la pelle (log Kp = -2.157).
- Distribuzione: Il legame previsto con le proteine plasmatiche (log Khsa = 0.656) è debole, il che significa che una buona parte della molecola rimarrebbe libera e attiva nel sangue. Inoltre, la predizione suggerisce che Z1362873773 abbia una bassa probabilità di attraversare la barriera emato-encefalica (log BR/BL = -0.481), un aspetto positivo dato che il suo bersaglio non è nel cervello.
- Metabolismo: Il numero previsto di metaboliti primari è basso (4), suggerendo una buona stabilità metabolica.
- Regole “Drug-like”: Z1362873773 rispetta le principali regole empiriche (come le regole di Lipinski e Jorgensen) che indicano se una molecola ha caratteristiche simili a quelle di un farmaco.
- Tossicità Potenziale: Le analisi predittive non hanno identificato interazioni con bersagli noti per causare tossicità significativa. In particolare, il valore previsto per l’interazione con il canale HERG K+ (associato ad aritmie cardiache) è favorevole, suggerendo un minor rischio cardiaco rispetto ad altri composti.
In generale, le proprietà ADMET previste per Z1362873773 sono risultate migliori o paragonabili a quelle di inibitori della fascina già noti e testati, alcuni dei quali usati come farmaci.
Un altro vantaggio non trascurabile riguarda la sintesi chimica. Abbiamo confrontato il processo di produzione di Z1362873773 con quello di G2. La sintesi di Z1362873773 richiede un solo passaggio, utilizza reagenti meno problematici e quantità inferiori di materiale di partenza rispetto ai due passaggi e ai reagenti più complessi (e talvolta tossici) necessari per G2. Questo potrebbe tradursi in una produzione più semplice, veloce ed economica.
Un Passo Avanti nella Lotta al Cancro
In sintesi, attraverso un’ampia esplorazione di una libreria chimica vastissima e un rigoroso processo di validazione sperimentale e computazionale, abbiamo identificato una nuova molecola, Z1362873773, che agisce come un potente inibitore della proteina fascina. Questa molecola ha dimostrato di poter bloccare la funzione della fascina, ridurre la migrazione e la vitalità delle cellule di cancro al colon-retto in vitro e mostrare effetti promettenti su organoidi derivati da pazienti.

La cosa entusiasmante è che Z1362873773 ha una struttura chimica unica, diversa dagli inibitori precedenti, e presenta proprietà farmacocinetiche predicted favorevoli e un percorso di sintesi potenzialmente più vantaggioso. Questo non solo ci fornisce un nuovo candidato promettente per lo sviluppo di terapie anti-metastatiche contro il cancro al colon-retto (e potenzialmente altri tumori dove la fascina è iperespressa), ma convalida anche il nostro approccio di screening su larga scala come metodo efficace per scoprire nuovi agenti terapeutici.
Naturalmente, siamo solo all’inizio. Serviranno ulteriori studi preclinici per ottimizzare questa molecola e valutarne appieno sicurezza ed efficacia prima di poter pensare a test clinici sull’uomo. Ma la scoperta di Z1362873773 rappresenta un passo avanti significativo e ci dà una nuova speranza nella difficile battaglia contro la diffusione del cancro. Il nostro lavoro dimostra che esplorare territori chimici inesplorati può portare a scoperte inaspettate e preziose. Continueremo su questa strada!
Fonte: Springer






