CLN2: Una Nuova Speranza nel Petto! Addio Infusioni Difficili al Cuoio Capelluto?
Ciao a tutti! Oggi voglio parlarvi di qualcosa di veramente innovativo nel campo delle malattie rare, un argomento che mi sta particolarmente a cuore. Immaginate una malattia genetica rara e devastante, la Lipofuscinosi Ceroide Neuronale di tipo 2 (CLN2), che colpisce i bambini portando a crisi epilettiche, perdita della vista, declino cognitivo e, purtroppo, a una morte prematura. È causata dalla mancanza di un enzima chiamato tripeptidil peptidasi 1 (TPP1).
Una Luce Chiamata Cerliponase Alfa
Fortunatamente, da qualche anno esiste una terapia enzimatica sostitutiva approvata, la cerliponase alfa (nome commerciale Brineura), che può rallentare la progressione della malattia. È un farmaco incredibile, il primo del suo genere somministrato direttamente nel cervello, più precisamente nei ventricoli cerebrali, attraverso un’infusione prolungata. Questa somministrazione avviene tramite un dispositivo impiantato chirurgicamente: un catetere nel ventricolo collegato a un piccolo serbatoio sottocutaneo, di solito posizionato sotto il cuoio capelluto.
Le Sfide del Trattamento Tradizionale
Qui iniziano le difficoltà. Questa terapia salva-vita deve essere somministrata ogni due settimane, per tutta la vita del paziente. Ogni infusione dura circa 4 ore e mezza. Provate a immaginare cosa significhi per un bambino piccolo, magari con crisi epilettiche, rimanere fermo per ore mentre un ago è inserito nel cuoio capelluto. Mantenere la sterilità in queste condizioni è una vera sfida. Inoltre, il serbatoio sotto il cuoio capelluto si usura dopo circa 105 punture (più o meno 4 anni di terapia), rendendo necessaria la sua sostituzione chirurgica. Aggiungiamoci il rischio di infezioni, gonfiori, perdite o ostruzioni del catetere… insomma, un percorso a ostacoli per i pazienti e le loro famiglie.
L’Idea Rivoluzionaria: Dal Cuoio Capelluto al Torace
Ed è qui che entra in gioco un’idea geniale, descritta per la prima volta nel 2020 da uno degli autori dello studio che vi racconto oggi, W. Bruce Cherny. E se, invece di collegare il catetere ventricolare al serbatoio sotto il cuoio capelluto, lo collegassimo a un dispositivo di accesso venoso centrale (CVAD), un tipo di “port” simile a quelli usati per altre terapie, impiantato però sottocute nella parte anteriore del torace? Questa tecnica combina due procedure ben note ai neurochirurghi: l’impianto del catetere (come per gli shunt ventricolo-peritoneali) e la creazione di una tasca sottocutanea (come per le batterie degli stimolatori del nervo vago). Ma stavolta, nella tasca ci mettiamo un port per l’infusione cerebrale!
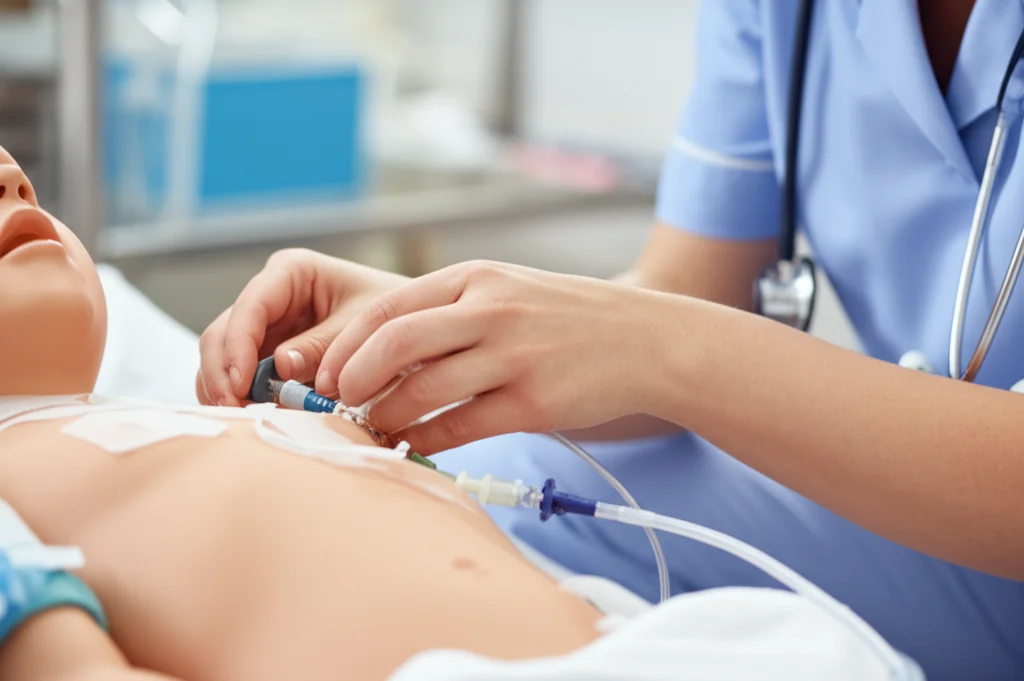
La Nostra Esperienza: Sette Storie di Successo
Nel nostro studio, abbiamo seguito sette pazienti, con età dai 2 ai 24 anni, che tra marzo 2019 e aprile 2024 hanno ricevuto questo sistema modificato o hanno convertito il loro vecchio dispositivo. E i risultati? Eccezionali! Nessuno di loro ha avuto problemi significativi di accesso, infezioni o necessità di revisione chirurgica da quando il nuovo sistema è stato impiantato.
Lasciate che vi racconti brevemente alcune storie:
- Paziente 1: Un ragazzo di 11 anni, diagnosticato a 2 anni. Dopo anni di difficoltà con il sistema tradizionale (accessi multipli, perdite), nel 2019 ha ricevuto il nuovo sistema con port toracico. Da allora, il suo dispositivo è stato usato più di 162 volte senza alcun problema. Abbiamo persino una foto del suo vecchio serbatoio danneggiato… fa impressione vedere l’usura causata dai ripetuti tentativi di accesso!
- Paziente 2: Una bambina di 8 anni, diagnosticata a 4. Ha ricevuto il port toracico nel 2020 e da allora è stato usato più di 100 volte senza complicazioni.
- Pazienti 3 e 4: Due fratelli, un maschio di 24 anni e una femmina di 19, entrambi con una forma atipica di CLN2. Avevano avuto difficoltà e persino un’infezione con il sistema tradizionale. Hanno scelto di passare al port toracico nel 2020 per la maggiore facilità d’uso. I loro port sono stati usati rispettivamente 140 e 110 volte, senza problemi.
- Pazienti 5, 6 e 7: Altri tre giovani pazienti (7, 3 e 5 anni) hanno ricevuto il sistema con port toracico più recentemente (fine 2023 e inizio 2024). Anche per loro, nessun problema di accesso o complicazioni finora, con decine di accessi già effettuati.
Come Funziona l’Intervento?
L’intervento viene eseguito in anestesia generale. Utilizzando la navigazione chirurgica intraoperatoria per la massima precisione, si inserisce un catetere ventricolare (impregnato di antibiotico) nel ventricolo laterale del cervello. Questo viene collegato a un piccolo serbatoio (tipo Rickham) sotto il cuoio capelluto, che serve più come punto di connessione intermedio. Poi, si crea una tasca sottocutanea nel torace e, tramite un tunnel sottocutaneo (simile a quello per gli shunt), si fa passare un secondo catetere (anch’esso impregnato di antibiotico) dal cuoio capelluto alla tasca toracica. Qui, il catetere viene collegato al port CVAD (noi abbiamo usato un PowerPort™ Slim, piccolo e leggero). Il port viene fissato saldamente e orientato per un facile accesso. Prima di chiudere, testiamo il sistema per assicurarci che funzioni e misuriamo il volume interno (di solito circa 1.5 mL, un po’ più del sistema tradizionale).
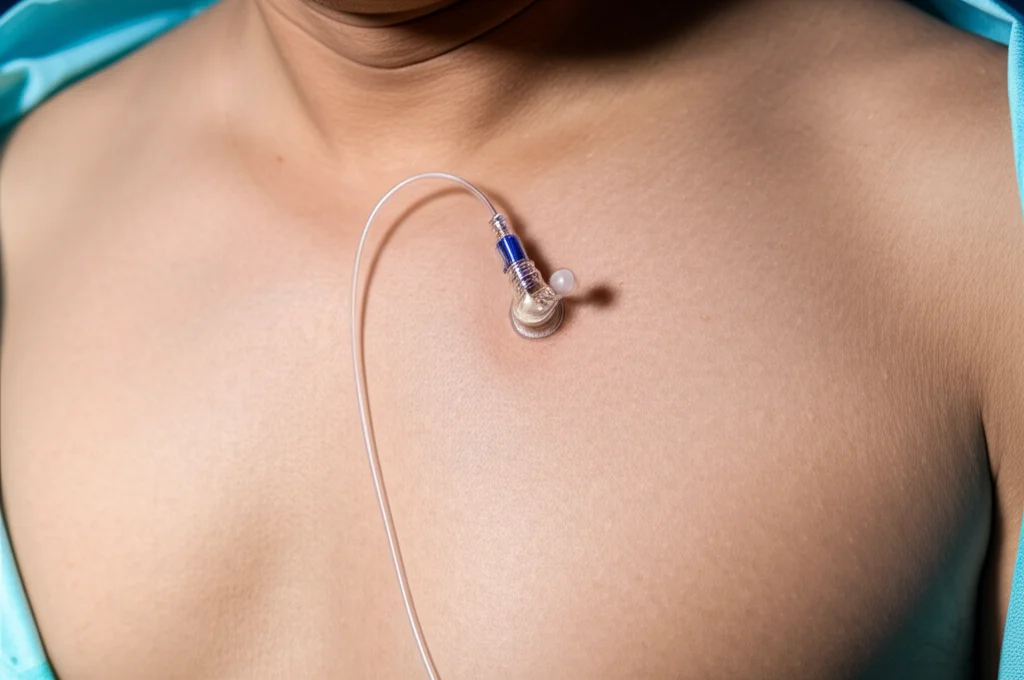
Perché Questo Approccio è Migliore?
I vantaggi sembrano davvero tanti. Pensateci:
- Accesso più facile e stabile: Stabilizzare un ago nel cuoio capelluto di un bambino per ore è complicato. Un port nel torace è intrinsecamente più stabile, più profondo, e può essere fissato meglio con cerotti trasparenti standard, permettendo anche una migliore visualizzazione dell’ago.
- Maggiore mobilità per il paziente: Durante l’infusione, il paziente ha potenzialmente più libertà di movimento.
- Migliore tollerabilità: La nostra esperienza suggerisce che i pazienti tollerano molto meglio questo sistema.
- Potenziale riduzione delle complicazioni: La struttura robusta del port toracico e la maggiore facilità nel mantenere la sterilità potrebbero ridurre il rischio di danni al dispositivo e di infezioni, che sono un problema serio con i sistemi tradizionali (alcuni studi riportano tassi di revisione fino al 50%!).
- Meno rischi chirurgici a lungo termine: Evitare revisioni chirurgiche significa anche evitare ulteriori anestesie generali, che comportano rischi maggiori in questi pazienti.
Ci Sono Svantaggi?
Ovviamente, dobbiamo essere onesti. Ci sono alcune considerazioni:
- Costo: Il port CVAD potrebbe costare leggermente di più di un serbatoio tradizionale.
- Curva di apprendimento: Gli operatori sanitari abituati ai serbatoi VAD potrebbero aver bisogno di familiarizzare con l’accesso ai port toracici.
- “Spazio morto”: Il tubo più lungo richiede una piccola modifica nella procedura di infusione. Noi rimuoviamo un po’ più di liquido cerebrospinale (circa 11.5 mL invece di 10 mL) e, dopo l’infusione del farmaco (10 mL), facciamo un “lavaggio” con 2 mL di soluzione salina sterile per assicurarci che tutto il farmaco raggiunga il cervello.
- Uso “off-label”: Attualmente, l’uso di un CVAD per l’infusione intraventricolare è considerato “off-label”, cioè non è l’indicazione primaria per cui il dispositivo è stato approvato.
- Necessità di dati a lungo termine: Anche se i nostri risultati iniziali sono molto promettenti (alcuni pazienti non hanno avuto problemi per oltre 1900 giorni!), servono più dati e follow-up più lunghi per confermare definitivamente la superiorità di questo metodo.
Un Futuro Più Sereno per i Pazienti CLN2?
In conclusione, questo approccio modificato che collega il catetere ventricolare a un port nel torace sembra offrire una soluzione più sicura, più tollerabile e potenzialmente più duratura per la somministrazione della cerliponase alfa nei pazienti con malattia CLN2. Rappresenta un passo avanti significativo per migliorare la qualità di vita di questi bambini e delle loro famiglie, riducendo il peso delle infusioni frequenti e prolungate e il rischio di complicazioni. È una testimonianza di come l’innovazione chirurgica possa fare una differenza enorme nella gestione di malattie complesse. Speriamo che ulteriori studi confermino questi risultati entusiasmanti!
Fonte: Springer







