Allergie Misteriose? Abbiamo Trovato una Chiave: Ecco il Super Antagonista per i Mastociti!
Ciao a tutti! Oggi voglio raccontarvi una storia affascinante che arriva direttamente dai nostri laboratori, una di quelle scoperte che ti fanno battere il cuore perché aprono strade completamente nuove nella lotta a malattie fastidiose e a volte debilitanti come allergie e infiammazioni croniche. Parliamo di mastociti, recettori misteriosi e di una molecola che potrebbe davvero fare la differenza.
Il Problema: Allergie e Infiammazioni Senza Trequa
Viviamo in un mondo dove le allergie sono sempre più diffuse. Si stima che il 30-40% della popolazione mondiale soffra di qualche forma di allergia: rinite, asma, dermatite atopica, allergie alimentari… un vero flagello! I sintomi vanno dal fastidioso prurito e starnuti fino a reazioni gravi che possono mettere a rischio la vita. Per non parlare delle malattie infiammatorie croniche. Le terapie attuali aiutano, certo, ma spesso non sono risolutive e c’è un bisogno disperato di nuove soluzioni.
Al centro di molte di queste reazioni ci sono i mastociti. Immaginateveli come sentinelle del nostro sistema immunitario, posizionate strategicamente nella pelle e nelle mucose. Quando vengono attivati, rilasciano una cascata di mediatori infiammatori, tra cui la ben nota istamina, scatenando i sintomi allergici. Tradizionalmente, pensiamo alle allergie come mediate dagli anticorpi IgE, ma c’è tutto un mondo di reazioni di ipersensibilità che non dipendono dalle IgE, definite “pseudo-allergiche” o, più recentemente, di tipo VII, causate da un’attivazione diretta dei mastociti.
Alla Scoperta di un Nuovo Bersaglio: MRGPRX2
Ed è qui che entra in gioco il protagonista della nostra storia: un recettore chiamato MRGPRX2 (MAS-related G protein-coupled receptor-X2). Si tratta di un recettore “orfano”, il che significa che all’inizio non si conosceva il suo attivatore naturale (ligando endogeno). Si trova proprio sui mastociti (ma anche su basofili ed eosinofili) ed è particolarmente espresso nei mastociti della pelle.
La cosa incredibile è che MRGPRX2 può essere attivato da un sacco di molecole diverse: peptidi prodotti dal nostro stesso corpo (come cortistatina-14, PAMP-12, LL-37, beta-defensine, e recentemente anche la chemochina CXCL14), ma anche da molti farmaci comuni! Questo spiega perché alcuni farmaci possono causare reazioni allergiche dirette, indipendenti dalle IgE. L’attivazione di MRGPRX2 porta alla degranulazione dei mastociti, cioè al rilascio di quei mediatori infiammatori di cui parlavamo prima.
Questo recettore è stato collegato a un bel po’ di patologie:
- Asma
- Rinite allergica
- Anafilassi
- Orticaria cronica
- Dermatite atopica
- Parodontite cronica
- Fibrosi polmonare idiopatica
- Altre malattie infiammatorie
Capite bene che trovare un modo per bloccare MRGPRX2 potrebbe essere rivoluzionario per trattare tutte queste condizioni.
La Sfida: Trovare un Antagonista Efficace
Se da un lato conosciamo tantissimi agonisti di MRGPRX2 (le molecole che lo attivano), dall’altro gli antagonisti (le molecole che lo bloccano) sono pochissimi e, fino ad ora, non particolarmente brillanti. La maggior parte ha una potenza modesta e manca di selettività, rischiando di interferire con altri processi biologici. Inoltre, non esistevano antagonisti noti capaci di bloccare anche il presunto “cugino” funzionale di MRGPRX2 nel topo, chiamato MRGPRB2, fondamentale per poter testare l’efficacia nei modelli animali preclinici.
Qui è iniziata la nostra avventura. Abbiamo messo in campo un approccio multidisciplinare, unendo chimica, biologia e scienza computazionale. L’obiettivo? Sviluppare un antagonista di MRGPRX2 piccolo, potente, selettivo, stabile e con buone proprietà farmacologiche.
Dallo Screening alla Super Molecola: Nasce PSB-172656
Siamo partiti da uno screening di “frammenti”, molecole molto piccole, e composti “drug-like” (simili a farmaci) dalla nostra collezione interna. Abbiamo usato un saggio biologico ingegnoso basato sul reclutamento di una proteina chiamata β-arrestina, che si lega al recettore quando viene attivato. Se un composto blocca il recettore, il segnale luminoso prodotto dal saggio diminuisce.
E voilà! Abbiamo trovato un “hit”, una molecola promettente: un composto eterotriciclico chiamato 1 (2-metil-3-propilbenzo[4,5]imidazo[1,2-a]pirimidin-4(1H)-one). Era un frammento piccolo (peso molecolare 241 g/mol), con una struttura chimica modificabile e già mostrava una certa potenza (nell’ordine dei micromoli) e selettività per MRGPRX2 rispetto agli altri membri della famiglia MRGPRX (X1, X3, X4).
Da lì è partita la fase di ottimizzazione. Immaginate un lavoro certosino, quasi da sarti molecolari. Abbiamo modificato sistematicamente le tre parti (anelli) della molecola 1, sintetizzando decine di nuovi composti e testandoli uno per uno, principalmente con un saggio che misura la mobilizzazione del calcio (Ca2+) all’interno delle cellule, un altro segnale chiave attivato da MRGPRX2 tramite le proteine Gq.
È stato un processo iterativo, guidato dalle relazioni struttura-attività (SAR): “Se cambio questo pezzetto, la potenza aumenta o diminuisce? E la selettività?”. Abbiamo scoperto, ad esempio, che un gruppo isopropile in posizione 2 e un gruppo etile in posizione 3 erano ottimali per la potenza. Abbiamo visto che mantenere un atomo di idrogeno (N1-H) era cruciale, probabilmente per formare un legame idrogeno essenziale con il recettore.
Il vero salto di qualità è arrivato introducendo due atomi di fluoro in posizioni specifiche (7 e 8) sull’anello benzenico. Questo ha portato alla nascita di PSB-172656 (composto 24: 3-etil-7,8-difluoro-2-isopropilbenzo[4,5]imidazo[1,2-a]pirimidin-4(1H)-one). Questa molecola ha mostrato una potenza subnanomolare (Ki = 0.142 nM nel saggio Ca2+), cioè è attiva a concentrazioni bassissime, quasi 2000 volte più potente del nostro hit iniziale! Un risultato pazzesco!

PSB-172656: Un Profilo da Campione
Ma la potenza non è tutto. Abbiamo caratterizzato a fondo PSB-172656:
- Selettività Altissima: Blocca MRGPRX2 ma ignora completamente gli altri recettori MRGPRX (X1, X3, X4), anche a concentrazioni 1000 volte superiori.
- Blocco Versatile: È efficace contro l’attivazione indotta da tantissimi agonisti diversi, sia peptidi (CST-14, Sostanza P – SP) che piccole molecole (come (R)-ZINC-3573 e clomipramina) e persino polimeri (Composto 48/80 – C48/80).
- Meccanismo Competitivo: I nostri studi suggeriscono che PSB-172656 competa con gli agonisti per lo stesso sito di legame sul recettore. Lo abbiamo confermato con esperimenti specifici (analisi di Schild).
- Blocco dei Segnali Intracellulari: Inibisce non solo il reclutamento della β-arrestina, ma anche l’attivazione delle principali vie di segnalazione a valle di MRGPRX2, mediate dalle proteine Gαq (che mobilizzano il calcio) e Gαi1 (che inibiscono l’adenilato ciclasi).
- Stabilità Metabolica: Ha mostrato una buona resistenza alla degradazione da parte degli enzimi del fegato (microsomi epatici umani), suggerendo una potenziale buona durata d’azione nell’organismo. I due atomi di fluoro sembrano proteggerlo dal metabolismo.
- Non Tossico: Non ha mostrato citotossicità in test su linee cellulari, anche a concentrazioni molto alte rispetto alla sua potenza sul recettore.
Abbiamo anche usato modelli computazionali (docking molecolare), basati su recenti strutture del recettore ottenute con criomicroscopia elettronica (cryo-EM), per predire come PSB-172656 si lega a MRGPRX2. Il modello suggerisce che si inserisca in una tasca specifica, formando un legame idrogeno chiave con un residuo di acido aspartico (Asp184) e interagendo con altri residui tramite forze idrofobiche ed elettrostatiche, spiegando la sua alta affinità e la SAR osservata.
La Prova del Nove: Efficacia sui Mastociti Umani
Ok, la molecola è potente e selettiva in provetta, ma funziona dove serve, cioè sui mastociti? Assolutamente sì!
Abbiamo testato PSB-172656 su diverse linee cellulari di mastociti:
- Cellule RBL-2H3 (di ratto) modificate per esprimere MRGPRX2 umano: PSB-172656 ha bloccato potentemente la degranulazione (misurata come rilascio di β-esosaminidasi) indotta da vari agonisti (C48/80, SP, PAMP-12, LL-37), con valori di IC50 (concentrazione che inibisce il 50% dell’effetto) nell’ordine dei nanomoli (da 3.8 a 15.5 nM). Importante: non ha bloccato la degranulazione indotta tramite la via classica IgE-dipendente, confermando la sua specificità per MRGPRX2.
- Cellule LAD2 (linea umana che esprime MRGPRX2 naturalmente): Anche qui, PSB-172656 ha inibito la degranulazione indotta da SP con altissima potenza (IC50 = 5.26 nM). Abbiamo anche usato la citometria a flusso per misurare l’espressione di marcatori di degranulazione sulla superficie cellulare (CD107a e CD63), confermando che PSB-172656 previene la loro comparsa dopo stimolazione con SP. Inoltre, non ha interferito con l’attivazione indotta da un altro mediatore, C3a, che agisce su un recettore diverso presente sulle LAD2, sottolineando ancora la sua selettività.
- Mastociti Primari Umani (isolati da cute umana): Questa è la prova più vicina alla realtà. Abbiamo isolato mastociti da campioni di pelle di donatori e li abbiamo trattati con PSB-172656. Anche in queste cellule “vere”, il nostro antagonista ha inibito in modo dose-dipendente la degranulazione indotta dall’agonista CST-14, mostrando un’efficacia significativa già a basse concentrazioni.
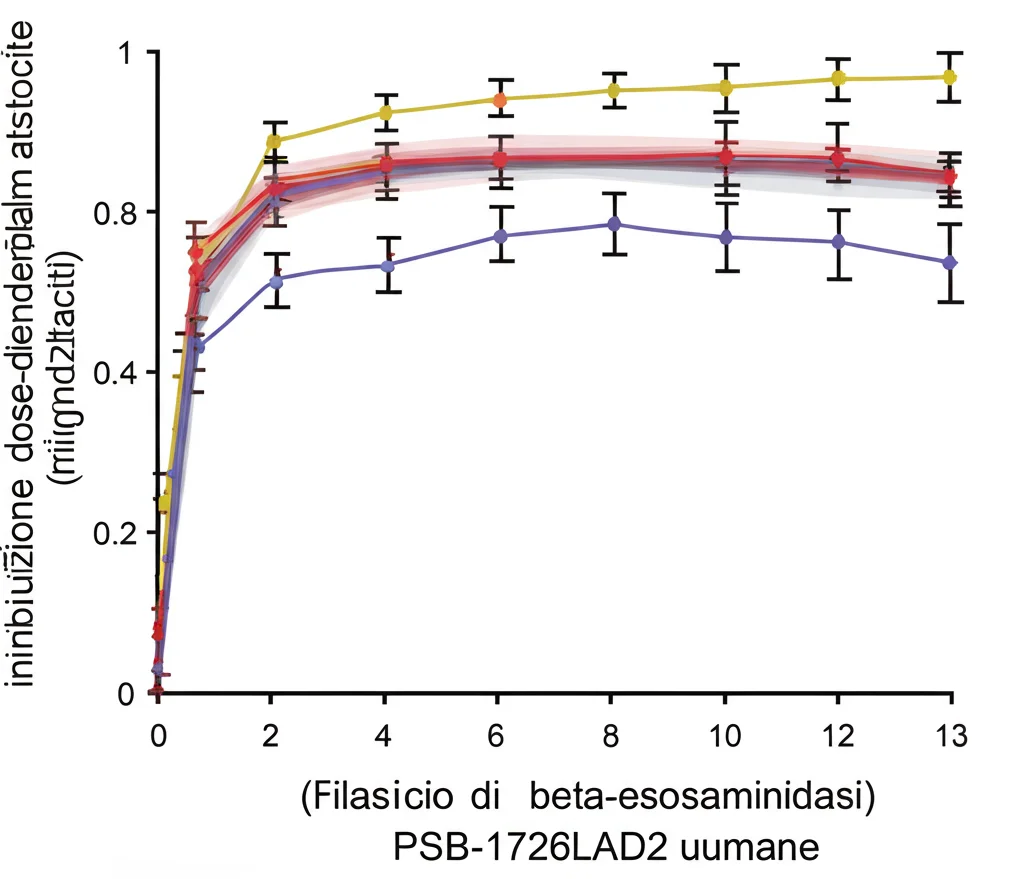
Questi risultati sono entusiasmanti perché dimostrano che PSB-172656 funziona specificamente sul suo bersaglio nei mastociti umani, senza interferire con altre vie di attivazione importanti. Questo lo rende un candidato promettente con potenziali minori effetti collaterali.
Un Ponte Verso la Clinica: Attività sul “Cugino” Murino e Modelli Animali
Come dicevo, per testare un farmaco in modelli preclinici, serve che sia attivo anche nell’animale modello, solitamente il topo. MRGPRX2 è specifico dei primati, ma si pensa che MRGPRB2 nel topo sia il suo ortologo funzionale. La grande notizia è che PSB-172656 blocca anche MRGPRB2 con una potenza incredibilmente alta (Ki = 0.302 nM), solo leggermente inferiore a quella sul recettore umano. Questo è un vantaggio enorme! La nostra analisi computazionale suggerisce che i siti di legame nei due recettori sono molto simili, spiegando questa attività incrociata.
Grazie a questa proprietà, abbiamo potuto testare PSB-172656 *in vivo* nei topi:
- Contrazione Tracheale: L’agonista C48/80 causa la contrazione della trachea nei topi, un effetto mediato da MRGPRB2. PSB-172656 ha bloccato efficacemente questa contrazione in esperimenti *ex vivo* su anelli tracheali. Questo suggerisce un potenziale ruolo nel trattamento dell’asma allergica indotta da questa via.
- Infiammazione Cutanea (Edema della Zampa): Iniettando C48/80 nella zampa di un topo si induce gonfiore (edema). La somministrazione sistemica (iniezione intraperitoneale) di PSB-172656 prima dell’iniezione di C48/80 ha ridotto significativamente il gonfiore della zampa.
- Reazione Anafilattica Sistemica: L’iniezione sistemica di C48/80 nei topi scatena una reazione simile all’anafilassi, con un aumento nel sangue di marcatori infiammatori come CCL2 (una chemochina) e IL-8. Il pre-trattamento con PSB-172656 ha impedito l’aumento significativo dei livelli di CCL2, indicando un effetto protettivo contro l’anafilassi mediata da MRGPRX2/B2.

Cosa Significa Tutto Questo? Prospettive Future
Abbiamo sviluppato PSB-172656, l’antagonista di MRGPRX2 più potente e selettivo descritto finora, con una struttura chimica unica (non peptidomimetica), ottime proprietà farmacologiche e, cosa cruciale, attività anche sull’ortologo murino MRGPRB2. Ha dimostrato efficacia nel bloccare l’attivazione dei mastociti umani e ha mostrato promettenti effetti anti-infiammatori e anti-anafilattici in modelli animali.
Questa molecola rappresenta uno strumento farmacologico preziosissimo per continuare a studiare il ruolo di MRGPRX2 (e MRGPRB2) in salute e malattia. Ma non solo: PSB-172656 ha il potenziale per essere sviluppato come un nuovo farmaco per tutte quelle malattie mediate dai mastociti e legate a MRGPRX2, come orticaria cronica, dermatite atopica, rosacea, asma, fibrosi polmonare e reazioni avverse a farmaci, per le quali le opzioni terapeutiche sono ancora limitate.
Certo, la strada è ancora lunga. Bisognerà confermare questi risultati in studi clinici sull’uomo, dato che l’ortologo murino non è identico al recettore umano, e valutare la sicurezza a lungo termine. Ma il punto di partenza è estremamente solido e promettente.
È stato un viaggio incredibile, fatto di chimica, biologia, farmacologia e tanta passione. Vedere una piccola molecola, nata da uno screening di frammenti, trasformarsi in un candidato così potente ed efficace è una soddisfazione enorme. Speriamo davvero che PSB-172656 possa un giorno arrivare ad aiutare i pazienti che soffrono di queste condizioni difficili da trattare. Continueremo a lavorarci!
Fonte: Springer