Superbatteri K.O.? Nanoparticelle d’Argento e Colistina, l’Alleanza Inaspettata Contro il Biofilm!
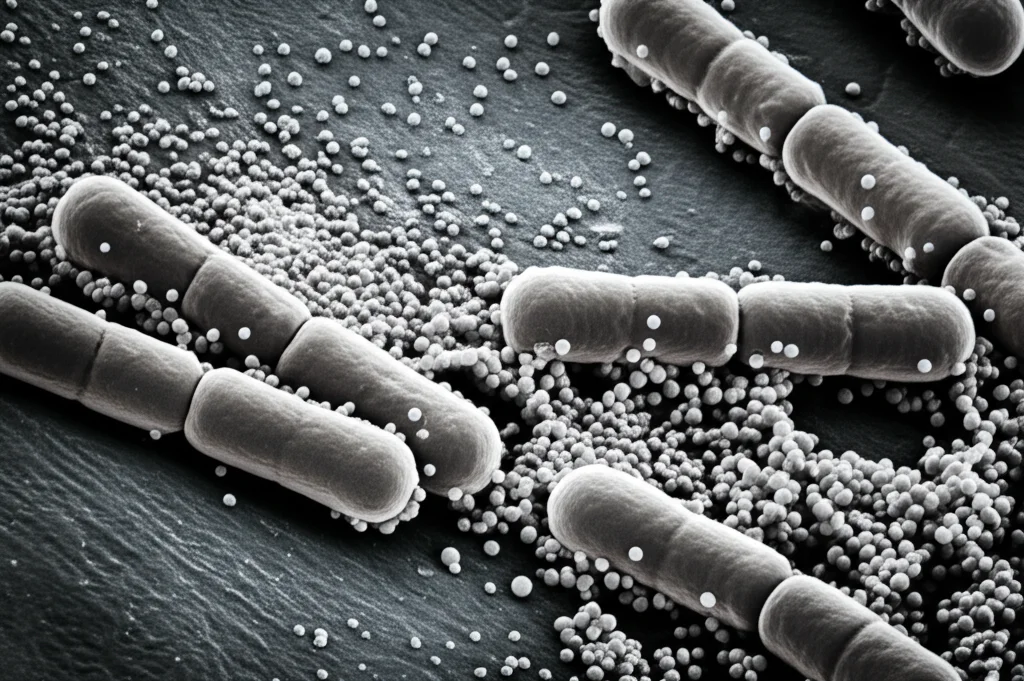
Ciao a tutti! Oggi voglio parlarvi di una sfida che mi appassiona tantissimo: la lotta contro quei nemici invisibili ma terribili che sono i batteri resistenti agli antibiotici. In particolare, ci concentreremo su un osso duro, lo Pseudomonas aeruginosa, e su come stiamo cercando nuove armi per sconfiggerlo, soprattutto quando si barrica dietro quella fortezza quasi impenetrabile chiamata biofilm.
Sì, lo so, sembra roba da film di fantascienza, ma è una realtà medica molto seria, specialmente per chi ha subito ustioni gravi. Immaginatevi: le ustioni sono già di per sé devastanti, ma le infezioni che possono subentrare, spesso causate proprio dal nostro Pseudomonas, possono peggiorare drasticamente le cose, rallentando la guarigione e aumentando il rischio di complicazioni fatali come la sepsi.
Il Nemico Numero Uno: Pseudomonas aeruginosa e la sua Corazza Biofilm
Questo batterio è un vero opportunista e un maestro della sopravvivenza. Una delle sue strategie più efficaci è quella di creare un biofilm. Cos’è? Pensatelo come una sorta di “città batterica”, una comunità organizzata di batteri avvolta in una matrice protettiva, una specie di melma appiccicosa (chiamata EPS, Sostanza Polimerica Extracellulare) che li tiene uniti e li difende. Questa barriera li protegge non solo dal nostro sistema immunitario, ma anche dagli antibiotici, rendendo le infezioni associate al biofilm incredibilmente difficili da debellare. Servono terapie antibiotiche lunghe, aggressive e, purtroppo, non sempre risolutive.
Comunicazione Batterica: Il Quorum Sensing
Come fanno i batteri a coordinarsi per costruire queste fortezze? Comunicano! Usano un sistema sofisticato chiamato Quorum Sensing (QS). In pratica, rilasciano delle molecole segnale (autoinduttori) e, quando queste raggiungono una certa concentrazione (un “quorum”, appunto), segnalano all’intera popolazione batterica che è ora di attivare certi comportamenti, come la produzione di tossine o, appunto, la formazione del biofilm. Nello Pseudomonas aeruginosa, ci sono diversi sistemi QS che lavorano insieme, come i sistemi Las e Rhl, che regolano l’espressione di geni cruciali per la virulenza e la struttura del biofilm, come pelA e pslA, responsabili della produzione dei mattoni fondamentali della matrice EPS. Capire e interrompere questa comunicazione è una delle chiavi che stiamo esplorando per indebolire il nemico.
Resistenza e Nuove Strategie: Entrano in Scena Colistina e Nanoparticelle
A complicare ulteriormente le cose, Pseudomonas aeruginosa è un campione di resistenza agli antibiotici. Ha un arsenale di meccanismi, da pompe che espellono i farmaci a mutazioni che rendono i bersagli degli antibiotici inefficaci, fino alla protezione offerta dal biofilm stesso. Per le infezioni più gravi, causate da ceppi resistenti a quasi tutto (come i CRPA, resistenti ai carbapenemi), spesso l’ultima spiaggia è la colistina. È un antibiotico “vecchio stile” ma potente, che agisce danneggiando la membrana esterna dei batteri Gram-negativi. Purtroppo, ha i suoi lati negativi, come la potenziale tossicità per reni e sistema nervoso, e anche contro la colistina sta emergendo resistenza.
Ecco perché la ricerca si sta muovendo verso strategie innovative. Una delle più promettenti è la terapia combinata e l’uso delle nanotecnologie. E qui entrano in gioco le protagoniste della nostra storia: le nanoparticelle d’argento (AgNPs).
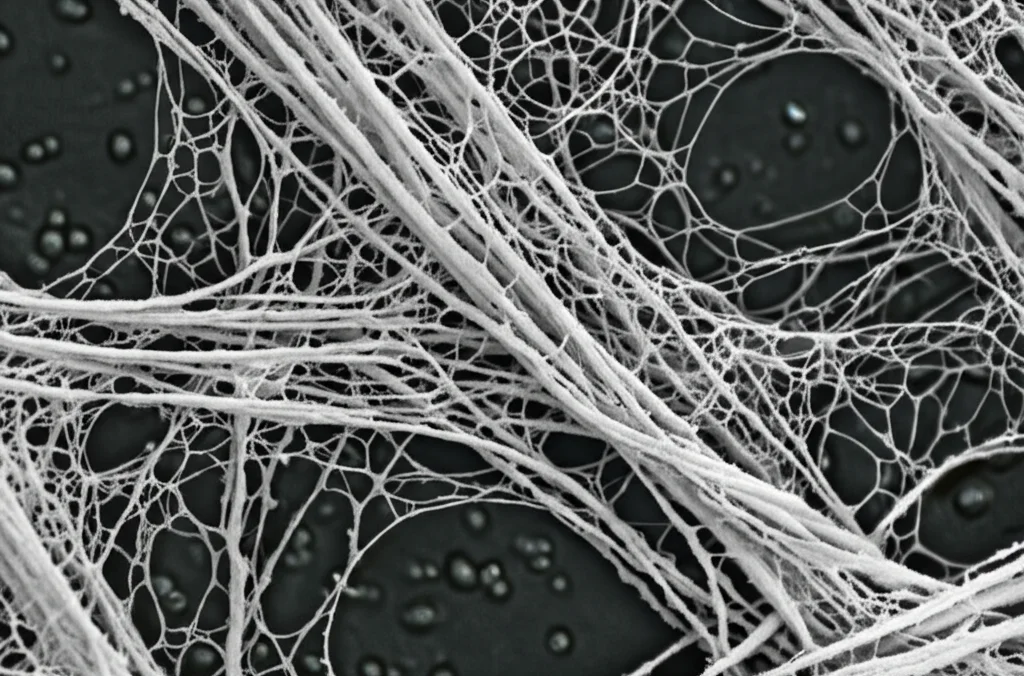
Queste particelle, infinitamente piccole, hanno dimostrato di avere potenti effetti antibatterici contro Pseudomonas, interferendo con funzioni vitali come la replicazione del DNA e l’integrità della membrana. Ma c’è di più! Stiamo parlando di AgNPs “verdi”.
Sintesi “Green” con la Propoli: La Natura ci Aiuta
Invece di usare metodi chimici potenzialmente inquinanti, abbiamo esplorato la sintesi “green” delle nanoparticelle d’argento, utilizzando estratti naturali. Nel nostro caso, abbiamo usato la propoli! Sì, quella sostanza resinosa prodotta dalle api, nota da secoli per le sue proprietà antimicrobiche. La propoli è ricca di composti (flavonoidi, acidi fenolici) che non solo aiutano a “costruire” le nanoparticelle d’argento (agendo come agenti riducenti e stabilizzanti), ma hanno anche un’attività antibatterica e anti-biofilm intrinseca. Possono disturbare le membrane batteriche, inibire enzimi essenziali e persino interferire con il Quorum Sensing. Un aiuto doppio dalla natura!
L’Esperimento: Unire le Forze Contro Ceppi Super-Resistenti
La nostra ipotesi era: e se combinassimo la colistina con queste nanoparticelle d’argento “verdi” create con la propoli? Potremmo ottenere un effetto sinergico, cioè un risultato maggiore della somma delle parti, permettendoci magari di usare meno colistina (riducendo la tossicità) e superando la resistenza?
Per verificarlo, abbiamo lavorato con 10 ceppi clinici di P. aeruginosa isolati da pazienti con gravi ustioni ricoverati in terapia intensiva in Iran. E non erano ceppi qualsiasi: erano tutti multiresistenti (MDR), molto resistenti alla colistina e forti produttori di biofilm. Una vera sfida.
Abbiamo prima sintetizzato e caratterizzato le nostre AgNPs “verdi” (verificandone forma, dimensione, composizione e sicurezza su cellule umane – un passo fondamentale!). Poi, abbiamo testato la sensibilità dei batteri a colistina e AgNPs separatamente e, soprattutto, in combinazione (usando una tecnica chiamata “checkerboard assay”). Abbiamo misurato la concentrazione minima per inibire la crescita (MIC) e quella per inibire la formazione del biofilm (MBIC).
Risultati Sorprendenti: Sinergia e Distruzione del Biofilm
I risultati sono stati davvero incoraggianti! Per molti dei ceppi testati, la combinazione di AgNPs e colistina (che abbiamo chiamato AgNPs@CL) ha mostrato un chiaro effetto sinergico. Questo significa che insieme, i due agenti erano molto più efficaci nell’inibire sia la crescita batterica che la formazione del biofilm, permettendo di ridurre significativamente le concentrazioni necessarie di entrambi rispetto all’uso singolo. In alcuni casi, la concentrazione di AgNPs necessaria è stata ridotta fino a 4 volte e quella di colistina fino a 3 volte! Per altri ceppi, l’effetto è stato “additivo”, comunque un miglioramento.
Ma volevamo vedere l’effetto sul biofilm con i nostri occhi. Abbiamo usato la Microscopia Elettronica a Scansione (SEM). Le immagini erano impressionanti: mentre i batteri non trattati formavano biofilm densi e strutturati, quelli trattati con AgNPs o colistina da soli mostravano una riduzione. Ma il trattamento combinato AgNPs@CL ha causato la devastazione più evidente: biofilm radi, disgregati, con pochissimi batteri superstiti.
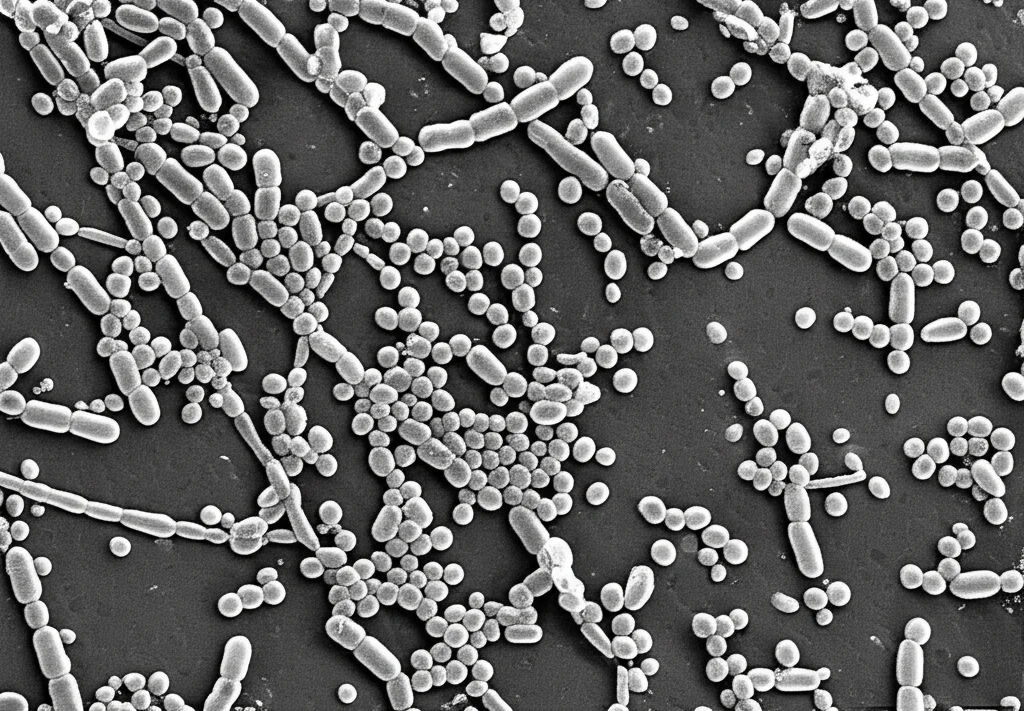
Ingrandendo ancora di più (fino a 20.000 volte!), abbiamo osservato i danni a livello cellulare: membrane perforate, cellule “sgonfie” e raggrinzite, perdite di materiale interno e strane vescicole sulla superficie. Segni inequivocabili che la combinazione stava colpendo duramente i batteri.
Silenziando la Comunicazione Batterica
E il Quorum Sensing? Abbiamo analizzato l’espressione dei geni chiave del QS (lasI, lasR, rhlI, rhlR) e della formazione del biofilm (pelA, pslA) usando la RT-qPCR. Nei ceppi che avevano mostrato sinergia con AgNPs@CL, abbiamo osservato una riduzione significativa dell’espressione di tutti questi geni, molto più marcata rispetto ai trattamenti singoli. In pratica, la combinazione stava “silenziando” la comunicazione batterica e bloccando la costruzione del biofilm alla radice! Il gene pelA è risultato tra i più soppressi. È interessante notare che nel ceppo che aveva mostrato solo un effetto additivo, la soppressione dei geni QS non era così significativa, suggerendo che la risposta alla terapia combinata è legata anche alle caratteristiche genetiche specifiche di ogni ceppo batterico.
Perché Funziona e Cosa Significa per il Futuro?
Come spieghiamo questa sinergia? L’idea è che le nanoparticelle d’argento, magari aiutate anche dai composti della propoli, danneggino la membrana esterna del batterio. Questa “breccia” faciliterebbe l’ingresso della colistina, permettendole di agire più efficacemente. Inoltre, entrambe le componenti colpiscono diverse funzioni vitali del batterio, inclusa la regolazione del QS, portando a un collasso delle difese e della capacità di formare il biofilm. La diversità genetica tra i ceppi spiega perché alcuni rispondono meglio (sinergia) e altri meno (additività).
Questi risultati sono entusiasmanti, specialmente pensando agli ambienti critici come le terapie intensive e i centri ustioni, dove le infezioni da P. aeruginosa MDR sono un incubo. La combinazione AgNPs@CL potrebbe diventare un’importante terapia aggiuntiva, da affiancare agli antibiotici convenzionali, per migliorare l’efficacia dei trattamenti, ridurre le dosi (e quindi la tossicità) e combattere i biofilm resistenti.
Certo, la strada è ancora lunga. Questo è uno studio preliminare su un numero limitato di ceppi. Serviranno ricerche più ampie, su una maggiore diversità di isolati batterici, per confermare questi risultati. Dovremo anche approfondire l’impatto su altri sistemi di QS (come il PQS) e investigare potenziali meccanismi di resistenza specifici per l’argento (geni *sil*). Magari potremmo anche esplorare l’aggiunta di altri composti naturali, come la curcumina, per potenziare ulteriormente l’effetto anti-biofilm.
Ma il messaggio fondamentale è chiaro e pieno di speranza: combinando la potenza “antica” della colistina con l’innovazione delle nanoparticelle d’argento “verdi”, derivate da un prodotto naturale come la propoli, abbiamo forse trovato un nuovo, potente alleato nella difficile battaglia contro i superbatteri e le loro fortezze biofilm. La natura e la tecnologia, insieme, potrebbero davvero fare la differenza!
Fonte: Springer