Osteosarcoma: La Nanomedicina che Scatena la “Morte Programmata” per Vincere!
Ciao a tutti, appassionati di scienza e scoperte! Oggi voglio parlarvi di qualcosa di veramente affascinante che sta emergendo nel campo della lotta contro i tumori, in particolare contro l’osteosarcoma, una forma di cancro osseo che purtroppo presenta ancora molte sfide terapeutiche. Immaginate un nemico difficile da sconfiggere, per cui le armi tradizionali a volte non bastano. Ecco, l’osteosarcoma è un po’ così. Ma la ricerca non si ferma mai, e oggi vi racconto di una nuova strategia super innovativa: una nanomedicina progettata per colpire il tumore su più fronti contemporaneamente.
L’Osteosarcoma: Un Nemico Ostico
Partiamo dalle basi. L’osteosarcoma (OS) è il tumore osseo primario più comune, soprattutto tra bambini e adolescenti. Nonostante i progressi con chirurgia, chemioterapia neoadiuvante e radioterapia, i risultati, specialmente nei casi metastatici o recidivanti, non sono ancora quelli che vorremmo. C’è un bisogno disperato di nuove terapie più efficaci e mirate. Negli ultimi anni, le fototerapie mediate dalla luce nel vicino infrarosso (NIR), come la terapia fototermica (PTT) e la terapia fotodinamica (PDT), si sono fatte strada come alternative promettenti. Sono precise, poco invasive e facili da usare. La PTT usa la luce per generare calore e “cuocere” le cellule tumorali, mentre la PDT usa la luce per attivare un agente fotosensibilizzante che produce specie reattive dell’ossigeno (ROS), molecole tossiche che uccidono le cellule cancerose. Figo, no? Però, c’è un “ma”. A causa dell’eterogeneità del tumore, della presenza di cellule resistenti al calore e di meccanismi di difesa delle cellule tumorali, spesso queste terapie, usate da sole, non riescono a eliminare completamente il cancro.
La Forza della Sinergia: PDT, PTT e… Ferroptosi!
E se potessimo combinare più strategie per un attacco massiccio? Qui entra in gioco la sinergia! Combinare PTT e PDT è già un passo avanti: il calore della PTT e i ROS della PDT lavorano insieme per distruggere le cellule tumorali, anche quelle più resistenti. Ma possiamo fare di più? Assolutamente sì! Introduciamo un terzo attore: la ferroptosi. Mai sentita? È una forma di morte cellulare programmata, diversa dall’apoptosi (la morte cellulare “classica”), che dipende dal ferro e si caratterizza per un accumulo letale di perossidi lipidici (danni ai grassi delle membrane cellulari). Pensate alle cellule tumorali come a delle fortezze con potenti sistemi di difesa antiossidante. Uno dei principali difensori è il glutatione (GSH), una molecola che neutralizza i ROS e protegge la cellula. La ferroptosi viene innescata quando questi sistemi di difesa vanno in tilt, in particolare quando l’enzima GPX4 (Glutatione Perossidasi 4), che usa il GSH come carburante per riparare i danni lipidici, viene messo fuori gioco. Se riusciamo a ridurre i livelli di GSH e/o a inibire GPX4, possiamo indurre la ferroptosi e far “autodistruggere” le cellule tumorali. Interessante, vero? Il problema è che le cellule tumorali sono furbe: anche se togliamo GSH, possono produrne di nuovo. Serve un doppio attacco: ridurre il GSH presente *e* bloccarne la produzione.
Ecco CSIR: La Nanoparticella “Tuttofare”
Ed è qui che arriva la nostra protagonista: una nanomedicina carrier-free (cioè senza un veicolo di trasporto inerte, fatta solo di molecole attive!) chiamata SRF@CuSO4.5H2O@IR780 (CSIR). Un nome un po’ tecnico, lo so, ma ogni pezzo ha un ruolo cruciale:
- IR780: È un colorante che ha due fantastiche proprietà. Primo, assorbe la luce nel vicino infrarosso (NIR, a 808 nm) e la converte sia in calore (per la PTT) sia in ROS (per la PDT). Secondo, ha una naturale tendenza ad accumularsi nei tumori e persino nei mitocondri, le centrali energetiche delle cellule.
- Sorafenib (SRF): È un farmaco già approvato per altri tumori, noto per la sua capacità di indurre ferroptosi. Come? Inibisce un trasportatore sulla membrana cellulare chiamato sistema xCT (SLC7A11), che è responsabile dell’importazione di cistina, un amminoacido essenziale per la sintesi del GSH. Bloccando xCT, SRF blocca la produzione di nuovo GSH.
- Ioni Rame (Cu2+): Il rame è un metallo affascinante. Gli ioni Cu2+ possono reagire direttamente con il GSH presente nella cellula, consumandolo. Inoltre, questa reazione può generare ioni Cu+, ancora più reattivi nel produrre ROS attraverso reazioni simili a quelle di Fenton, amplificando lo stress ossidativo. E non è tutto: il Cu2+ funge anche da “ponte” per tenere insieme SRF e IR780 nella nanoparticella, grazie a interazioni elettrostatiche e di coordinazione.
Queste tre componenti si auto-assemblano, formando nanoparticelle stabili (le CSIR) grazie a interazioni elettrostatiche e π-π stacking. Essendo “carrier-free”, si riducono i potenziali effetti collaterali legati ai materiali trasportatori.
Come Funziona l’Attacco Combinato di CSIR?
Immaginate queste nanoparticelle CSIR iniettate nel flusso sanguigno. Grazie alle loro dimensioni nanometriche e all’effetto EPR (Enhanced Permeability and Retention) – un fenomeno per cui le nanoparticelle tendono ad accumularsi nei tumori perché i vasi sanguigni tumorali sono “permeabili” e il drenaggio linfatico è inefficiente – le CSIR raggiungono il sito del tumore. Una volta dentro l’ambiente tumorale, che è leggermente acido e ricco di GSH, succede la magia:
- Il GSH presente reagisce con il Cu2+ delle nanoparticelle, venendo consumato. Questa reazione destabilizza anche le CSIR, che iniziano a rilasciare i loro componenti: IR780, SRF e Cu2+.
- Il SRF rilasciato va a bloccare il trasportatore xCT, impedendo alla cellula tumorale di produrre nuovo GSH.
- Il Cu2+ rilasciato continua a consumare il GSH rimasto e potenzialmente genera altri ROS.
- A questo punto, illuminiamo il tumore con un laser NIR (808 nm). L’IR780 assorbe la luce e scatena l’inferno: genera un forte calore (PTT) e una grande quantità di ROS (PDT).
- L’aumento massiccio di ROS e la drastica riduzione del GSH (sia per consumo diretto sia per blocco della sintesi) mandano in tilt l’enzima GPX4.
- Senza la protezione di GSH e GPX4, i lipidi delle membrane cellulari vengono danneggiati irreparabilmente (perossidazione lipidica).
- La cellula tumorale entra in ferroptosi e muore.
Un attacco sinergico su tutti i fronti: PTT + PDT + Ferroptosi indotta dalla deplezione e dall’inibizione della sintesi di GSH!
Le Prove sul Campo: Dalle Cellule ai Topi
Bello sulla carta, ma funziona davvero? Beh, i ricercatori hanno messo alla prova le CSIR con una serie di esperimenti.
In vitro (sulle cellule di osteosarcoma K7M2 in laboratorio):
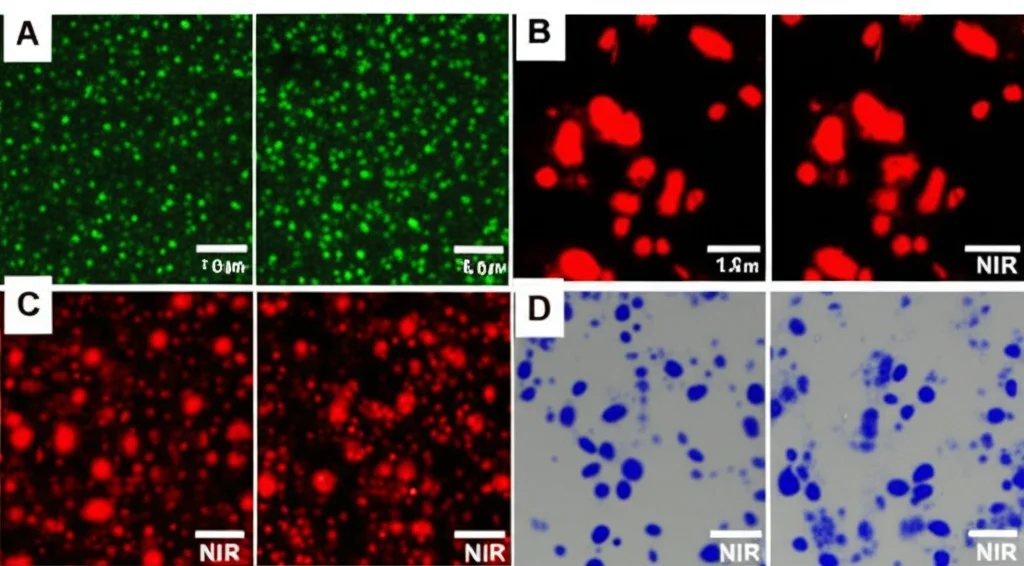
- Internalizzazione: Hanno visto che le cellule tumorali “mangiavano” avidamente le nanoparticelle CSIR, molto più dei componenti liberi somministrati separatamente.
- GSH e ROS: Hanno confermato che le CSIR riducevano drasticamente i livelli di GSH e, con l’irradiazione NIR, aumentavano enormemente i livelli di ROS intracellulari.
- Morte Cellulare: Usando coloranti specifici (Calceina-AM/PI), hanno visto che il trattamento con CSIR + NIR uccideva la stragrande maggioranza delle cellule tumorali (fino al 98%!), molto più efficacemente dei singoli componenti o delle combinazioni parziali.
- Ferroptosi Confermata: Hanno osservato i segni tipici della ferroptosi: danni ai mitocondri (visibili al microscopio elettronico e tramite misurazione del potenziale di membrana mitocondriale), accumulo di perossidi lipidici (misurato con la sonda BODIPY-C11) e riduzione dei livelli delle proteine chiave GPX4 e xCT (verificata con Western Blot).
- Analisi Genomica: Un’analisi dell’espressione genica (RNA-Seq) ha mostrato che le cellule trattate con CSIR attivavano proprio i percorsi molecolari legati alla ferroptosi, confermando il meccanismo d’azione a livello molecolare.
In vivo (su topi con tumori di osteosarcoma):
- Accumulo nel Tumore: Utilizzando l’imaging a fluorescenza, hanno visto che le CSIR iniettate nei topi si accumulavano preferenzialmente nel tumore grazie all’effetto EPR, rimanendo lì per ore.
- Effetto Fototermico: Irradiando i tumori dei topi trattati con CSIR, la temperatura nella zona tumorale saliva rapidamente sopra i 42°C (la soglia per l’ablazione termica), confermando l’efficacia della PTT anche in un organismo vivente.
- Efficacia Antitumorale: Questo è il dato più importante! I topi trattati con CSIR + irradiazione NIR hanno mostrato una riduzione drastica della crescita tumorale rispetto a tutti gli altri gruppi di controllo (topi non trattati, trattati solo con i singoli componenti, o con la miscela dei componenti non assemblati in nanoparticelle). In alcuni topi trattati con CSIR, il tumore è addirittura scomparso completamente!
- Sicurezza: Durante il trattamento, i topi non hanno mostrato perdita di peso significativa e gli esami del sangue e l’analisi istologica degli organi principali (cuore, fegato, milza, polmoni, reni) non hanno rivelato segni di tossicità rilevante. Questo suggerisce un buon profilo di sicurezza per le CSIR.
- Conferma Istologica: L’analisi dei tumori prelevati alla fine dell’esperimento ha mostrato estesa necrosi (morte tissutale) nei tumori trattati con CSIR + NIR. Inoltre, i marcatori di proliferazione cellulare (Ki-67) e le proteine chiave della ferroptosi (GPX4, xCT) erano significativamente ridotti, confermando l’efficacia e il meccanismo d’azione anche in vivo.

Un Futuro Brillante per la Lotta all’Osteosarcoma?
Questi risultati sono davvero entusiasmanti! Abbiamo sviluppato una nanomedicina “intelligente”, la CSIR, che non ha bisogno di veicoli esterni, è biocompatibile e attacca l’osteosarcoma con una strategia combinata potentissima: PTT, PDT e ferroptosi indotta mirando al GSH. Sfruttando le vulnerabilità metaboliche delle cellule tumorali (la loro dipendenza dal GSH per difendersi dallo stress ossidativo) e combinandole con l’azione mirata delle fototerapie, si ottiene un effetto sinergico che sembra in grado di eradicare il tumore in modo molto efficace, almeno nei modelli preclinici.
Certo, siamo ancora in una fase di ricerca. Saranno necessari ulteriori studi, magari su modelli animali immunocompetenti (i topi usati qui erano immunodeficienti) per valutare anche la risposta immunitaria, e poi, si spera, studi clinici sull’uomo. Ma la strada aperta da questa ricerca è incredibilmente promettente. L’idea di usare nanomedicine auto-assemblanti per orchestrare un attacco multi-modale che include la ferroptosi potrebbe rivoluzionare il trattamento non solo dell’osteosarcoma, ma potenzialmente anche di altri tipi di cancro difficili da trattare.
Insomma, teniamo d’occhio questi sviluppi! La nanomedicina ci sta regalando strumenti sempre più sofisticati e potenti nella nostra battaglia contro il cancro. E la storia di CSIR è un bellissimo esempio di come l’ingegneria molecolare e la comprensione profonda della biologia tumorale possano portare a terapie innovative e piene di speranza. Alla prossima scoperta!
Fonte: Springer