Nanomateriali Magnetici: La Rivoluzione Solare che Spazza Via l’Inquinamento Acquatico!
Ciao a tutti, appassionati di scienza e curiosi! Oggi voglio portarvi con me in un viaggio entusiasmante nel mondo delle nanotecnologie, un campo dove piccolo è bello, anzi, potentissimo! Immaginate di avere un supereroe microscopico capace di ripulire le nostre acque inquinate usando solo la luce del sole. Sembra fantascienza? Beh, tenetevi forte, perché stiamo per scoprire come dei nanocompositi magnetici a base di NiMnFeO4 e nitruro di carbonio grafitico (g-C3N4) stiano aprendo scenari incredibili nella lotta contro i coloranti industriali che appestano fiumi e mari.
Il Problema: Acque Colorate, Pericolo Invisibile
Partiamo dal problema: l’avanzamento della società, l’aumento della popolazione e la crescita industriale, se da un lato portano progresso, dall’altro generano un conto salato in termini di inquinamento. Tra i “cattivi” di questa storia ci sono i coloranti organici sintetici, rilasciati in quantità industriali da settori come quello tessile, della carta, della plastica e della pelle. Queste sostanze non solo colorano le acque, rendendole esteticamente sgradevoli, ma possono essere davvero nocive per la nostra salute, causando danni a organi vitali e, in alcuni casi, essendo cancerogene o teratogene. Insomma, una vera spina nel fianco per l’ambiente e per noi!
La Soluzione Brillante: La Fotocatalisi
Ma non disperiamo! La scienza ci offre strumenti potenti, e uno di questi si chiama fotocatalisi. Immaginatela come una reazione chimica che si attiva grazie alla luce (solare o artificiale) e a un “catalizzatore”, una sostanza che accelera la reazione senza consumarsi. Questo fotocatalizzatore, quando colpito dalla luce, “eccita” i suoi elettroni, creando delle coppie elettrone-lacuna (e-/h+). Queste coppie sono il motore che trasforma i coloranti pericolosi e stabili in sostanze innocue come acqua e anidride carbonica. Figo, no? Il trucco sta nel trovare materiali sempre più efficienti, capaci di sfruttare al meglio la luce visibile, che è la parte più abbondante dello spettro solare.
I Nostri Eroi Nanoscopici: NiMnFeO4 e g-C3N4
Ed è qui che entrano in gioco i protagonisti della nostra storia: le nanoparticelle di NiMnFeO4 e i foglietti di nitruro di carbonio grafitico (g-C3N4). Il NiMnFeO4 è un tipo di ferrite spinello mista, un materiale con proprietà magnetiche affascinanti e un sacco di siti attivi sulla sua superficie, perfetti per l’attività catalitica. Pensate che materiali simili sono già usati in medicina, per l’imaging a risonanza magnetica e persino per generare calore in terapie contro il cancro! Il g-C3N4, d’altro canto, è un semiconduttore polimerico che ama la luce visibile. L’idea geniale è stata: perché non unirli?
Una Sintesi “Su Misura” con un Tocco di Alchimia Moderna
Per creare queste meraviglie nanoscopiche, i ricercatori hanno usato un metodo di sintesi super affascinante chiamato sol-gel auto-combustione, con un piccolo aiuto da molecole speciali chiamate ligandi a base di Schiff (in particolare, H2Salen, H2Salpn e H2Salophen). Questi ligandi agiscono come “agenti di controllo”, influenzando la dimensione e la forma delle nanoparticelle di NiMnFeO4 durante la loro “cottura”. Si è scoperto che il ligando H2Salpn è stato il migliore, permettendo di ottenere nanoparticelle con una struttura cristallina pura, una morfologia desiderabile e un’energia di bandgap ottico di 2.0 eV (un valore ottimo per assorbire la luce visibile!).
Una volta ottenute le nanoparticelle di NiMnFeO4 perfette, è stato il momento di creare il nanocomposito. Immaginate di mescolare queste nanoparticelle con i foglietti di g-C3N4 usando una tecnica che sfrutta gli ultrasuoni, una specie di “frullatore” ad alta potenza, per poi farli precipitare insieme. L’obiettivo? Creare un’interfaccia intima tra i due materiali per massimizzare i benefici.

Sotto la Lente: Caratterizzazione dei Nanocompositi
Ma come facciamo a sapere se abbiamo davvero creato quello che volevamo? Qui entrano in gioco tecniche di analisi sofisticate, i nostri “occhi super potenti” per guardare nel nanomondo.
- La diffrazione dei raggi X (XRD) ci ha confermato la struttura cristallina e la purezza delle fasi del NiMnFeO4 (soprattutto con H2Salpn) e il successo nella formazione del composito con g-C3N4, mostrando i picchi caratteristici di entrambi i materiali.
- La spettroscopia infrarossa a trasformata di Fourier (FTIR) ha rivelato i legami chimici presenti, confermando la presenza dei gruppi funzionali tipici sia del NiMnFeO4 che del g-C3N4 nel composito.
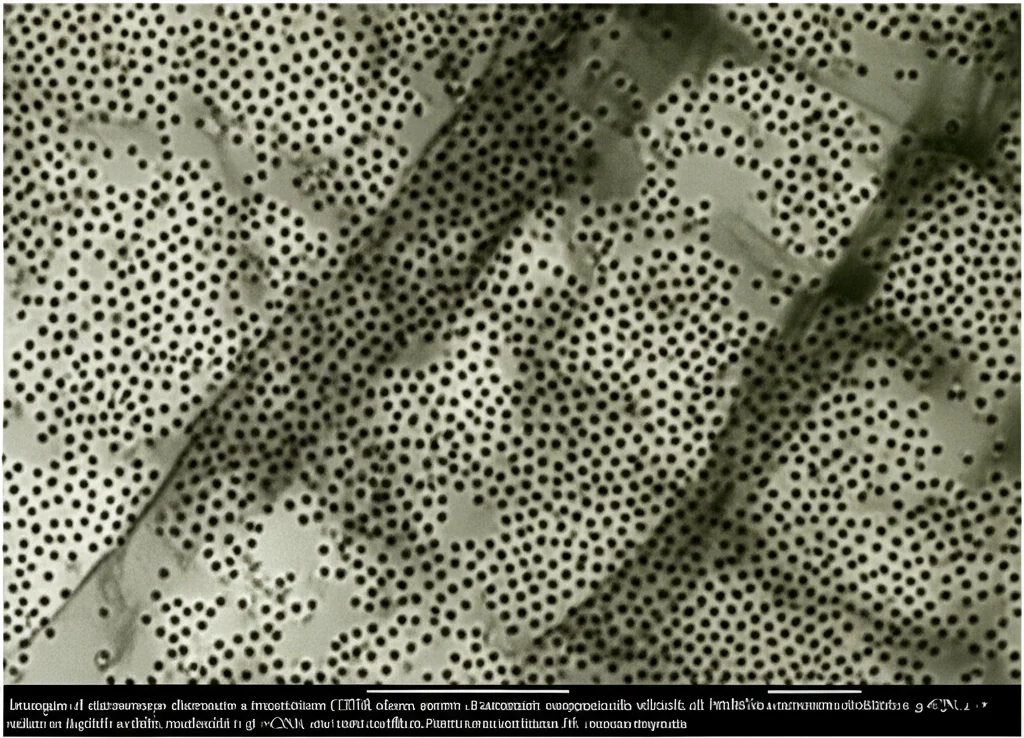
- La microscopia elettronica a scansione a emissione di campo (FE-SEM) e la microscopia elettronica a trasmissione (TEM) ci hanno regalato immagini mozzafiato della morfologia: le nanoparticelle di NiMnFeO4, specialmente quelle sintetizzate con H2Salpn, apparivano uniformi e di dimensioni comprese tra 24.74 e 87.41 nm. Nelle immagini del composito, si vedeva chiaramente come le nanoparticelle di NiMnFeO4 avvolgessero uniformemente i fogli di g-C3N4.
- L’analisi EDS (spettroscopia a dispersione di energia) ha confermato la composizione elementare, mostrando la presenza di Ni, Mn, Fe, O nel NiMnFeO4 puro, e l’aggiunta di C e N nel composito, senza impurità indesiderate.
Questi risultati ci dicono che la sintesi è andata a buon fine e che abbiamo tra le mani un materiale ben strutturato e promettente!
Proprietà Magnetiche e Ottiche: I Segreti dell’Efficienza
Una caratteristica super interessante del NiMnFeO4 è la sua natura magnetica. Le misure con un magnetometro a campione vibrante (VSM) hanno mostrato che il NiMnFeO4 puro ha proprietà ferromagnetiche. Quando è stato combinato con il g-C3N4, la magnetizzazione è diminuita un po’, ma questo è un buon segno: indica un’interazione tra i due componenti. Il vantaggio? Questi nanocompositi possono essere facilmente recuperati dall’acqua usando un semplice magnete dopo il processo di depurazione, rendendoli riutilizzabili! Immaginate quanto sia pratico!
Dal punto di vista ottico, la spettroscopia UV-Vis a riflettanza diffusa (DRS) ha confermato che il NiMnFeO4 ha un bandgap di circa 2.0 eV, mentre il g-C3N4 ha un bandgap di circa 2.7 eV. L’unione di questi due materiali in un eterostruttura non solo arricchisce i siti catalitici attivi ma, cosa fondamentale, accelera la separazione delle cariche (elettroni e lacune) generate dalla luce, rendendo il processo fotocatalitico più efficiente. Pensatela come una squadra ben assortita dove ognuno fa il suo lavoro al meglio, potenziando il risultato finale.
Inoltre, le analisi BET hanno rivelato che l’area superficiale del nanocomposito NiMnFeO4/g-C3N4 è significativamente maggiore (circa 10.2 volte!) rispetto a quella del NiMnFeO4 puro. Una maggiore area superficiale significa più “punti di contatto” per le reazioni, quindi una maggiore efficienza!
All’Opera! La Degradazione dei Coloranti
E ora, il momento della verità: questi nanocompositi funzionano davvero? Per testarli, i ricercatori hanno usato due coloranti modello: il verde malachite (cationico) e l’eosina Y (anionico), entrambi ampiamente usati e noti inquinanti. Hanno messo 30 mg di catalizzatore in 30 mL di soluzione di colorante (10 ppm) e hanno illuminato il tutto con una lampada a luce visibile.
I risultati sono stati strabilianti! Il nanocomposito NiMnFeO4/g-C3N4 con un rapporto in peso di 0.25:1 si è rivelato il campione più performante. È riuscito a degradare ben il 95.12% dell’eosina Y in soli 120 minuti! Per darvi un’idea, il NiMnFeO4 puro ha raggiunto il 90.48% e il g-C3N4 l’89.77% per lo stesso colorante. Un miglioramento notevole, che dimostra il sinergismo tra i due componenti. Curiosamente, entrambi i materiali (singoli e compositi) si sono dimostrati più efficaci contro l’eosina (anionica) rispetto al verde malachite (cationico).
Aumentare ulteriormente la quantità di NiMnFeO4 nel composito (rapporti 0.5:1 e 1:1) non ha portato a miglioramenti, anzi, ha leggermente ridotto l’efficienza. Questo suggerisce che c’è un “punto dolce” nel rapporto tra i due materiali per massimizzare la separazione delle cariche e l’area superficiale attiva.
Il Meccanismo Segreto: Chi Fa il Lavoro Sporco?
Ma come avviene esattamente questa degradazione? Per capirlo, sono stati condotti esperimenti con degli “spazzini” di specie reattive. Aggiungendo sostanze che “catturano” specifici radicali, si può capire quali sono i principali responsabili della pulizia. Ebbene, si è scoperto che i radicali idrossilici (•OH) e i radicali superossido (•O2‒) sono i veri eroi che attaccano e scompongono le molecole di colorante. Le lacune (h+), invece, sembrano avere un ruolo meno preponderante in questo specifico sistema.
Il meccanismo proposto è affascinante: sotto la luce visibile, sia il NiMnFeO4 che il g-C3N4 si eccitano. Grazie alla loro intima connessione nell’eterostruttura, gli elettroni e le lacune fotogenerati si separano più efficacemente e migrano tra i due materiali. Gli elettroni possono reagire con l’ossigeno per formare i radicali •O2‒, mentre le lacune (o gli elettroni che reagiscono con l’acqua) possono portare alla formazione dei potentissimi radicali •OH. Questi radicali, altamente ossidanti, sono i killer dei coloranti!

Riciclabilità e Prospettive Future
Un altro aspetto cruciale è la stabilità e la riciclabilità del catalizzatore. Il nostro campione ottimale NiMnFeO4/g-C3N4 (0.25:1) è stato testato per cinque cicli consecutivi di degradazione dell’eosina. Anche se c’è stato un leggero calo di efficienza (dal 95.12% al 74.67% dopo 5 cicli, probabilmente dovuto a un po’ di materiale perso durante il recupero o a siti attivi occupati), i risultati dimostrano una buona robustezza. E ricordate, grazie alle sue proprietà magnetiche, recuperarlo è un gioco da ragazzi!
In conclusione, questa ricerca ci mostra come l’ingegneria a livello nanometrico, combinando sapientemente materiali con proprietà complementari, possa portare a soluzioni innovative ed efficaci per problemi ambientali urgenti. I nanocompositi NiMnFeO4/g-C3N4 non sono solo affascinanti dal punto di vista scientifico, ma rappresentano una speranza concreta per avere acque più pulite, sfruttando l’energia più abbondante e pulita che abbiamo: quella del sole. C’è ancora strada da fare per l’applicazione su larga scala, ma la direzione è quella giusta. E chissà quali altre meraviglie ci riserverà il nanomondo!
Alla prossima avventura scientifica!
Fonte: Springer







