Arsenico Addio! Nanobarre di Ematite dalla Laterite: La Mia Rivoluzionaria Scoperta per Acque Più Pulite
Ciao a tutti! Oggi voglio parlarvi di una sfida che mi sta particolarmente a cuore: la contaminazione da arsenico nelle nostre acque. È un problema serio, sapete? Questo metalloide tossico, rilasciato da attività industriali, minerarie e agricole, può finire nelle nostre riserve idriche, mettendo a rischio la salute di milioni di persone e l’equilibrio degli ecosistemi. Pensate che la concentrazione consigliata di arsenico (As(V)) nell’acqua potabile deve essere inferiore a 10 µg/L! Superata questa soglia, i rischi per reni, pelle, polmoni e vescica diventano concreti, per non parlare di altre malattie.
Esistono già diverse tecniche per rimuovere questi inquinanti, come l’ossidazione avanzata, l’ozonizzazione, la nanofiltrazione… ma spesso sono costose, richiedono molta energia o producono rifiuti secondari. Tra tutte, l’adsorbimento si distingue per efficacia, costi contenuti e sostenibilità ambientale. Ecco perché, nel mio laboratorio, ci siamo messi alla ricerca di un materiale adsorbente “supereroe”: economico, efficiente, facile da produrre e, perché no, derivato da risorse naturali abbondanti.
La Genesi delle Nanobarre di Ematite: Un Tesoro dalla Laterite
E se vi dicessi che la soluzione potrebbe trovarsi in una comunissima roccia? Abbiamo puntato gli occhi sulla laterite, un minerale ferroso naturale, abbondante e a basso costo, proveniente specificamente dalla zona di El-Gedida, nell’Oasi di Bahariya, nel Deserto Occidentale egiziano. Questa laterite è composta per ben il 96.73% da Fe2O3 (ossido di ferro, il componente principale dell’ematite), con piccole impurità di SiO2 e Al2O3.
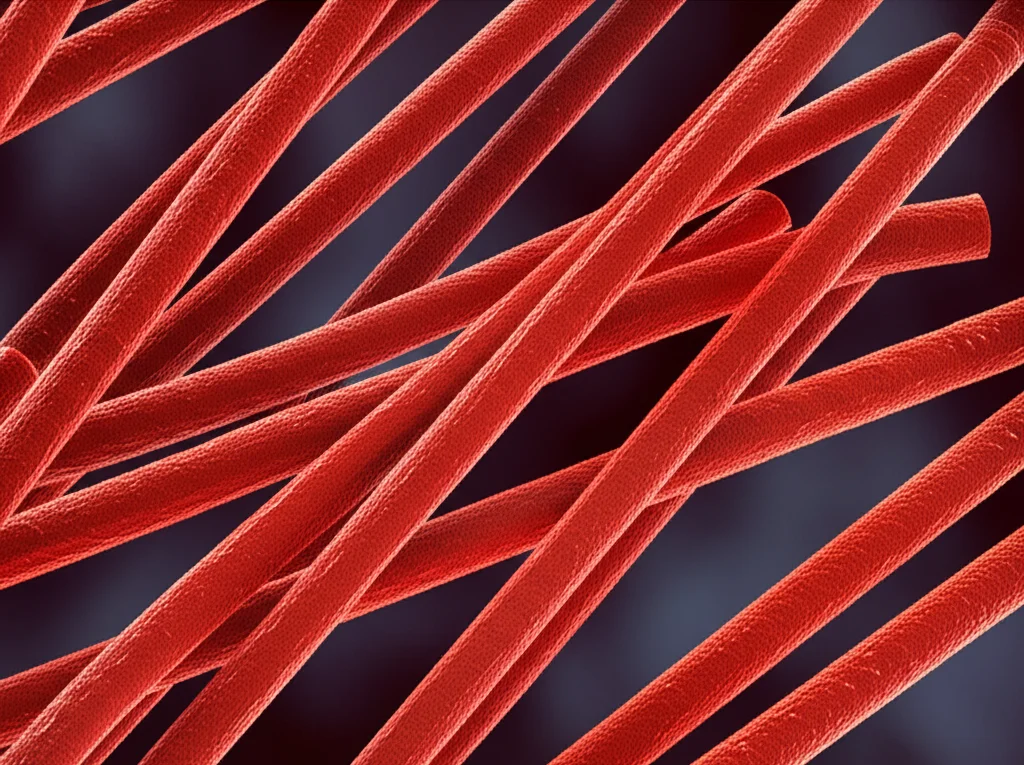
La nostra idea? Trasformare questa materia prima grezza in qualcosa di molto più potente: nanobarre di ematite (α-Fe2O3). L’ematite è già nota per le sue buone proprietà adsorbenti, ma sapevamo che modificandone la morfologia a livello nanometrico avremmo potuto fare un salto di qualità. E come l’abbiamo fatto? Con un metodo idrotermale semplice ed ecologico. In pratica, abbiamo preso la polvere di laterite (macinata finemente), l’abbiamo mescolata con una soluzione alcalina di NaOH e poi “cotta” in un reattore idrotermale a 100°C per periodi di tempo variabili: 12 ore (campione HM12), 24 ore (HM24), 36 ore (HM36) e 48 ore (HM48). Questo processo, amici, ha portato a una vera e propria metamorfosi!
La Magia della Modificazione: HM36, la Star dell’Adsorbimento
Analizzando i nostri campioni con tecniche sofisticate come la diffrazione a raggi X (XRD), la spettroscopia infrarossa a trasformata di Fourier (FT-IR) e la microscopia elettronica a scansione (SEM), abbiamo visto cose incredibili. L’XRD ci ha mostrato che, sebbene la fase cristallina rimanesse ematite, c’erano cambiamenti significativi nella struttura, come deformazioni del reticolo e un aumento dei difetti superficiali, soprattutto con l’aumentare del tempo di modificazione. La dimensione media dei cristalliti, per esempio, si è ridotta dai 18 nm del materiale grezzo ai 13 nm di HM36 e ai 12.4 nm di HM48.
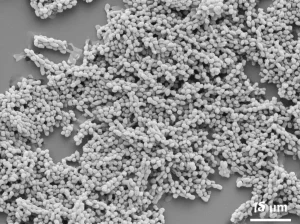
L’FT-IR ha confermato le modifiche nella coordinazione Fe-O e la comparsa di gruppi idrossilici sulla superficie, segno dell’impatto del trattamento. Ma la vera sorpresa è arrivata dalla SEM e dall’analisi dell’area superficiale BET. Le immagini SEM hanno rivelato che le particelle massicce e agglomerate della laterite originale si trasformavano in nanobarre ben sviluppate, soprattutto nel campione HM36. E questa trasformazione morfologica ha avuto un effetto esplosivo sull’area superficiale: HM36 ha raggiunto un valore pazzesco di 154.7 m2/g, molto più alto degli altri campioni (HM12: 83.5 m2/g, HM24: 141.5 m2/g, HM48: 144.6 m2/g)! Più area superficiale significa più “punti di aggancio” per l’arsenico. Infatti, i campioni HM24, HM36 e HM48 hanno mostrato anche la presenza di mesopori, utili per l’adsorbimento.

I test di adsorbimento dell’arsenato (As(V)) hanno confermato le nostre aspettative: HM36 è risultato il campione migliore, con una capacità di rimozione di ben 151.4 mg/g! Seguito da HM48 (138.2 mg/g), HM24 (125.4 mg/g) e HM12 (113.8 mg/g). Questi risultati sono fantastici se confrontati con molti altri materiali adsorbenti riportati in letteratura.
Dentro il Meccanismo di Adsorbimento: Sterica ed Energetica
Ma come funziona esattamente questa “cattura” dell’arsenico? Abbiamo usato modelli di equilibrio avanzati, basati sulla fisica statistica, per capirci di più. Questi modelli ci hanno permesso di svelare parametri sterici ed energetici. Per esempio, HM36 ha mostrato la più alta densità di siti attivi (Nm = 67.9 mg/g). E la cosa più affascinante è che ogni sito attivo è in grado di ospitare fino a tre ioni As(V)! Questo suggerisce un meccanismo di interazione multi-ionica, con gli ioni di arsenico che si dispongono in modo verticale sulla superficie dell’adsorbente. Immaginate delle piccole torri di arsenico che si formano sui siti attivi!
L’energia di adsorbimento, valutata sia con modelli classici (< 4 kJ/mol) che con quelli di fisica statistica (< 9 kJ/mol), ha confermato che il processo è prevalentemente fisico (fisisorbimento) ed esotermico (cioè rilascia calore). Questo significa che le forze in gioco sono principalmente attrazioni elettrostatiche, legami idrogeno e forze di van der Waals. Le analisi termodinamiche hanno ulteriormente supportato la natura spontanea e favorevole dell’adsorbimento di As(V) su tutte le nostre ematiti modificate.
Fattori Chiave e Performance nel Mondo Reale
Abbiamo studiato vari parametri. Il pH della soluzione è cruciale: l’adsorbimento ottimale avviene intorno a pH 6. A pH più bassi o più alti, l’efficienza cala a causa della speciazione dell’arsenico e delle cariche superficiali dell’ematite. Il tempo di contatto necessario per raggiungere l’equilibrio è di circa 240 minuti. All’inizio l’adsorbimento è rapido, grazie all’abbondanza di siti liberi, poi rallenta man mano che questi si saturano. Gli studi cinetici hanno mostrato che il modello di pseudo-primo ordine descrive meglio il processo, confermando la predominanza del fisisorbimento.
Un aspetto fondamentale è la selettività e la robustezza in presenza di altri ioni. Abbiamo testato HM36 in presenza di anioni come NO3-, SO42-, PO43- e CO32-, e cationi come Cd(II), Pb(II), Ni(II), Co(II) e Cr(VI). Gli anioni hanno interferito poco, tranne PO43- e CO32- che, essendo simili all’arsenato, competono per i siti attivi. I cationi metallici hanno ridotto un po’ la capacità di adsorbimento, ma HM36 ha comunque mantenuto una buona efficienza.
E nel mondo reale? Abbiamo messo alla prova HM36 con acqua di rubinetto, acqua sotterranea e acque reflue. I risultati sono stati eccellenti! La capacità di adsorbimento è stata di 119.5 mg/g per acqua distillata, 111.4 mg/g per acqua di rubinetto, 105.3 mg/g per acqua sotterranea e 97.4 mg/g per acque reflue. Anche a concentrazioni di arsenico elevate (100 mg/L), ben superiori ai livelli ambientali tipici, HM36 ha fatto un ottimo lavoro.
Riciclabilità e Sostenibilità: Un Futuro Promettente
Un altro punto di forza è la riciclabilità. Dopo l’uso, abbiamo lavato HM36 con una soluzione alcalina e l’abbiamo riutilizzato per cinque cicli di adsorbimento. Certo, l’efficienza è gradualmente diminuita (da 146.7 mg/g nel primo ciclo a 98.5 mg/g nel quinto), probabilmente a causa dell’accumulo di complessi di arsenico sui siti attivi. Tuttavia, il bassissimo rilascio di ferro (< 0.001 mg/L) durante i test conferma la stabilità strutturale di HM36 e il suo minimo contributo a una contaminazione secondaria. Questo è un grande vantaggio ambientale!
Conclusioni di un Viaggio Entusiasmante
Insomma, questa ricerca mi ha davvero entusiasmato! Siamo riusciti a trasformare un minerale naturale ed economico, la laterite, in nanobarre di ematite 2D altamente efficienti per la rimozione dell’arsenico. Il campione HM36, ottenuto con 36 ore di trattamento idrotermale, si è dimostrato una vera star, con un’elevata area superficiale e una notevole capacità di adsorbimento.
Abbiamo svelato i meccanismi sterici ed energetici che governano questo processo, evidenziando l’importanza delle interazioni multi-ioniche. La facilità di sintesi, il basso costo del precursore naturale, l’elevata efficienza di rimozione e la buona riciclabilità rendono queste nanobarre di ematite, e HM36 in particolare, candidati promettenti per applicazioni reali nel trattamento delle acque reflue industriali e agricole.
Credo fermamente che questa tecnologia possa offrire soluzioni sostenibili ed economicamente vantaggiose per affrontare il grave problema della contaminazione da arsenico. E chissà, la ricerca futura potrebbe estendere l’applicazione di questi materiali ad altri inquinanti, ampliando ulteriormente il loro impatto positivo sull’ambiente e sulla nostra salute!
Fonte: Springer