Un Nano-Eroe Magnetico al Servizio dell’Ambiente: La Mia Avventura con i Fotocatalizzatori!
Ciao a tutti! Oggi voglio raccontarvi di un progetto entusiasmante a cui ho lavorato, qualcosa che potrebbe davvero fare la differenza nella lotta contro l’inquinamento idrico. Parliamoci chiaro: l’acqua pulita è una risorsa preziosissima e, con la popolazione mondiale in continua crescita, la sua gestione sta diventando una sfida sempre più critica. Pensate a quanta acqua serve per l’agricoltura, per l’industria… è fondamentale trovare modi per riciclare e riutilizzare le acque reflue industriali, non credete?
Il Problema dei Coloranti Industriali: Un Arcobaleno Tossico
Uno dei “cattivi” principali quando si parla di inquinamento idrico sono i coloranti organici. Li troviamo ovunque: nell’industria tessile, della pelle, cosmetica, della carta, delle vernici… Insomma, un sacco di prodotti che usiamo ogni giorno. Il guaio è che questi coloranti, una volta rilasciati nell’ambiente, sono un bel problema. Sono sintetici, hanno strutture chimiche complesse e, diciamocelo, sono spesso tossici, a volte addirittura cancerogeni o esplosivi!
Prendiamo ad esempio l’eosina, un colorante rosso-rosato usato in istologia (sì, quella branca della biologia che studia i tessuti!) e nell’industria tessile. O il verde malachite, un colorante cationico verde brillante usato per seta, pelle e carta. Belli da vedere, certo, ma possono causare reazioni allergiche, problemi respiratori, irritazioni agli occhi e, nei casi peggiori, aumentare il rischio di tumori. Non solo: la loro presenza nell’acqua impedisce alla luce solare di penetrare, compromettendo la fotosintesi delle piante acquatiche e portando a una carenza di ossigeno. Un vero disastro ecologico!
Vecchie Strategie e Nuove Speranze: L’Ascesa dei Nanomateriali
Negli anni, abbiamo provato un sacco di strategie per eliminare questi inquinanti: filtrazione su membrana, ozonizzazione, adsorbimento, coagulazione, trattamenti biologici… Ma spesso ci si scontra con problemi come una capacità di assorbimento insufficiente, una rimozione incompleta o la scarsa durabilità meccanica dei materiali adsorbenti. Qui entrano in gioco i nanomateriali semiconduttori. Grazie alle loro proprietà uniche, come un’elevata area superficiale e gli effetti di confinamento quantistico, stanno diventando protagonisti in molte applicazioni avanzate, inclusa la fotocatalisi.
La fotocatalisi a semiconduttore è una tecnologia super promettente, specialmente per eliminare i contaminanti organici. Immaginate: un fotocatalizzatore semiconduttore che cattura l’energia solare per degradare gli inquinanti. Il bello è che, con i fotocatalizzatori giusti, si possono degradare completamente i composti organici in poche ore, a temperatura ambiente, trasformandoli in sostanze innocue come acqua e CO2, senza produrre sottoprodotti tossici. Fantastico, no?
La Mia Idea: Un Nanocomposito Magnetico Super Efficiente!
Il punto cruciale, però, è trovare il catalizzatore giusto e, soprattutto, poterlo recuperare e riutilizzare facilmente dopo il processo. Ed è qui che la mia ricerca si è concentrata! Ho pensato: perché non combinare le proprietà fotocatalitiche con quelle magnetiche? I semiconduttori magnetici come Fe₂O₃, Fe₃O₄, e le ferriti MFe₂O₄ (dove M può essere Mn, Ni, Co, o Zn) sono molto interessanti. In particolare, la ferrite di nichel (NiFe₂O₄) ha attirato la mia attenzione per il suo basso costo, la facilità di recupero magnetico, un band gap diretto stretto e un’eccellente stabilità termica e chimica.
C’era un però: il NiFe₂O₄ da solo tende ad agglomerarsi e i portatori di carica (elettroni e lacune) si ricombinano troppo velocemente, riducendone l’efficienza. La soluzione? Combinarlo con altri semiconduttori! E così è nata l’idea di creare un nanocomposito binario magnetico NiFe₂O₄/CeO₂.
L’ossido di cerio (CeO₂), un ossido di terre rare, è un semiconduttore di tipo n con un band gap di circa 3.2 eV, economico, stabile chimicamente ed ecologico. Proprio come il TiO₂, ma con il vantaggio di poter rispondere alla luce visibile e avere un range di assorbimento più ampio. L’accoppiata NiFe₂O₄/CeO₂ mi sembrava vincente!

La “Ricetta” Sol-Gel: Semplice ed Efficace
Per preparare questi nanocompositi, ho utilizzato un metodo chiamato sol-gel auto-combustione. È una tecnica versatile che permette di controllare la struttura dei materiali, come porosità e dimensione delle particelle, e garantisce un’elevata omogeneità e purezza, il tutto a temperature più basse rispetto ai metodi tradizionali. In pratica, si parte da precursori metallici (nitrati di nichel, cerio e ferro), si aggiunge un “carburante” organico (acido maleico nel mio caso) e si forma un sol. Questo sol viene poi essiccato in un gel che, una volta acceso, subisce una reazione esotermica auto-sostenuta. Un processo quasi “magico”!
Un aspetto interessante è stato sperimentare con diversi agenti gelificanti (come TEPA, ammoniaca, etilendiammina e NaOH) per vedere come influenzassero la purezza e la dimensione delle particelle del nanocomposito NiFe₂O₄/CeO₂. Ho scoperto che usando la tetraetilenepentammina (TEPA) come base si ottenevano nanoparticelle più piccole, il che è ottimo per la fotocatalisi perché aumenta l’area superficiale attiva.
Mettiamo alla Prova il Nostro Nano-Eroe!
Una volta sintetizzato il mio nanocomposito ottimale (quello con TEPA, che ho chiamato campione S1), era il momento di testarlo. Ho scelto due coloranti “bersaglio”: l’eosina (EO), un colorante anionico, e il verde malachite (MG), un colorante cationico. L’esperimento consisteva nel mescolare 50 mg del mio fotocatalizzatore con una soluzione di colorante e illuminare il tutto con una lampada a luce visibile per 120 minuti.
I risultati sono stati davvero incoraggianti! Il mio fotocatalizzatore NiFe₂O₄/CeO₂ ha mostrato una performance notevole, con un’efficienza del 95% nella degradazione dell’eosina e un’efficienza un po’ più bassa, del 68.29%, per il verde malachite. Questo suggerisce che il mio materiale è più bravo a degradare i coloranti anionici. La costante di velocità (k) per la decolorazione dell’eosina è stata di 0.02798 min⁻¹. Non male, eh?
Abbiamo anche studiato come la concentrazione iniziale del colorante e la quantità di fotocatalizzatore influenzassero l’efficienza. Per l’eosina, una concentrazione di 10 mg/L e 50 mg di catalizzatore si sono rivelate le condizioni ottimali.
Capire Come Funziona: Il Meccanismo Segreto
Ma come fa esattamente questo nanocomposito a “mangiare” i coloranti? Tutto si basa sulla generazione di specie reattive dell’ossigeno (ROS) quando il materiale è esposto alla luce. La luce eccita gli elettroni nel semiconduttore, creando coppie elettrone-lacuna. Gli elettroni reagiscono con l’ossigeno per formare radicali superossido (·O₂⁻), mentre le lacune possono reagire con l’acqua o gli ioni OH⁻ per formare radicali idrossilici (·OH). Queste specie super reattive attaccano le molecole di colorante, spezzettandole in molecole più piccole e innocue come H₂O e CO₂.
Per capire quale di queste specie fosse la “star” del processo, ho condotto esperimenti con degli “scavenger”, delle sostanze che intrappolano specifici radicali. Aggiungendo acido ascorbico (che cattura i ·O₂⁻), l’efficienza di degradazione dell’eosina è crollata dal 95% al 58.96%! Questo ci ha fatto capire che i radicali superossido ·O₂⁻ giocano un ruolo cruciale nel meccanismo di degradazione con il mio NiFe₂O₄/CeO₂.

Caratteristiche da Campione e un Futuro Brillante
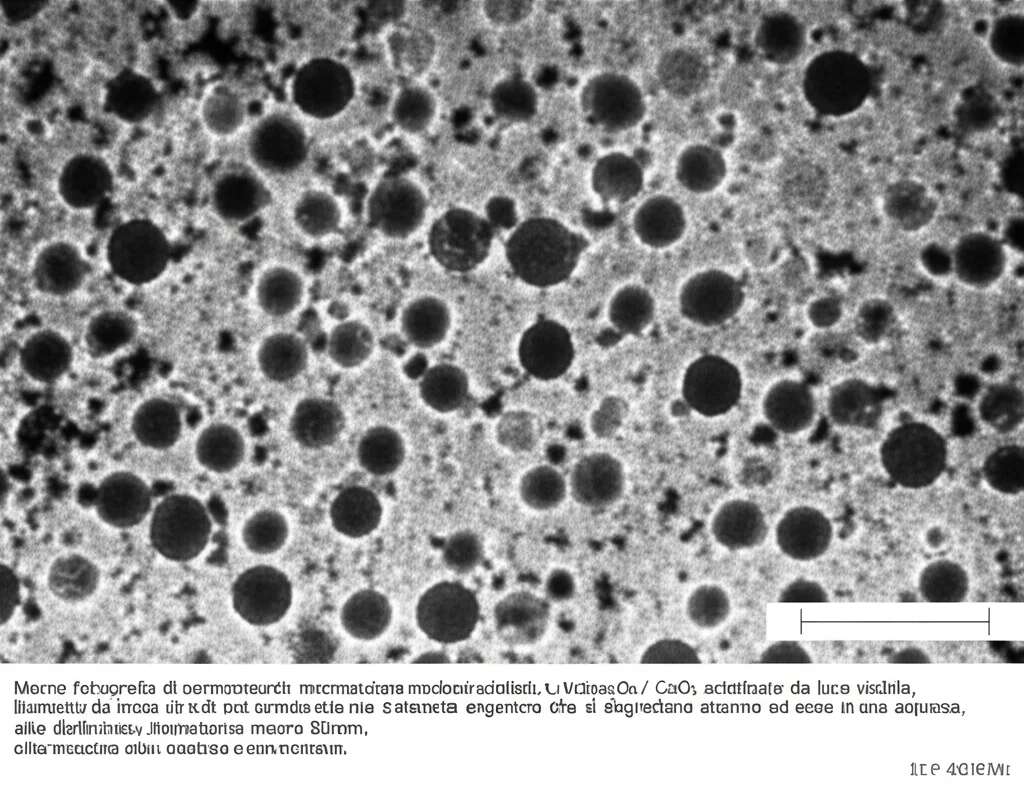
Ovviamente, non ci siamo fermati ai test di degradazione. Abbiamo analizzato a fondo il nostro campione S1. L’analisi XRD ha confermato la natura cristallina e le fasi di NiFe₂O₄ e CeO₂, con una dimensione media dei cristalliti di circa 27 nm. Le immagini FESEM e TEM hanno mostrato nanoparticelle uniformi e ben distribuite, con una dimensione media delle particelle di circa 53.77 nm, e hanno confermato la riuscita combinazione dei due ossidi. L’analisi EDS ha confermato la purezza del campione, con la presenza di Ni, Fe, O e Ce.
Le proprietà ottiche, studiate con UV-Vis-DRS, hanno rivelato un band gap di 1.73 eV, il che significa che il mio catalizzatore può assorbire efficientemente la luce visibile. E le proprietà magnetiche? L’analisi VSM ha mostrato un comportamento ferromagnetico, con una magnetizzazione di saturazione di 12.5 emu/g. Questo è fantastico perché significa che il catalizzatore può essere facilmente recuperato dall’acqua usando un semplice magnete!
Infine, l’analisi BET ha indicato che il materiale è mesoporoso con un’area superficiale specifica di 7.807 m²g⁻¹, adatta per applicazioni fotocatalitiche. E la durabilità? Il mio fotocatalizzatore ha mantenuto una buona efficienza di rimozione dell’eosina anche dopo cinque cicli di riutilizzo, dimostrando la sua stabilità.
Cosa Ci Portiamo a Casa?
Quindi, cosa abbiamo imparato da tutta questa avventura scientifica? Che abbiamo sviluppato un nuovo nanofotocatalizzatore magnetico binario NiFe₂O₄/CeO₂ super efficiente, preparato con un metodo semplice e scalabile. Questo materiale non solo sfrutta la luce visibile (quindi l’energia solare!) per degradare inquinanti organici ostici come l’eosina, ma è anche facilmente recuperabile grazie alle sue proprietà magnetiche e stabile nel tempo.
La combinazione di NiFe₂O₄ e CeO₂ crea un effetto sinergico che migliora la separazione delle cariche, riduce la ricombinazione elettrone-lacuna e aumenta i siti attivi disponibili. Credo davvero che questa ricerca possa aprire la strada allo sviluppo di nuovi materiali semiconduttori per tantissime applicazioni fotocatalitiche, contribuendo a un futuro con acque più pulite per tutti. E per me, è stata una soddisfazione enorme vedere un’idea trasformarsi in qualcosa di così promettente!
Fonte: Springer