Un Eroe Microscopico: Come un Nano-Enzima al Platino Salva i Reni dallo Stress Ossidativo
Ciao a tutti! Oggi voglio parlarvi di qualcosa di veramente affascinante che sta emergendo dal mondo della nanomedicina. Immaginate i nostri reni, organi incredibili che lavorano senza sosta per filtrare il nostro sangue. A volte, però, possono subire un duro colpo, specialmente a causa di quella che chiamiamo lesione acuta da ischemia-riperfusione (I/R). In pratica, succede quando il flusso di sangue ai reni si interrompe e poi riprende bruscamente, come può accadere durante certi interventi chirurgici o trapianti. Questo evento scatena un vero inferno a livello cellulare: una produzione eccessiva di “specie reattive dell’ossigeno” (ROS), i famosi radicali liberi, che danneggiano le cellule e causano infiammazione. È un po’ come una tempesta perfetta che può portare a un rapido declino della funzione renale, noto come insufficienza renale acuta (AKI), una condizione seria che può persino evolvere in malattia renale cronica.
Il problema è che, fino ad oggi, non avevamo armi farmacologiche davvero efficaci per contrastare questo danno. Certo, il nostro corpo ha i suoi sistemi di difesa antiossidanti, come gli enzimi SOD (superossido dismutasi) e CAT (catalasi), ma spesso non bastano o hanno dei limiti, come la scarsa stabilità o difficoltà a raggiungere il bersaglio. Ed è qui che entriamo in gioco noi, o meglio, la nanotecnologia!
La Nostra Scommessa: Il Nano-Enzima Pt/SAE
Ci siamo chiesti: e se potessimo creare un “super-enzima” artificiale, piccolissimo ma potentissimo, capace di imitare e potenziare le difese naturali del nostro corpo contro lo stress ossidativo? Così è nato il nostro progetto: abbiamo sviluppato un enzima a singolo atomo di platino ultrasmall (Pt/SAE). Cosa significa? Immaginate dei puntini di carbonio (carbon dots, CDs) incredibilmente piccoli, sulla cui superficie abbiamo ancorato singoli atomi di platino (Pt) in una configurazione specifica (chiamata Pt-N₄). Questa struttura “a singolo atomo” è il segreto della sua potenza: massimizza l’efficienza catalitica, rendendo ogni atomo di platino un guerriero contro i ROS.
Le dimensioni contano, eccome! Il nostro Pt/SAE misura appena 2-4 nanometri. Questa taglia “ultrasmall” è fondamentale perché permette al nano-enzima di viaggiare più facilmente nel corpo e accumularsi proprio lì dove serve: nei reni danneggiati.
Come Funziona Questo Super-Eroe Nano?
Il bello del Pt/SAE è la sua versatilità. Non si limita a fare una cosa sola, ma agisce su più fronti:
- Azione Antiossidante Multipla: Imita l’attività degli enzimi naturali SOD e CAT, trasformando i pericolosi anioni superossido prima in perossido di idrogeno e poi in innocua acqua e ossigeno. Ma non solo! È anche bravissimo a neutralizzare un altro radicale molto cattivo, il radicale idrossile (·OH). Praticamente, fa piazza pulita dei principali ROS.
- Blocca la “Tempesta di Morte Cellulare”: L’ischemia-riperfusione non solo genera ROS, ma innesca anche diversi programmi di morte cellulare, una sorta di “tempesta” che include processi chiamati ferroptosi e PANoptosi (un mix complesso di piroptosi, apoptosi e necroptosi). La ferroptosi è legata all’accumulo di danni ai grassi delle membrane cellulari (perossidazione lipidica), mentre la PANoptosi è spesso innescata da segnali di pericolo come il DNA mitocondriale danneggiato che assume una strana forma a “Z” (Z-DNA) e interagisce con una proteina chiamata ZBP1. Il nostro Pt/SAE, riducendo i ROS, riesce a frenare sia la perossidazione lipidica (contrastando la ferroptosi) sia la formazione di Z-DNA e la sua interazione con ZBP1 (contrastando la PANoptosi). In pratica, dice alle cellule renali: “Ehi, calma, non è ancora il momento di autodistruggersi!”.
- Spegne l’Infiammazione: Lo stress ossidativo e la morte cellulare richiamano cellule immunitarie, in particolare i macrofagi. Questi possono diventare “cattivi” (fenotipo M1 pro-infiammatorio) e peggiorare il danno. Il Pt/SAE aiuta a calmare la situazione, riducendo l’infiltrazione di cellule infiammatorie e spingendo i macrofagi verso un fenotipo “buono” (M2 anti-infiammatorio), che favorisce la riparazione del tessuto.

Dalla Provetta al Modello Vivente: Le Prove sul Campo
Ovviamente, non ci siamo fermati alle ipotesi. Abbiamo messo alla prova il nostro Pt/SAE prima in vitro, su cellule epiteliali tubulari prossimali (PTEC) di rene sottoposte a stress da ipossia/riossigenazione (H/R) per mimare l’I/R. I risultati sono stati entusiasmanti!
- Le cellule trattate con Pt/SAE sopravvivevano molto meglio allo stress H/R.
- Abbiamo visto con i nostri occhi (usando microscopi confocali e citometria a flusso) che il Pt/SAE entrava efficacemente nelle cellule, riduceva drasticamente i livelli di ROS e proteggeva i mitocondri (le centrali energetiche della cellula).
- Abbiamo confermato che il Pt/SAE riduceva significativamente i marcatori sia della ferroptosi (come la perossidazione lipidica e l’aumento di ferro libero Fe²⁺) sia della PANoptosi (come l’espressione di proteine chiave come ZBP1, caspasi attivate, GSDMD, p-RIPK3, p-MLKL e il rilascio di Z-DNA mitocondriale).
- Abbiamo anche testato la sua capacità di modulare l’infiammazione in un sistema di co-coltura, vedendo che le cellule immunitarie (macrofagi derivati da midollo osseo, BMDM) esposte a cellule PTEC danneggiate e trattate con Pt/SAE tendevano meno a polarizzarsi verso il fenotipo infiammatorio M1.

Il passo successivo era fondamentale: testare il Pt/SAE in vivo, in un modello animale (topi) di danno renale da I/R. Abbiamo iniettato il nostro nano-enzima (marcandolo con un colorante fluorescente, ICG, per seguirne il percorso) e abbiamo osservato cosa succedeva.
Risultati In Vivo: Una Conferma Promettente
Anche qui, i risultati ci hanno dato grande soddisfazione:
- Targeting Renale: Il Pt/SAE si accumulava preferenzialmente nei reni danneggiati dall’I/R e vi rimaneva a lungo (fino a 24 ore), suggerendo un effetto terapeutico mirato e prolungato.
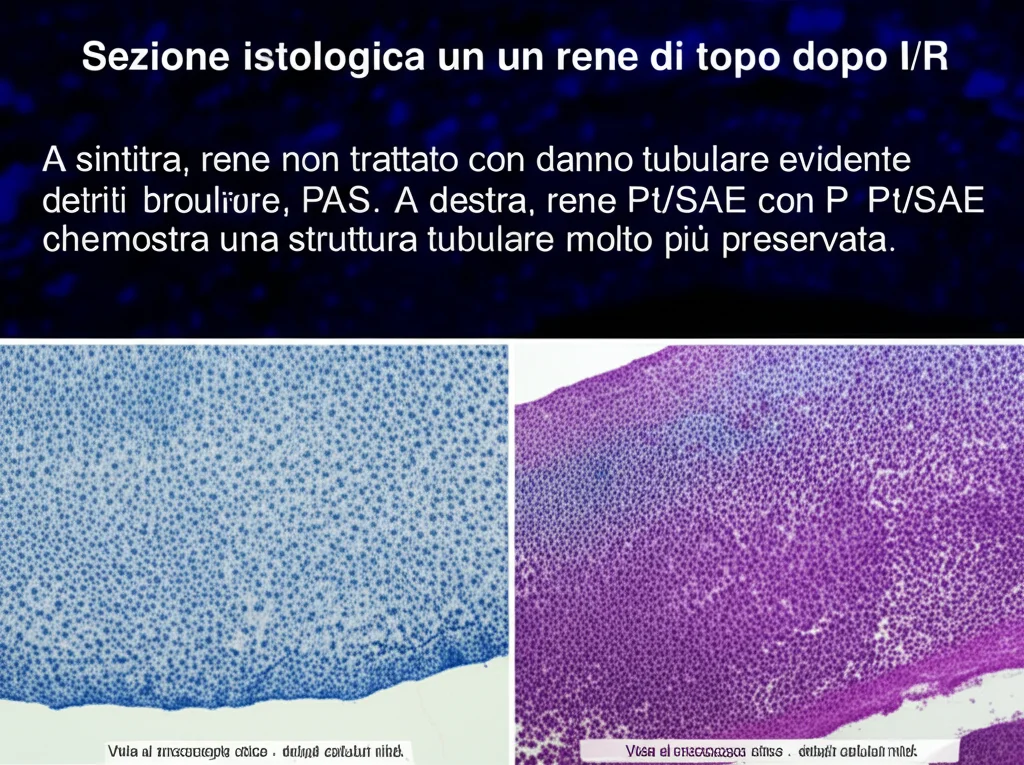
- Protezione Funzionale e Strutturale: I topi trattati con Pt/SAE mostravano un danno tubulare significativamente ridotto (valutato con colorazioni specifiche come PAS e TUNEL per l’apoptosi) rispetto ai topi non trattati. Soprattutto, la loro funzione renale era nettamente migliore, come dimostrato dai livelli più bassi nel sangue di creatinina (Scr) e azoto ureico (BUN), due indicatori chiave di salute renale. L’effetto era dose-dipendente: una dose maggiore offriva una protezione migliore.
- Conferma dei Meccanismi: Analizzando i tessuti renali, abbiamo confermato che il Pt/SAE riduceva lo stress ossidativo (meno marcatori come 4-HNE), la ferroptosi (ripristinando i livelli di proteine come GPX4 e FSP1) e la PANoptosi (riducendo ZBP1, Z-DNA citosolico e altri marcatori di morte programmata).
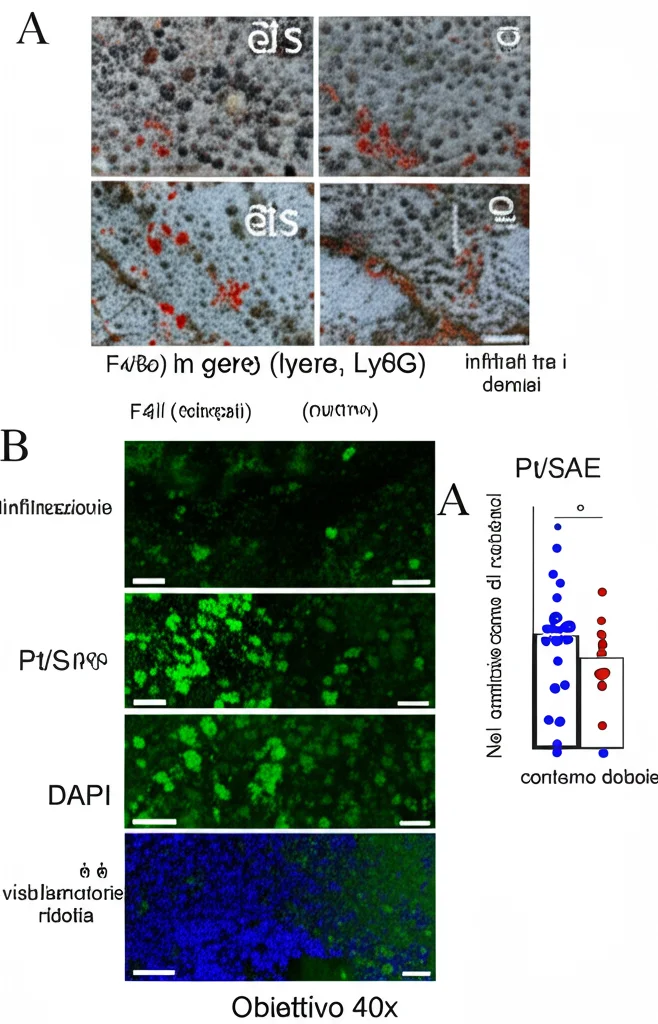
- Effetto Anti-infiammatorio: Abbiamo osservato una minore infiltrazione di cellule infiammatorie (neutrofili Ly6G+ e macrofagi F4/80+) nei reni trattati. Inoltre, l’analisi dei macrofagi presenti nel rene ha mostrato una riduzione della polarizzazione M1 (iNOS+) e livelli più bassi di citochine pro-infiammatorie come TNF-α, IL-1β e IL-6.
Sicurezza Prima di Tutto!
Un aspetto cruciale per qualsiasi potenziale terapia è la sicurezza. Abbiamo condotto test approfonditi per valutare la biocompatibilità del Pt/SAE. I risultati sono stati ottimi: il nano-enzima ha mostrato una tossicità minima sulle cellule anche a concentrazioni elevate, non ha causato emolisi (rottura dei globuli rossi), non ha alterato i parametri ematici di routine né la funzionalità di fegato e reni, e l’analisi istologica degli organi principali non ha rivelato segni di danno. Questo ci dà grande fiducia sulla sua potenziale sicurezza per future applicazioni.
Cosa Significa Tutto Questo? Prospettive Future
Questo studio, secondo me, è davvero entusiasmante perché introduce un approccio innovativo per combattere l’AKI indotta da I/R. Il nostro Pt/SAE si è dimostrato un potente spazzino di ROS, un inibitore della “tempesta di morte cellulare” (ferroptosi e PANoptosi) e un modulatore dell’infiammazione. Supera molti limiti degli antiossidanti naturali e di altri nanozimi precedentemente studiati, grazie alla sua efficienza catalitica elevata, stabilità, dimensioni ultrasmall che favoriscono l’accumulo renale e ottima biocompatibilità.
Certo, la strada verso l’applicazione clinica è ancora lunga. Serviranno ulteriori ricerche per comprendere ancora più a fondo i meccanismi molecolari e per validare questi risultati in contesti più complessi e, infine, sull’uomo. Tuttavia, crediamo che questo lavoro fornisca una solida base teorica e sperimentale per lo sviluppo di nanomateriali avanzati che potrebbero, un giorno, migliorare significativamente la vita dei pazienti affetti da insufficienza renale acuta.
È affascinante pensare come qualcosa di così piccolo, a livello atomico, possa avere un impatto così grande sulla salute di un organo complesso come il rene. Continueremo a lavorare in questa direzione, spinti dalla speranza di trasformare questa promessa scientifica in una realtà terapeutica.
Fonte: Springer