μFR Coronarico: Target o Vaso? Sveliamo il Miglior Detective per il Tuo Cuore!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona molto nel campo della cardiologia: come facciamo a capire se una stenosi, un restringimento delle nostre arterie coronarie, è davvero problematica e necessita di un intervento? È una domanda cruciale, perché riguarda la salute del nostro cuore, il motore della nostra vita.
Il Gold Standard e i suoi Limiti: FFR
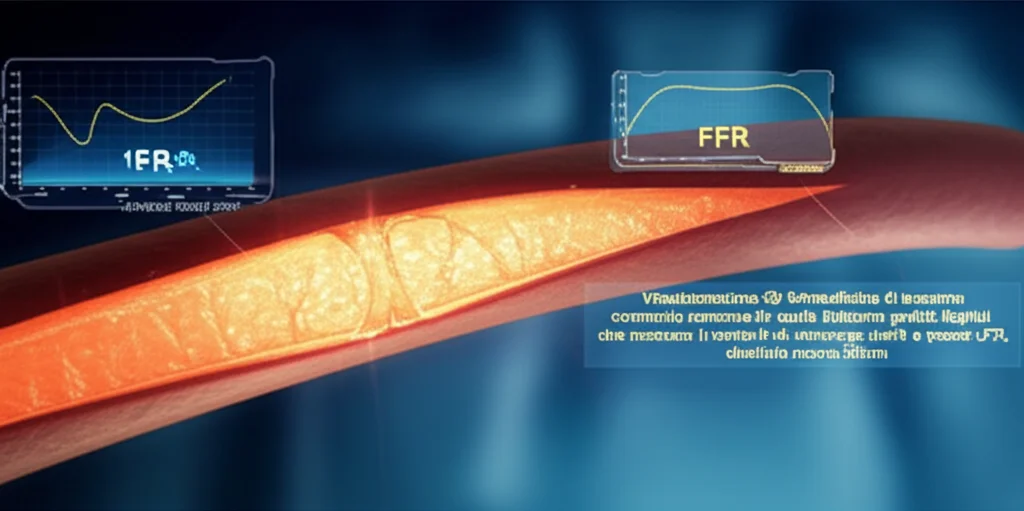
Per anni, il metodo considerato il “gold standard” per valutare la significatività funzionale di una stenosi coronarica è stata la Riserva Frazionale di Flusso (FFR). In pratica, si misura la pressione del sangue prima e dopo il restringimento durante una condizione di massimo flusso sanguigno (iperemia), indotta da farmaci. Se il rapporto tra la pressione a valle e quella a monte (FFR) è inferiore a una certa soglia (di solito 0.80), significa che la stenosi limita significativamente il flusso e potrebbe causare ischemia (mancanza di ossigeno al muscolo cardiaco).
L’FFR è fantastico, supportato da studi solidi come DEFER, FAME e FAME II, e raccomandato dalle linee guida con il massimo livello di evidenza (classe IA). Ma, diciamocelo, non è una passeggiata. Richiede una procedura invasiva, l’inserimento di un filo guida speciale dotato di sensore di pressione direttamente nell’arteria coronaria, e la somministrazione di farmaci vasodilatatori (come l’adenosina) che possono dare qualche fastidio al paziente. Inoltre, c’è un costo associato all’attrezzatura e un piccolo, ma non trascurabile, rischio di complicanze. Per questi motivi, nonostante la sua validità, l’FFR non è utilizzato così diffusamente nella pratica clinica quotidiana come forse dovrebbe.
L’Alternativa Virtuale: Arriva il QFR e il suo “Fratello” Veloce μFR
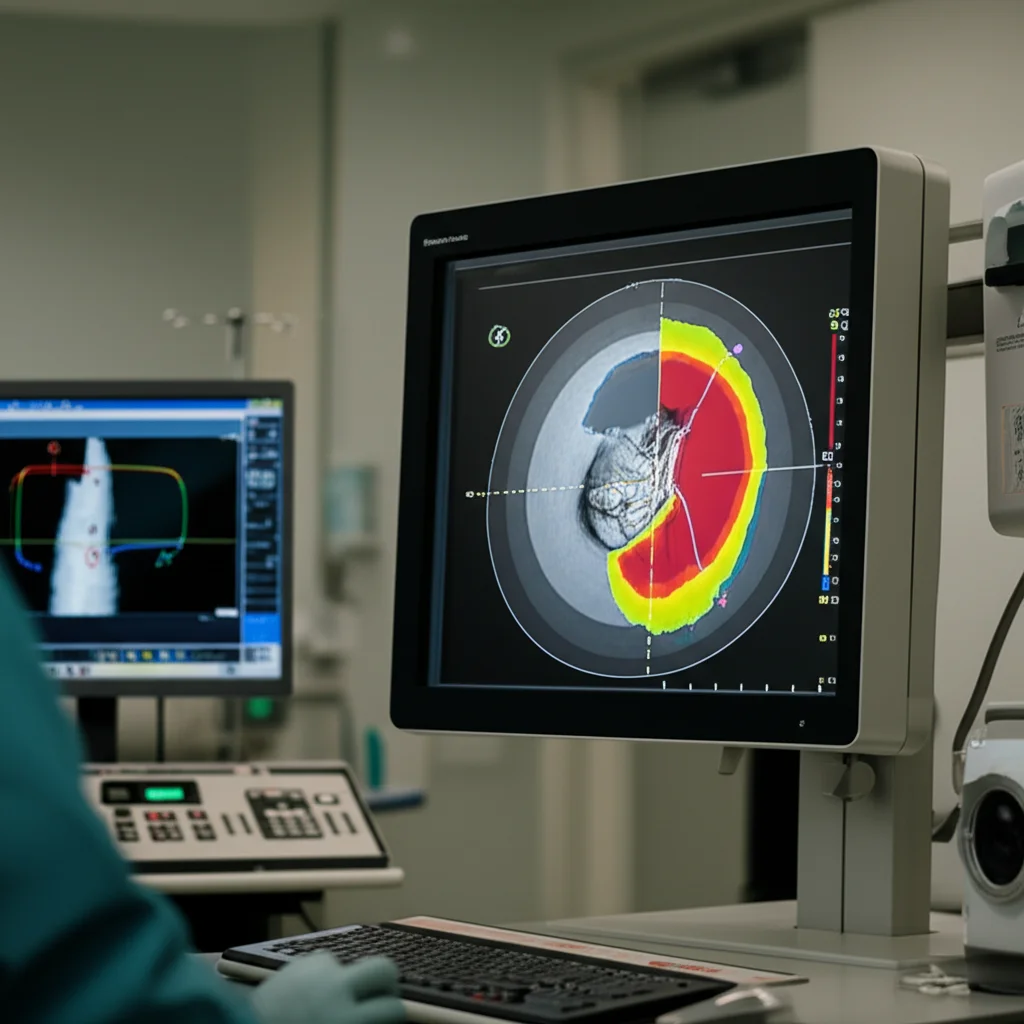
E se potessimo ottenere informazioni simili a quelle dell’FFR senza tutta quella “invasività”? Qui entra in gioco la cosiddetta FFR virtuale, calcolata a partire dalle immagini angiografiche. Una delle tecniche più promettenti è il Quantitative Flow Ratio (QFR). Il QFR stima l’FFR analizzando le immagini della coronarografia (CAG), l’esame radiologico standard che visualizza le coronarie.
Recentemente, è emersa una versione ancora più smart e veloce del QFR, chiamata μFR (QFR derivato dalla Legge di Murray). Questa tecnica innovativa utilizza algoritmi basati sull’intelligenza artificiale e la Legge di Murray (che descrive la relazione tra il diametro dei vasi sanguigni e il flusso) per calcolare l’FFR virtuale da una singola proiezione angiografica, in modo semiautomatico e molto rapido. Pensate: si parla di tempi di calcolo di 1-2 minuti, contro i 5 minuti del QFR standard e i 7 minuti (più tutta la procedura) dell’FFR invasivo!
La Domanda Cruciale: Dove Misurare? Target vs. Vessel
Ok, abbiamo questo strumento fantastico, il μFR. Ma dove esattamente dobbiamo misurare il valore lungo l’arteria? Qui nasce il dilemma che abbiamo voluto indagare nel nostro studio: è meglio misurare il μFR in una posizione specifica, circa 2-3 cm dopo la lesione target (target-μFR), imitando la posizione tipica del sensore FFR, oppure misurarlo nel punto più distale del vaso analizzato (vessel-μFR)?
Studi precedenti su altre tecniche di FFR virtuale (come il CT-FFR, derivato dalla TAC coronarica) avevano suggerito che la misurazione “target” potesse essere più accurata e clinicamente rilevante rispetto a quella “vessel”, che a volte potrebbe sovrastimare l’ischemia a causa della valutazione sull’intero vaso. Quindi, la nostra ipotesi era: forse anche per il μFR, la misurazione target è superiore?
Il Nostro Studio: Mettiamo alla Prova Target-μFR e Vessel-μFR
Per rispondere a questa domanda, abbiamo condotto uno studio retrospettivo, analizzando i dati di pazienti con malattia coronarica sospetta o nota che erano stati sottoposti sia a coronarografia che a misurazione FFR invasiva nel nostro centro tra gennaio 2021 e marzo 2023. Dopo aver applicato criteri di inclusione ed esclusione (per garantire la qualità delle immagini e l’affidabilità delle misurazioni), abbiamo incluso nell’analisi finale 137 pazienti con 146 lesioni coronariche.
Per ogni lesione, abbiamo calcolato sia il target-μFR (nel punto corrispondente alla misurazione FFR) sia il vessel-μFR (nel punto più distale del vaso), utilizzando il software dedicato basato su AI (AngioPlus Core). Ovviamente, chi calcolava i valori μFR non conosceva il risultato dell’FFR invasivo, per evitare bias. Abbiamo poi confrontato le performance diagnostiche di entrambi i metodi μFR usando l’FFR invasivo (con soglia ≤ 0.80) come nostro riferimento, il nostro “giudice” imparziale.
I Risultati: Sorprese e Conferme
Ebbene, cosa abbiamo scoperto?
- Ottima Correlazione e Accordo con FFR: Sia il target-μFR che il vessel-μFR hanno mostrato una correlazione fortissima (R rispettivamente 0.84 e 0.83) e un ottimo accordo con i valori dell’FFR invasivo. Questo conferma che il μFR, in generale, è un ottimo “simulatore” dell’FFR.
- Performance Diagnostiche Simili: Qui la sorpresa rispetto alla nostra ipotesi iniziale. Quando abbiamo valutato la capacità di predire un FFR ≤ 0.80, le performance dei due metodi sono risultate molto simili. L’area sotto la curva ROC (un indice globale di accuratezza diagnostica) era praticamente identica: 0.937 per il target-μFR e 0.936 per il vessel-μFR.
- Sensibilità e Specificità: Usando la soglia predefinita di 0.80 anche per il μFR, il target-μFR ha mostrato una sensibilità dell’86.44% e una specificità dell’88.51% (accuratezza 91.78%). Il vessel-μFR ha dimostrato una sensibilità del 92.98% e una specificità del 91.01% (accuratezza 87.67%). Anche se i numeri specifici variano leggermente, nel complesso la capacità diagnostica è risultata comparabile. Il target-μFR sembrava avere un tasso di errata classificazione leggermente inferiore (7.02% vs 13.46%), suggerendo forse una maggiore precisione complessiva nonostante una sensibilità/specificità leggermente diverse in questo set di dati.
- Affidabilità: Entrambi i metodi hanno mostrato una buona affidabilità sia intra-osservatore (lo stesso operatore che ripete la misura) che inter-osservatore (due operatori diversi).
Cosa Significa Tutto Questo?
La conclusione principale del nostro studio è che, per quanto riguarda il μFR, la scelta del punto di misurazione (target vs. vessel) sembra avere un impatto minore sull’accuratezza diagnostica complessiva rispetto a quanto ipotizzato o visto per altre tecniche. Entrambi gli approcci, target-μFR e vessel-μFR, si sono dimostrati strumenti validi e affidabili per valutare la significatività emodinamica delle stenosi coronariche, con performance molto vicine a quelle dell’FFR invasivo.
Questo è molto incoraggiante! Significa che abbiamo a disposizione uno strumento, il μFR, che non solo è veloce ed evita l’uso di fili guida e farmaci, ma è anche robusto rispetto alla precisa localizzazione della misurazione distale.
Tuttavia, un piccolo vantaggio del target-μFR potrebbe esserci: concentrandosi sulla zona immediatamente successiva alla lesione, potrebbe semplificare il processo decisionale, specialmente in casi complessi come le biforcazioni, riducendo la necessità di analizzare segmenti molto distali del vaso che potrebbero essere influenzati da altri fattori. Basandoci sulla differenza osservata nella sensibilità e nel tasso di errata classificazione, suggeriamo che scegliere un punto di misurazione μFR vicino ai 2-3 cm distali dalla lesione (come nel target-μFR) potrebbe essere leggermente preferibile per ottimizzare la strategia clinica.
Limiti e Prospettive Future
Come ogni studio, anche il nostro ha dei limiti. È retrospettivo, condotto in un singolo centro e con un numero di pazienti non enorme (anche a causa della non diffusissima adozione dell’FFR). Inoltre, abbiamo dovuto escludere alcuni casi per problemi tecnici o qualità delle immagini. Serviranno sicuramente studi più ampi, multicentrici e prospettici per confermare questi risultati e valutare l’impatto clinico a lungo termine dell’utilizzo del μFR (sia target che vessel) nelle decisioni terapeutiche. Bisognerà anche analizzare meglio l’impatto di caratteristiche anatomiche specifiche o di precedenti interventi.
In Conclusione
Il μFR si conferma come una tecnologia estremamente promettente. Sia la misurazione target che quella vessel offrono performance diagnostiche elevate e simili all’FFR invasivo, ma con i vantaggi della rapidità e della non invasività (niente filo guida, niente farmaci iperemizzanti). L’accuratezza del μFR non sembra essere pesantemente influenzata dalla scelta del punto di misurazione distale, anche se l’approccio “target” potrebbe offrire una leggera semplificazione nel processo decisionale.
Possiamo dire che abbiamo tra le mani un altro strumento computazionale potente per diagnosticare l’ischemia coronarica e aiutarci a prendere decisioni cliniche migliori per i nostri pazienti. E questo, per chi come me lavora ogni giorno con il cuore, è davvero affascinante!
Fonte: Springer