Cancro dell’Endometrio: E se un Piccolo RNA Fosse la Chiave per Fermarlo?
Ciao a tutti, appassionati di scienza e curiosi! Oggi voglio portarvi con me in un viaggio affascinante nel mondo della ricerca oncologica, un campo dove ogni piccola scoperta può accendere una grande speranza. Parleremo di un nemico subdolo, il cancro dell’endometrio, e di un potenziale, minuscolo eroe che potrebbe aiutarci a combatterlo: un microRNA chiamato miR-200b-3p.
Il Cancro dell’Endometrio: Un Nemico in Crescita
Prima di addentrarci nei meccanismi molecolari, facciamo un passo indietro. Il cancro dell’endometrio (EC) è un tumore che colpisce il rivestimento interno dell’utero. Viene spesso definito “adenocarcinoma” perché è il tipo più comune. Purtroppo, la sua incidenza è in aumento a livello globale. Se diagnosticato precocemente, le prospettive sono generalmente buone. Tuttavia, quando il gioco si fa duro, cioè quando il cancro è in stadio avanzato o recidiva, la situazione si complica parecchio e i tassi di sopravvivenza crollano drasticamente. Pensate che per le pazienti con metastasi pelviche ed extra-pelviche, la sopravvivenza a 5 anni scende rispettivamente al 69% e, purtroppo, solo al 17%. È l’unico tumore ginecologico con tassi di mortalità in aumento, il che ci spinge con urgenza a capirne meglio i meccanismi per trovare nuove strategie.
MicroRNA: I Piccoli Registi della Cellula
Ed è qui che entrano in gioco i nostri protagonisti: i microRNA (miRNA). Immaginateli come dei minuscoli interruttori molecolari, piccoli frammenti di RNA non codificante (lunghi appena 19-24 nucleotidi) che possono accendere o spegnere l’attività di altri geni. Hanno un ruolo cruciale nel regolare una miriade di processi cellulari, inclusi quelli che, se impazziscono, portano al cancro. Molti miRNA sono già stati collegati allo sviluppo del cancro dell’endometrio. Tra questi, la famiglia miR-200b ha mostrato di influenzare la progressione del cancro regolando un processo chiamato transizione epitelio-mesenchimale (EMT) – ne parleremo tra poco, promesso!
In particolare, il nostro eroe di oggi, miR-200b-3p, un membro di questa famiglia, ha già dato prova di sé in altri tipi di tumore, dimostrando di poter frenare la proliferazione, l’invasione e la migrazione delle cellule tumorali. Ma cosa fa esattamente nel cancro dell’endometrio? E come?
FOSL2: Un Attore Chiave Sotto i Riflettori
Per capirlo, dobbiamo introdurre un altro personaggio: FOSL2 (FOS-like antigen 2). FOSL2 fa parte di una famiglia di fattori di trascrizione chiamata AP-1, ed è un vero e proprio tuttofare nella cellula, implicato nella crescita, nello sviluppo e nelle risposte immunitarie, sia in condizioni normali che patologiche. Diversi studi hanno indicato che FOSL2 può essere un bersaglio dei miRNA e giocare un ruolo nella progressione dei tumori maligni, influenzando l’EMT e le metastasi.
Nonostante sapessimo già parecchio su miR-200b-3p e FOSL2 presi singolarmente in vari contesti tumorali, il loro legame specifico e il loro ruolo nel cancro dell’endometrio erano ancora un mistero. Ed è proprio questo mistero che lo studio che vi racconto oggi ha cercato di svelare. L’obiettivo? Capire come miR-200b-3p regola FOSL2 e quali effetti ha sulla proliferazione e sulla capacità delle cellule di cancro endometriale di formare metastasi.

Cosa Hanno Scoperto i Ricercatori? Un Sottile Equilibrio Sconvolto
I ricercatori hanno iniziato analizzando i livelli di miR-200b-3p e FOSL2 in linee cellulari di cancro dell’endometrio, confrontandole con cellule endometriali normali. E voilà, la prima sorpresa (o forse una conferma di un sospetto):
- L’espressione di miR-200b-3p era significativamente ridotta nelle cellule tumorali. Come se il “freno” naturale fosse meno presente.
- Al contrario, l’espressione di FOSL2 era significativamente aumentata. Come se l'”acceleratore” fosse premuto a tavoletta.
Questo squilibrio suggeriva già una potenziale relazione inversa tra i due. Utilizzando strumenti bioinformatici (come il database Starbase), hanno predetto che miR-200b-3p potesse legarsi direttamente a una regione specifica dell’RNA messaggero di FOSL2, impedendone la traduzione in proteina. E gli esperimenti di laboratorio (saggi di luciferasi duale, per i più tecnici) hanno confermato questa interazione diretta: miR-200b-3p “becca” FOSL2 e lo zittisce!
L’Effetto Domino: Proliferazione, Migrazione e Invasione
Ma cosa succede quando si altera artificialmente questo equilibrio nelle cellule tumorali? I ricercatori hanno condotto una serie di esperimenti ingegnosi, “pompando” miR-200b-3p (usando un “mimic”) o bloccandolo (usando un “inhibitor”), e facendo lo stesso con FOSL2 (sovraesprimendolo o silenziandolo).
Ecco i risultati chiave, che sembrano usciti da un thriller scientifico:
- Quando si aumentava miR-200b-3p (mimic):
- L’espressione di FOSL2 diminuiva (come previsto!).
- La proliferazione delle cellule tumorali rallentava.
- La loro capacità di migrare (muoversi) e invadere (attraversare barriere) si riduceva drasticamente.
- Quando si bloccava miR-200b-3p (inhibitor):
- L’espressione di FOSL2 aumentava.
- Le cellule tumorali proliferavano, migravano e invadevano di più. Un vero disastro!
E il colpo di scena? Gli effetti benefici dell’aumento di miR-200b-3p potevano essere annullati se si forzava la sovraespressione di FOSL2. Allo stesso modo, gli effetti negativi del blocco di miR-200b-3p potevano essere contrastati silenziando FOSL2. Questo dimostra in modo elegante che FOSL2 è un bersaglio funzionalmente importante di miR-200b-3p in questo contesto.
Il Ruolo della Transizione Epitelio-Mesenchimale (EMT)
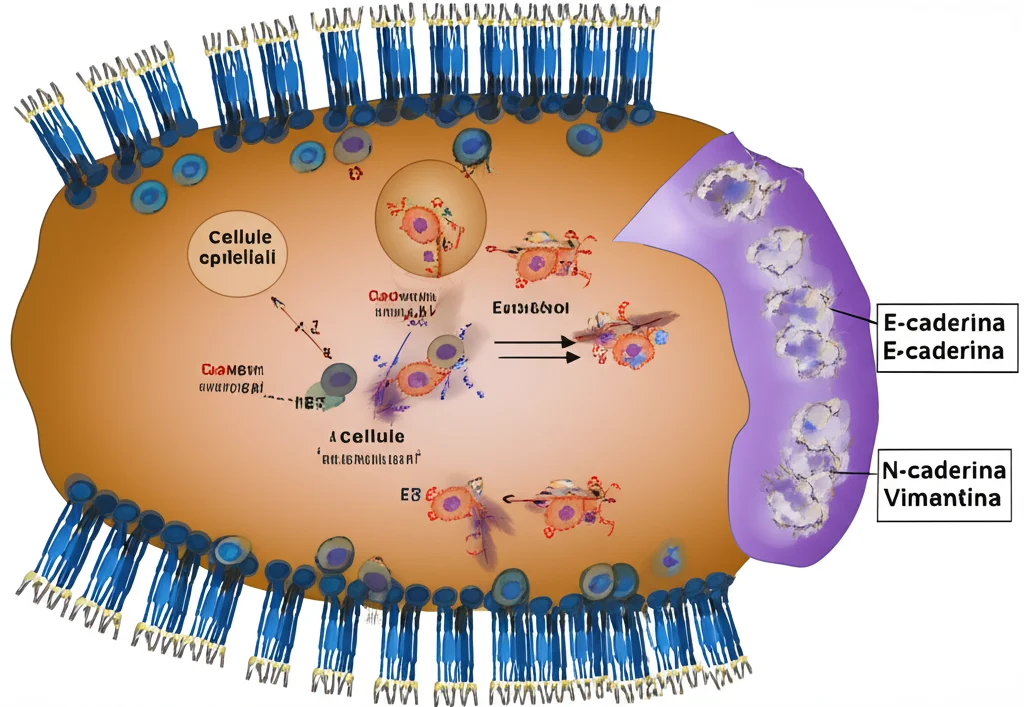
Vi avevo promesso di tornare sull’EMT. Questo è un processo cellulare affascinante e complesso. Immaginate le cellule epiteliali come mattoncini ben ordinati e coesi. Durante l’EMT, queste cellule perdono la loro “forma” e le loro connessioni, diventando più simili a cellule mesenchimali, che sono più mobili e invasive. È un po’ come se un soldato in formazione rompesse le righe per diventare un agente infiltrato. Questo processo è cruciale per lo sviluppo embrionale, ma nel cancro è una brutta notizia, perché favorisce la diffusione delle cellule tumorali e la formazione di metastasi.
L’EMT è caratterizzato da cambiamenti nell’espressione di specifiche proteine:
- E-caderina (un marcatore epiteliale, “colla” tra cellule) diminuisce.
- N-caderina e Vimentina (marcatori mesenchimali, associati a motilità) aumentano.
Nello studio, si è visto che aumentare miR-200b-3p portava a un aumento di E-caderina e a una diminuzione di N-caderina e Vimentina. In pratica, miR-200b-3p sembrava ostacolare l’EMT! E, ancora una volta, questo effetto era mediato dalla sua capacità di mettere a tacere FOSL2. Infatti, la sovraespressione di FOSL2 poteva invertire questi cambiamenti, promuovendo l’EMT.
Conferme dal Mondo Reale: Gli Studi su Modelli Animali
Tutto molto bello in provetta, direte voi, ma nel “mondo reale” di un organismo vivente? I ricercatori hanno fatto un ulteriore passo, utilizzando modelli animali (topi nude, privi di un sistema immunitario efficiente, per non rigettare le cellule tumorali umane). Hanno iniettato cellule di cancro endometriale in questi topi, alcune delle quali modificate per avere bassi livelli di FOSL2.
I risultati? I tumori derivanti da cellule con FOSL2 “silenziato” crescevano molto più lentamente e avevano un volume significativamente ridotto rispetto ai controlli. L’analisi istologica dei tessuti tumorali ha anche mostrato un maggior grado di necrosi (morte cellulare) nei tumori con FOSL2 ridotto. Questo conferma che abbassare FOSL2 inibisce la crescita tumorale anche in vivo.
Cosa Significa Tutto Questo per il Futuro?
Mettiamo insieme i pezzi del puzzle. Questo studio ci dice che nel cancro dell’endometrio, il piccolo miR-200b-3p è spesso presente in quantità ridotte. Questa carenza permette a FOSL2 di “scatenarsi”, promuovendo la proliferazione delle cellule tumorali, la loro capacità di invadere e migrare (anche attraverso il processo EMT), e quindi la progressione della malattia.
La scoperta che miR-200b-3p agisce come un soppressore tumorale bersagliando FOSL2 è importantissima. Apre la strada a nuove possibili strategie terapeutiche. Immaginate di poter “ricaricare” le cellule tumorali di miR-200b-3p, o di sviluppare farmaci che blocchino specificamente FOSL2. Potrebbe essere un modo per frenare la crescita del tumore e prevenire le metastasi.
Certo, la strada è ancora lunga. Bisognerà approfondire ulteriormente questi meccanismi, capire come miR-200b-3p e FOSL2 interagiscono con altre vie di segnale cellulare e, naturalmente, testare la sicurezza e l’efficacia di potenziali terapie basate su queste scoperte in studi clinici.
Ma ogni passo avanti nella comprensione di come funziona il cancro ci avvicina a sconfiggerlo. E la storia di miR-200b-3p e FOSL2 è un capitolo promettente in questa continua battaglia. Una piccola molecola, un grande impatto: la scienza non smette mai di stupirci!
Fonte: Springer