Occhio al Diabete: Lipidi, Proteine e i Segreti della Retinopatia Svelati dalla Genetica
Ciao a tutti! Oggi voglio portarvi con me in un viaggio affascinante nel mondo della ricerca medica, un campo dove ogni scoperta può davvero fare la differenza nella vita delle persone. Parleremo di retinopatia diabetica (DR), una delle complicanze più temute del diabete mellito e una causa principale di cecità prevenibile negli adulti. Pensate che entro il 2045 si stima che oltre 160 milioni di persone nel mondo ne soffriranno! È una sfida enorme per la salute pubblica, non trovate?
La Retinopatia Diabetica: Un Nemico Silenzioso
La DR danneggia progressivamente i piccoli vasi sanguigni della retina. Sappiamo che la glicemia alta gioca un ruolo chiave, ma c’è di più. Le differenze nei livelli di emoglobina glicata (HbA1c), il nostro indicatore del controllo glicemico a lungo termine, spiegano solo una piccola parte (circa il 6.6%) del rischio di sviluppare la DR. E allora, cos’altro entra in gioco?
Qui entrano in scena i lipidi, i grassi nel nostro sangue. La dislipidemia, cioè avere livelli anormali di lipidi, è comune nelle persone con diabete ed è stata collegata a varie complicanze, inclusa la DR. Ma stabilire un legame di causa-effetto è complicato. Gli studi epidemiologici tradizionali faticano a districare la matassa: ci sono troppi fattori confondenti (come stile di vita, altri farmaci, ecc.) e c’è sempre il rischio della “causalità inversa” (è la DR a influenzare i lipidi o viceversa?). Pensate che anche mettendo insieme pressione sanguigna, colesterolo totale e HbA1c, si spiega solo il 9% della progressione della DR! Chiaramente, ci manca qualche pezzo del puzzle.
La Rivoluzione della Metabolomica e della Mendelian Randomization
Ed è qui che la scienza moderna ci viene in aiuto con strumenti potentissimi. Avete mai sentito parlare di metabolomica? È lo studio su larga scala dei metaboliti, piccole molecole coinvolte nel nostro metabolismo. È affascinante pensare che circa il 50% della variazione dei livelli di metaboliti tra le persone sia dovuto alla genetica! Questo ci offre un’opportunità unica per capire le cause delle malattie.
Come? Attraverso una tecnica chiamata Randomizzazione Mendeliana (MR). Immaginatevela come un modo furbo per usare la genetica come una sorta di “esperimento naturale”. In pratica, usiamo le varianti genetiche che influenzano specifici fattori (come i livelli di lipidi o metaboliti) come “strumenti”. Poiché queste varianti sono assegnate casualmente alla nascita (proprio come in un esperimento randomizzato), ci aiutano a capire se quel fattore causa *davvero* una malattia, bypassando i problemi di confondimento e causalità inversa. È un approccio che sta rivoluzionando la ricerca!
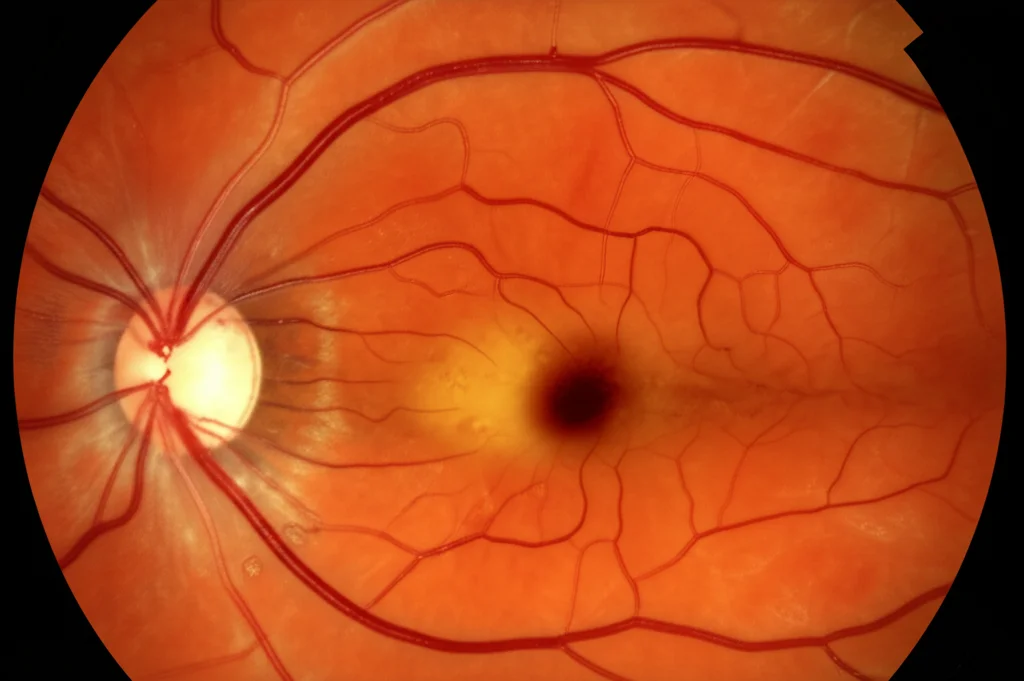
Il Nostro Studio: A Caccia di Cause e Mediatori
Nel nostro studio, ci siamo tuffati proprio in questo mondo. Volevamo capire le relazioni causali tra cinque principali lipidi (trigliceridi, colesterolo HDL e LDL, apolipoproteina A-I e B) e ben 249 metaboliti circolanti con diversi stadi della retinopatia diabetica: la DR generale, la forma iniziale (background DR), quella più severa (severe background DR) e la forma proliferativa (PDR), la più grave.
Ma non ci siamo fermati qui. Volevamo anche identificare le proteine plasmatiche che potessero fare da “mediatori” in queste relazioni causali. Trovare queste proteine significa individuare potenziali bersagli per nuove terapie. Per farlo, abbiamo usato analisi di MR su larga scala (metabolome-wide e proteome-wide) e tecniche più avanzate come la MR Multivariata (MVMR) con un approccio chiamato MR-BMA, particolarmente bravo a gestire molti fattori insieme, e la MR mediata a due passaggi (two-step MR) per scovare le proteine mediatrici. Abbiamo attinto a enormi set di dati pubblici, come quelli della UK Biobank e del consorzio FinnGen, analizzando informazioni genetiche e cliniche di centinaia di migliaia di persone.
Scoperte Chiave: Trigliceridi “Cattivi”, HDL “Buono”
Cosa abbiamo scoperto? Beh, alcune cose molto interessanti!
- I trigliceridi si sono confermati un fattore di rischio significativo. Livelli elevati aumentano causalmente il rischio di DR generale (con prove robuste), ma anche di background DR e severe background DR (con prove suggestive). È come se dessero una spinta alla malattia.
- Il colesterolo HDL (il cosiddetto “colesterolo buono”) ha mostrato un effetto protettivo, soprattutto riducendo il rischio di background DR (con prove robuste) e di severe background DR. Avere HDL alto sembra fare da scudo!
- Anche l’apolipoproteina A-I (componente principale dell’HDL) ha mostrato effetti protettivi, seppur con evidenza più suggestiva.
- Curiosamente, il colesterolo LDL (il “cattivo”) e l’apolipoproteina B (sua componente) hanno mostrato lievi effetti protettivi contro la DR generale e, nel caso dell’LDL, effetti causali suggestivi contro la PDR. Questo è un po’ controintuitivo e merita ulteriori indagini, ma sottolinea come la biologia sia complessa!
È importante dire che per alcuni di questi risultati abbiamo trovato eterogeneità o pleiotropia (cioè le varianti genetiche potrebbero influenzare la malattia anche per vie diverse dai lipidi). Abbiamo usato metodi statistici specifici (come MR-Egger e Weighted Median) per assicurarci che le nostre conclusioni fossero il più solide possibile.

Le Proteine Mediatrici: I Burattinai Molecolari
La parte forse più eccitante è stata identificare le proteine che mediano questi effetti. Per i trigliceridi, abbiamo trovato ben dieci proteine coinvolte! Tra queste spiccano:
- DKK3 (Dickkopf-3): Una proteina che modula una via di segnalazione cellulare importante (Wnt). Altri studi l’hanno trovata elevata nell’occhio di pazienti con edema maculare diabetico. Sembra che possa contribuire alla formazione di nuovi vasi anomali (neovascolarizzazione). Il nostro studio suggerisce che i trigliceridi potrebbero aumentare il rischio di DR proprio *attraverso* DKK3.
- ST4S6 (ST6 N-acetylglucosamine transferase 6): Un enzima coinvolto in modifiche molecolari.
- NEO1 (Neogenin 1): Un recettore importante per la guida degli assoni nervosi, ma coinvolto anche in altri processi.
Abbiamo anche visto che alcune di queste proteine interagiscono tra loro, suggerendo una rete complessa.
Per l’effetto protettivo dell’HDL sulla background DR, abbiamo identificato la proteina RPN1 (Ribophorin I) come mediatore significativo.
Non Solo Lipidi Principali: Il Ruolo dei Metaboliti Specifici
Andando più a fondo con i 249 metaboliti, abbiamo trovato altri legami causali affascinanti:
- Alcune particelle di lipoproteine molto piccole (very small VLDL) e alcune particelle LDL sono risultate protettive contro la DR generale. Questo è interessante perché spesso le VLDL sono viste come “cattive”. La loro protezione sembra mediata da proteine come CLIC5 (Chloride Intracellular Channel 5) e BCAM (Basal Cell Adhesion Molecule). CLIC5, peraltro, è risultato ridotto in pazienti con nefropatia diabetica, suggerendo un ruolo protettivo più ampio.
- Per la background DR, un rapporto specifico (fosfolipidi/lipidi totali) nelle particelle LDL grandi è emerso come fattore di rischio causale. L’effetto sembra mediato dalla proteina NAD(P)H deidrogenasi, un enzima chiave nel bilancio energetico e nello stress ossidativo della cellula, processi notoriamente alterati nel diabete.
- Per la PDR (la forma più grave), abbiamo trovato che livelli più alti di acidi grassi polinsaturi (PUFA) e di coline totali sono protettivi. Questo è in linea con l’idea generale che i PUFA (come gli omega-3 e omega-6) siano benefici. La cosa nuova è che abbiamo identificato proteine che mediano questa protezione: RFNG (Radical Fringe Gene) e PDE4D. RFNG è coinvolta nella via di segnalazione Notch, importante per lo sviluppo e forse per la neurogenesi nella retina.

Cosa Significa Tutto Questo?
Questi risultati sono entusiasmanti! Per la prima volta, grazie alla Randomizzazione Mendeliana applicata a dati metabolomici e proteomici, stiamo iniziando a stabilire dei legami causali diretti tra specifici lipidi, metaboliti e proteine e i diversi stadi della retinopatia diabetica. Non si tratta più solo di associazioni osservate, ma di vere e proprie catene di causa-effetto a livello molecolare.
Questo ci aiuta a capire molto meglio *perché* e *come* le alterazioni metaboliche nel diabete portano al danno retinico. E, cosa forse ancora più importante, le proteine mediatrici che abbiamo identificato (DKK3, RPN1, CLIC5, BCAM, NAD(P)H deidrogenasi, RFNG, PDE4D e le altre) diventano potenziali bersagli per nuove terapie. Immaginate farmaci che possano modulare specificamente l’attività di queste proteine per prevenire o rallentare la progressione della DR!
Un Passo Avanti, Ma la Strada è Ancora Lunga
Ovviamente, come in ogni ricerca, ci sono delle limitazioni. La MR si basa su assunzioni che potrebbero non essere sempre perfettamente soddisfatte (come l’assenza di pleiotropia). I nostri dati provengono principalmente da popolazioni europee, quindi dobbiamo verificare se i risultati valgono anche per altri gruppi etnici. Inoltre, misurare i lipidi nel sangue potrebbe non riflettere perfettamente cosa succede dentro la retina. E, naturalmente, questi risultati ottenuti con analisi statistiche su grandi numeri dovranno essere confermati con studi sperimentali in laboratorio per capire i meccanismi biologici nel dettaglio.
In Conclusione: Nuove Speranze all’Orizzonte
Nonostante le cautele, credo che questo studio rappresenti un passo avanti significativo. Abbiamo usato tecniche all’avanguardia per svelare la complessa danza tra lipidi, metaboliti e proteine nella retinopatia diabetica. Abbiamo identificato:
- I trigliceridi come fattore di rischio causale per la DR, mediato da DKK3, ST4S6, NEO1.
- L’HDL come fattore protettivo per la background DR, mediato da RPN1.
- Specifiche particelle VLDL protettive contro la DR, mediate da CLIC5 e BCAM.
- Un rapporto lipidico nelle LDL grandi come rischio per la background DR, mediato da NAD(P)H deidrogenasi.
- PUFA e coline come protettori contro la PDR, mediati da RFNG e PDE4D.
Queste scoperte non solo migliorano la nostra comprensione della malattia, ma aprono anche nuove strade promettenti per lo sviluppo di terapie mirate. La ricerca continua, e ogni pezzo del puzzle che aggiungiamo ci avvicina a combattere più efficacemente la retinopatia diabetica e a preservare la vista di milioni di persone.
Fonte: Springer