Jejumide: Il Depsipeptide Marino che Sfida le Regole e Combatte l’Infiammazione!
Ciao a tutti! Oggi voglio raccontarvi un’avventura scientifica che ci ha portati nelle profondità marine, non fisicamente, ma attraverso l’analisi del DNA di un microrganismo affascinante. Parliamo di batteri, in particolare del genere Streptomyces, veri campioni nella produzione di molecole bioattive che hanno rivoluzionato la medicina. Pensate, quasi la metà dei prodotti naturali batterici noti proviene da loro! E una buona fetta di questi sono peptidi non ribosomiali (NRP), molecole complesse assemblate da macchinari cellulari specializzati chiamati NRPS (Non-Ribosomal Peptide Synthetase).
L’Universo Nascosto degli Streptomyces Marini
Da sempre, noi ricercatori siamo affascinati dagli Streptomyces terrestri, ma negli ultimi anni l’attenzione si è spostata verso i loro cugini marini. L’oceano copre il 70% del pianeta ed è un ambiente estremo, il che spinge i microrganismi che lo abitano a sviluppare strategie di sopravvivenza uniche, spesso producendo molecole con strutture e attività biologiche mai viste prima. Tra queste, gli NRP sono particolarmente interessanti. Solitamente, le NRPS funzionano come catene di montaggio: ogni modulo aggiunge uno specifico “mattone” (amminoacido) alla catena in crescita, e l’ordine dei moduli detta la sequenza del peptide finale. Ma la natura ama la complessità, e sempre più spesso ci imbattiamo in NRPS “non canoniche”, che non seguono queste regole lineari, creando strutture peptidiche intricate e inaspettate. Il problema è che spesso troviamo il gene, ma non la molecola corrispondente, o viceversa. Capire come funzionano queste NRPS non canoniche è una sfida entusiasmante, perché potrebbe aprirci le porte a nuove classi di farmaci.
La Caccia al Tesoro nel Genoma di SNJ102
La nostra storia inizia con un ceppo batterico isolato dai sedimenti marini profondi (108 metri!) al largo dell’isola di Jeju, in Corea del Sud: Streptomyces sp. SNJ102. Analizzando il suo genoma con strumenti bioinformatici come antiSMASH, abbiamo setacciato i suoi “pacchetti di geni” per la biosintesi di metaboliti secondari (BGC – Biosynthetic Gene Cluster). Ne abbiamo trovati ben 31! Tra questi, la nostra attenzione è caduta su un BGC, denominato BGC 24, che sembrava codificare per una NRPS decisamente strana. Non aveva la classica struttura modulare completa; presentava domini isolati o moduli incompleti. Era chiaramente una NRPS non canonica, e le analisi preliminari suggerivano potesse produrre un depsipeptide. I depsipeptidi sono una classe particolare di NRP in cui uno o più legami peptidici sono sostituiti da legami esterei. Sono noti per avere attività antitumorali, antinfiammatorie e antimicrobiche. Curiosamente, mentre i funghi sono grandi produttori di depsipeptidi ciclici, spesso con strutture simmetriche, quelli prodotti dagli Streptomyces sono solitamente più complessi, asimmetrici e con il legame estereo formato in modo diverso. Il BGC 24 sembrava un ibrido, qualcosa di nuovo. La sfida era chiara: riuscire a far produrre la molecola a questo batterio (o a un altro) per poterla studiare.

Dare Vita alla Molecola: L’Espressione Eterologa
Spesso, i geni per metaboliti secondari sono “silenti” in condizioni di laboratorio, oppure il batterio originale è difficile da coltivare o manipolare geneticamente. Per superare questo ostacolo, abbiamo deciso di usare una tecnica chiamata espressione eterologa: in pratica, prendiamo il BGC dal batterio originale e lo inseriamo in un batterio “ospite” più facile da gestire, sperando che quest’ultimo produca la molecola per noi. Per prima cosa, dovevamo “catturare” il BGC 24 dal genoma di SNJ102. Abbiamo utilizzato una tecnica sofisticata chiamata Transformation-Associated Recombination (TAR) cloning nel lievito Saccharomyces cerevisiae. Abbiamo costruito una libreria BAC (Cromosoma Artificiale Batterico) del genoma di SNJ102, identificato il clone BAC contenente il nostro BGC, e poi usato il lievito per “ritagliare” precisamente il BGC e inserirlo in un vettore plasmidico (pCB_Apr) che potesse poi essere trasferito in altri batteri. Il plasmide risultante, pCB_102DP, conteneva l’intero BGC 24. Ora dovevamo scegliere l’ospite giusto. La scelta dell’ospite è cruciale: non tutti gli Streptomyces sono ugualmente bravi a esprimere geni estranei. Abbiamo provato tre ceppi diversi: Streptomyces albus J1074, Streptomyces venezuelae YJ028 e Streptomyces roseosporus NRRL 11379. Abbiamo trasferito il plasmide pCB_102DP in ciascuno di essi tramite coniugazione. I risultati sono stati netti: S. roseosporus non esprimeva quasi nulla, S. venezuelae esprimeva solo una parte dei geni, mentre S. albus J1074 si è rivelato l’ospite perfetto, esprimendo tutti i geni biosintetici chiave del BGC 24 in diverse condizioni di coltura. Analizzando gli estratti delle colture di S. albus contenente il nostro BGC con la cromatografia liquida accoppiata alla spettrometria di massa (LC-MS), abbiamo avuto la conferma: c’era un nuovo composto, assente nel ceppo di controllo! Ce l’avevamo fatta!
Svelare l’Identità: Ecco Jejumide!
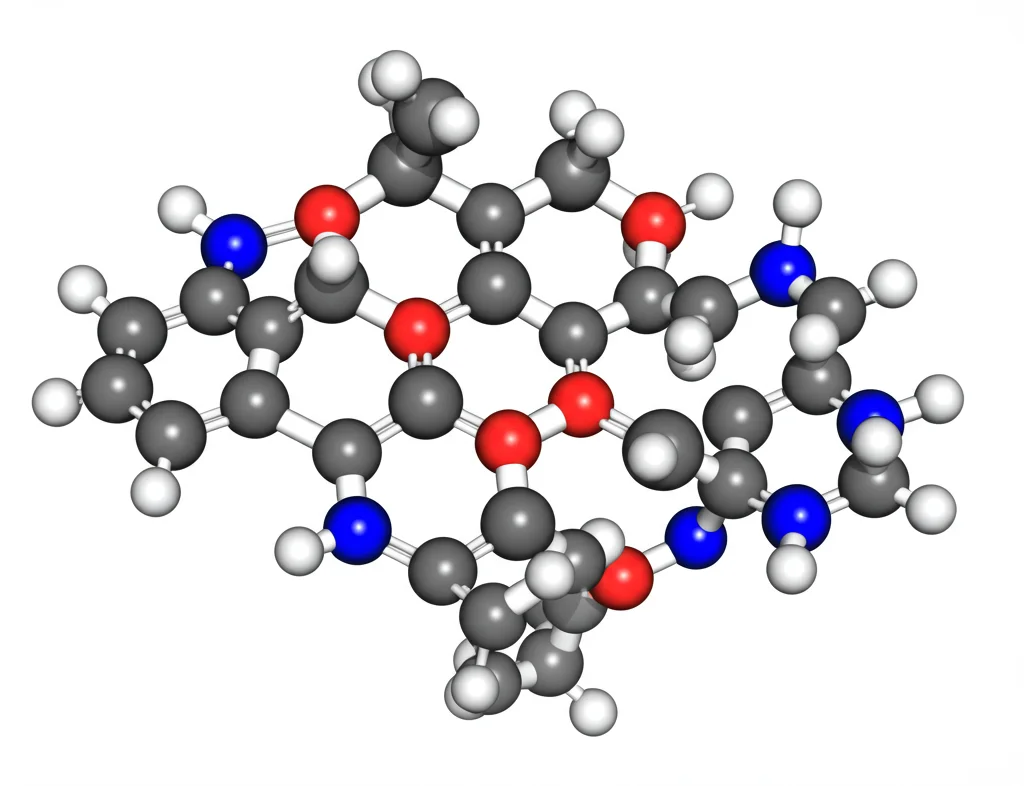
A questo punto, dovevamo capire cosa fosse esattamente questo nuovo composto. Abbiamo coltivato S. albus::pCB_102DP su larga scala (ben 30 litri!) per ottenere una quantità sufficiente di molecola pura. Dopo un lungo processo di estrazione e purificazione cromatografica, abbiamo isolato 0.7 mg di un composto incolore, che abbiamo chiamato Jejumide (composto 1), in onore del luogo di origine del batterio SNJ102. Per determinarne la struttura, abbiamo usato la spettrometria di massa ad alta risoluzione (HR-ESI-MS) e la spettroscopia di risonanza magnetica nucleare (NMR). L’HR-MS ci ha dato la formula molecolare: C22H40N2O7. L’analisi NMR (1H, 13C, COSY, HSQC, HMBC) è stata come risolvere un puzzle complesso. Abbiamo identificato i vari “pezzi” della molecola: quattro gruppi carbonilici, due metini legati all’ossigeno (indicativi di idrossiacidi), due metini legati all’azoto (tipici degli amminoacidi), e vari altri gruppi metinici, metilenici e metilici. Mettendo insieme tutti i dati, abbiamo ricostruito la struttura: Jejumide è un depsipeptide lineare composto da quattro unità: Acido D-leucico, D-Valina, L-Idrossiisovalerato (L-Hiv) e L-Leucina. La determinazione della configurazione assoluta (D o L) di ciascun centro chirale è stata fatta usando il metodo di Marfey, che prevede la derivatizzazione degli amminoacidi/idrossiacidi ottenuti dopo idrolisi acida del depsipeptide e l’analisi LC-MS. La cosa sorprendente? La struttura di Jejumide, in particolare la sequenza e il tipo di legami, assomigliava più alla forma monomerica di depsipeptidi ciclici prodotti da funghi (come la bassianolide) che ai depsipeptidi tipicamente isolati da altri Streptomyces! Questa scoperta suggerisce una possibile convergenza evolutiva o forse un trasferimento genico orizzontale tra batteri e funghi, un’ipotesi affascinante che merita ulteriori indagini.
Jejumide in Azione: Un Potenziale Antinfiammatorio
Molti depsipeptidi fungini simili strutturalmente a Jejumide, come la beauvericina e la bassianolide, hanno attività antibatterica. Abbiamo quindi testato Jejumide contro batteri Gram-negativi come E. coli e Pseudomonas putida. Sorprendentemente, Jejumide non ha mostrato alcuna attività antibatterica significativa. Forse la sua struttura lineare, rispetto a quella ciclica dei suoi analoghi fungini, ne influenza l’attività? Non ci siamo persi d’animo e abbiamo esplorato altre possibili attività biologiche. Abbiamo testato Jejumide per la sua capacità di modulare la risposta infiammatoria in cellule immunitarie murine (macrofagi RAW264.7) stimulate con lipopolisaccaride (LPS), una molecola che mima un’infezione batterica e scatena una forte infiammazione. Per prima cosa, abbiamo verificato che Jejumide non fosse tossico per le cellule alle concentrazioni testate (fino a 100 µmol/L). Poi, abbiamo misurato la produzione di ossido nitrico (NO), un mediatore chiave dell’infiammazione prodotto dall’enzima iNOS (ossido nitrico sintasi inducibile). L’LPS aumentava notevolmente la produzione di NO, ma il pre-trattamento con Jejumide, specialmente alla concentrazione più alta (100 µmol/L), riduceva significativamente i livelli di NO (una riduzione di circa 2.5 volte). Incoraggiati da questo risultato, siamo andati a vedere l’effetto di Jejumide sull’espressione delle proteine responsabili della produzione di NO e di altri mediatori infiammatori: iNOS e COX-2 (cicloossigenasi-2). L’LPS induceva fortemente l’espressione di entrambe le proteine. Il trattamento con Jejumide a 100 µmol/L inibiva in modo significativo l’espressione sia di iNOS che di COX-2 indotta da LPS. Questi risultati sono molto promettenti: Jejumide possiede un’attività antinfiammatoria agendo sulla via di segnalazione indotta da LPS, riducendo la produzione di mediatori chiave dell’infiammazione.
Il Mistero della Sintesi e Forme Dimeriche
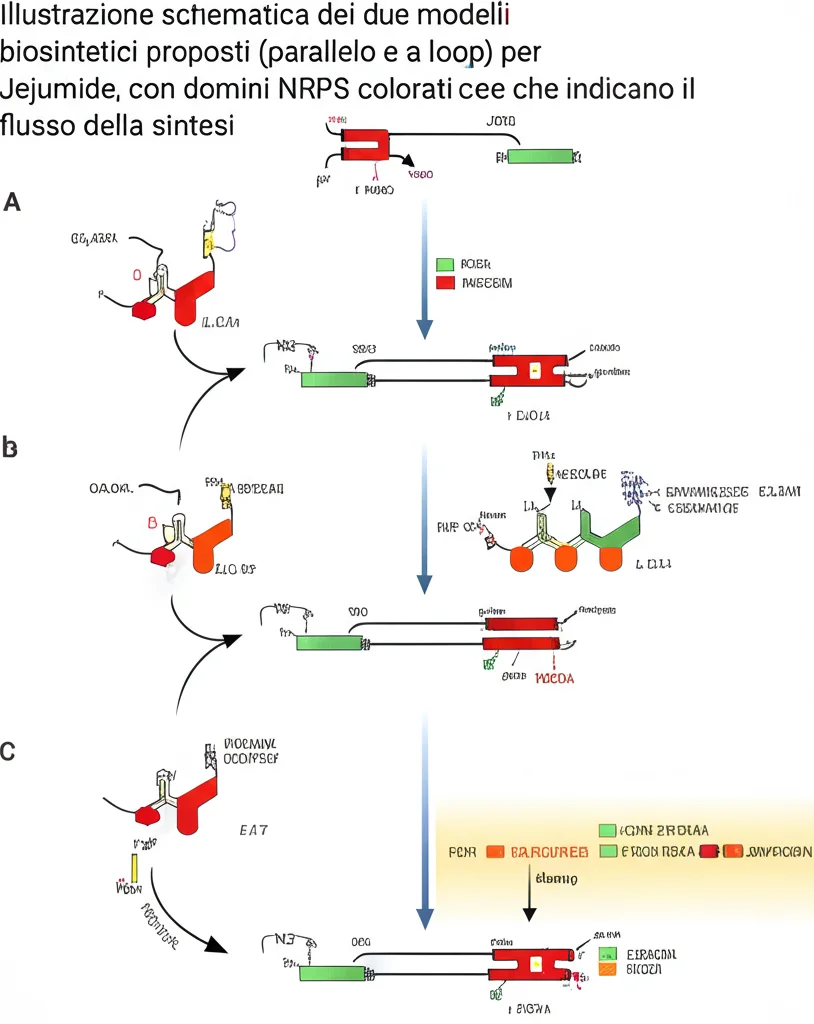
Come viene assemblato Jejumide da quella strana NRPS non canonica? Questa è la domanda da un milione di dollari! Basandoci sui modelli proposti per la biosintesi di depsipeptidi fungini simili, abbiamo ipotizzato due possibili meccanismi “iterativi”: un modello “parallelo” e un modello “a loop”. Entrambi coinvolgono i diversi domini della NRPS (A per attivare i precursori, PCP per trasportarli, C per formare i legami peptidici o esterei), ma differiscono nel modo in cui la catena peptidica viene allungata e trasferita tra i moduli. La presenza di un dominio TE (Tioesterasi) alla fine della NRPS di Jejumide suggerisce che sia responsabile del rilascio della molecola lineare, a differenza di molti depsipeptidi fungini che vengono rilasciati in forma ciclica da un dominio C terminale. Chiarire l’esatto meccanismo richiederà studi più approfonditi, magari con esperimenti in vitro usando le proteine purificate. Un’altra scoperta intrigante è stata la rilevazione, tramite LC-MS ad alta risoluzione, di tracce di composti con masse corrispondenti a dimeri di Jejumide (cioè, due molecole di Jejumide legate insieme). Abbiamo trovato due picchi distinti con la stessa massa, suggerendo la possibile presenza sia di un dimero lineare che di uno ciclico, analogamente a quanto osservato per alcuni depsipeptidi fungini. Purtroppo, le quantità erano troppo piccole per isolarli e caratterizzarli completamente, ma apre un’altra affascinante linea di ricerca.
Conclusioni e Prospettive Future
La scoperta di Jejumide è un esempio perfetto di come l’esplorazione del genoma di microrganismi marini, combinata con tecniche di espressione eterologa, possa portare alla luce nuove molecole bioattive con strutture inaspettate. Il fatto che un batterio Streptomyces produca un depsipeptide strutturalmente più simile a quelli fungini solleva domande interessanti sull’evoluzione e la diversità chimica nel mondo microbico. Inoltre, l’attività antinfiammatoria di Jejumide, dimostrata dalla sua capacità di inibire iNOS e COX-2, lo rende un candidato interessante per ulteriori studi preclinici come potenziale agente terapeutico. Questa ricerca non solo arricchisce il nostro arsenale di prodotti naturali, ma ci aiuta anche a decifrare i complessi meccanismi delle NRPS non canoniche, aprendo la strada allo sviluppo di nuovi strumenti di biologia sintetica e all’ingegneria di nuove molecole bioattive. C’è ancora tanto da scoprire negli oceani e nel genoma dei loro abitanti!
Fonte: Springer