Interleuchina-37: Un Possibile Scudo Contro i Danni della Parodontite?
Ciao a tutti! Oggi voglio parlarvi di qualcosa di veramente affascinante che sta emergendo nel campo della ricerca sulla salute delle nostre gengive. Immaginate il nostro corpo come un campo di battaglia incredibilmente complesso, dove ogni giorno si combattono guerre silenziose contro invasori microscopici. Una di queste battaglie si svolge proprio nella nostra bocca e riguarda la parodontite, una malattia infiammatoria cronica che, se non controllata, può portare alla perdita dei denti. Ma cosa scatena questa guerra e, soprattutto, abbiamo delle armi segrete per difenderci?
La Parodontite: Quando l’Equilibrio si Rompe
La parodontite non è semplicemente un’infiammazione delle gengive; è una condizione molto più seria che colpisce le strutture di supporto dei denti. Tutto inizia con un cambiamento nell’ecosistema microbico della nostra bocca, il famoso biofilm subgengivale. Quando questo delicato equilibrio si altera (un fenomeno chiamato disbiosi), alcuni batteri “cattivi” prendono il sopravvento. Questi microrganismi non solo sono più aggressivi, ma sono anche maestri nel manipolare la nostra risposta immunitaria, promuovendo un’infiammazione cronica che, invece di risolvere il problema, finisce per danneggiare i nostri stessi tessuti [4].
Il nostro sistema immunitario riconosce componenti specifici di questi batteri, come il famigerato lipopolisaccaride (LPS), considerato un “pattern molecolare associato ai patogeni” (PAMP). Questo riconoscimento attiva una cascata di segnali che porta alla produzione di citochine pro-infiammatorie e di enzimi particolari chiamati MetalloProteinasi di Matrice (MMP) [5,6].
MMP-9: L’Enzima “Demolitore”
Tra le varie MMP, una in particolare gioca un ruolo da protagonista nella parodontite: la MMP-9 (o Gelatinasi B). Questo enzima è un vero e proprio “demolitore” della matrice extracellulare, la struttura che tiene insieme i nostri tessuti, compresi quelli che sostengono i denti [7]. La MMP-9 è prodotta da diverse cellule, incluse le nostre stesse cellule epiteliali gengivali, quelle che formano la prima linea di difesa della gengiva. Livelli elevati di MMP-9 sono spesso associati a una maggiore gravità della parodontite, perché questo enzima non solo degrada direttamente il collagene e altre proteine strutturali, ma può anche attivare altre molecole infiammatorie, amplificando il danno [8,9]. In studi precedenti, abbiamo visto una chiara associazione tra le forme attive e inattive di MMP-9 e la progressione della malattia [10].
Le cellule epiteliali gengivali, quindi, non sono solo una barriera fisica, ma partecipano attivamente alla risposta immunitaria, rispondendo agli stimoli batterici (come l’LPS, riconosciuto dal recettore TLR-4 sulla loro superficie) e rilasciando molecole come la MMP-9 [11,12,13,14].

Entra in Scena l’Interleuchina-37 (IL-37): Un Possibile Pacificatore?
Qui le cose si fanno interessanti. Nella grande famiglia delle citochine Interleuchina-1 (IL-1), che solitamente sono associate all’infiammazione [15,16,17], c’è un membro relativamente nuovo e un po’ “controcorrente”: l’Interleuchina-37 (IL-37). A differenza delle sue “cugine”, l’IL-37 è riconosciuta per avere un ruolo soppressivo sull’infiammazione innata [18,19]. È stata trovata in diversi tessuti umani, ma i suoi livelli sembrano aumentare significativamente proprio in risposta a stimoli infiammatori come i PAMP [20,21,22].
Cosa c’entra l’IL-37 con la parodontite? Gli studi finora sono limitati e con risultati a volte contrastanti. Alcuni hanno trovato livelli più alti di IL-37 nei tessuti gengivali di pazienti con parodontite [23], mentre altri hanno riportato una diminuzione nel fluido gengivale crevicolare [24]. C’era quindi bisogno di capire meglio il suo ruolo funzionale, specialmente in relazione alle cellule epiteliali gengivali e alla produzione di MMP-9.
La Nostra Indagine: Cosa Abbiamo Scoperto?
Nel nostro studio, abbiamo voluto investigare due aspetti principali:
- Come cambia l’espressione di IL-37 nei tessuti gengivali passando da uno stato sano a uno di parodontite?
- L’IL-37 può influenzare la produzione di MMP-9 da parte delle cellule epiteliali gengivali quando queste sono “provocate” dal batterico LPS?
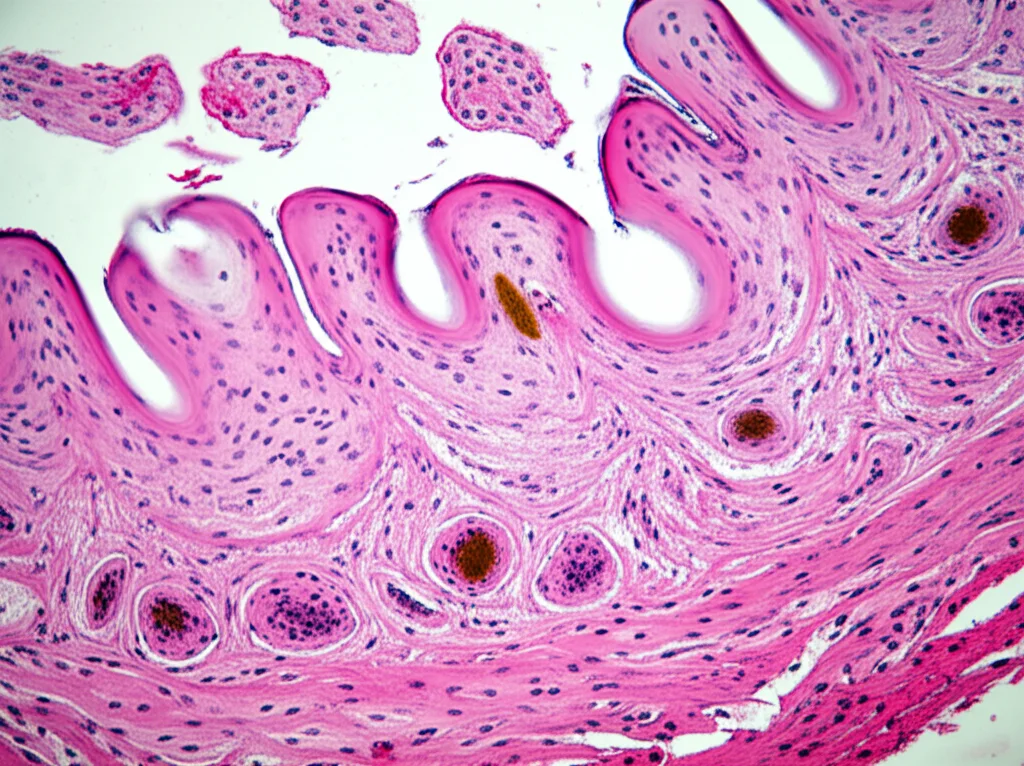
Per rispondere alla prima domanda, abbiamo analizzato campioni di tessuto gengivale di pazienti con parodontite e di controlli sani tramite immunoistochimica. I risultati sono stati chiari: nei tessuti affetti da parodontite, l’espressione di IL-37 era significativamente più alta, sia nelle cellule epiteliali (soprattutto nello strato basale) sia, in modo ancora più marcato, nel tessuto connettivo sottostante, dove si trovano cellule immunitarie migrate, fibroblasti e cellule endoteliali [Fig.1]. Questo suggerisce che l’organismo, di fronte all’attacco batterico e all’infiammazione cronica, cerca di “alzare le difese” anti-infiammatorie producendo più IL-37.
Per la seconda domanda, siamo passati a esperimenti in vitro usando colture di cellule epiteliali gengivali umane. Abbiamo stimolato queste cellule con LPS (per mimare l’attacco batterico) e abbiamo misurato i livelli di IL-37 e MMP-9 prodotti.
Prima scoperta interessante: le cellule stimolate con LPS producevano significativamente più IL-37 rispetto a quelle non stimolate [Fig.2]. Sembra quasi che le cellule, sentendosi attaccate, chiamino a raccolta questo “pompiere” molecolare.
Seconda scoperta, come previsto: la stimolazione con LPS aumentava notevolmente la produzione di MMP-9, sia a livello di gene (mRNA misurato con qPCR) che di proteina (misurata con ELISA) [Fig.3, Fig.4]. Questo conferma il ruolo dell’LPS nell’indurre questo enzima dannoso.

Ma ecco il punto cruciale: cosa succedeva se stimolavamo le cellule con LPS e contemporaneamente aggiungevamo IL-37? I risultati sono stati entusiasmanti! La co-stimolazione con IL-37 riduceva in modo marcato l’aumento di MMP-9 indotto dall’LPS, sia a livello di mRNA che di proteina [Fig.3, Fig.4]. In pratica, l’IL-37 sembrava mettere un freno alla produzione dell’enzima “demolitore” scatenata dall’infiammazione batterica. È importante notare che l’IL-37 da sola non aumentava i livelli di MMP-9, anzi, li manteneva bassi come nelle cellule non stimolate.
Cosa Significa Tutto Questo?
Questi risultati ci dicono che le cellule epiteliali gengivali non sono solo vittime passive dell’infiammazione, ma attori che cercano di modulare la risposta. Producono MMP-9 sotto attacco batterico (contribuendo potenzialmente al danno), ma producono anche IL-37, che sembra avere la capacità di controbilanciare questo effetto dannoso, almeno in parte. L’aumento di IL-37 osservato nei tessuti malati potrebbe quindi rappresentare un tentativo, forse insufficiente nelle fasi avanzate della malattia, di limitare la distruzione tissutale.
L’IL-37 emerge come una molecola con un potenziale ruolo protettivo nel microambiente gengivale. La sua capacità di sopprimere la produzione di MMP-9 indotta da LPS nelle cellule epiteliali gengivali è un meccanismo affascinante. Questo apre scenari interessanti: potrebbe l’IL-37, o molecole che ne mimano l’azione, diventare un giorno un’opzione terapeutica per aiutare a controllare l’infiammazione e la distruzione tissutale nella parodontite?

Certo, la biologia della parodontite è complessa. Ci sono molti altri attori in gioco, come gli inibitori naturali delle MMP (i TIMP) [49] e altre citochine anti-infiammatorie come l’IL-10 [50]. Inoltre, bisogna considerare il ruolo dei peptidi antimicrobici (AMPs) che pure modulano l’immunità orale [31,32]. Il modo esatto in cui l’IL-37 interagisce con tutte queste componenti richiede ulteriori indagini.
Tuttavia, il nostro studio aggiunge un tassello importante alla comprensione dei meccanismi di difesa endogeni nella parodontite. Abbiamo dimostrato che l’IL-37 è presente e aumentata nella malattia e che ha la capacità specifica di ridurre un enzima chiave nella distruzione tissutale, l’MMP-9, proprio nelle cellule che formano la prima barriera della gengiva. Un piccolo passo avanti nella comprensione di questa complessa malattia, che ci ricorda quanto sia affascinante e intricato il dialogo tra i microbi e il nostro sistema immunitario.
Fonte: Springer