Parkinson: E se la Chiave Fosse Nascosta in Minuscole Vescicole?
Ciao a tutti! Oggi voglio parlarvi di qualcosa di veramente affascinante che sta emergendo nel campo della ricerca sul Parkinson. Sapete, questa malattia neurodegenerativa è la seconda più comune al mondo e, ammettiamolo, rappresenta un peso enorme per chi ne soffre e per le loro famiglie. La cosa frustrante è che, ancora oggi, le cause esatte ci sfuggono un po’. Sappiamo che c’entra la perdita dei neuroni dopaminergici nella substantia nigra, quella parte del cervello fondamentale per il movimento, e l’accumulo di una proteina “sbagliata”, l’alfa-sinucleina, che forma i corpi di Lewy. Ma cosa scatena tutto questo?
Messaggeri Nascosti nel Sangue: Le Vescicole Extracellulari (EVs)
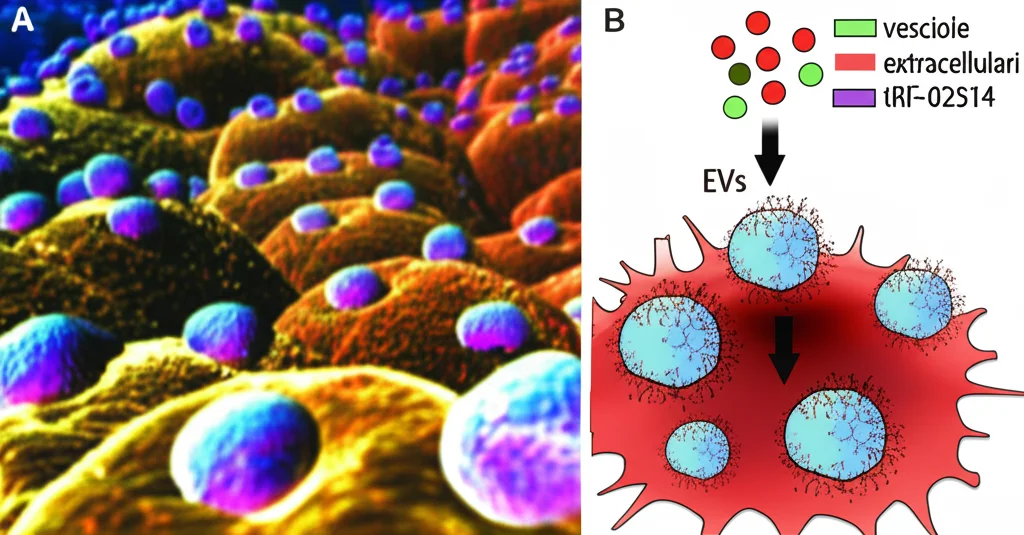
Qui entra in gioco una scoperta pazzesca: le vescicole extracellulari, o EVs. Immaginatele come minuscole “bolle” lipidiche, dei veri e propri pacchetti postali che le nostre cellule si scambiano continuamente. Si trovano ovunque nel nostro corpo, specialmente nel sangue, e trasportano un sacco di molecole bioattive. Sono fondamentali per la comunicazione tra cellule, anche tra i neuroni, e aiutano a mantenere tutto in equilibrio. Recentemente, abbiamo capito che queste EVs potrebbero giocare un ruolo cruciale anche nel Parkinson, forse addirittura nel diffondere l’alfa-sinucleina “malata” da un neurone all’altro, un po’ come un effetto domino. Capire come funzionano queste EVs è diventato quindi un obiettivo primario per trovare nuove terapie.
Un Nuovo Protagonista: i Frammenti di tRNA (tRFs)
Ma la storia non finisce qui. Dentro queste EVs c’è un mondo! Oltre a proteine e lipidi, trasportano anche piccoli pezzi di RNA non codificante. Tra questi, una nuova classe sta attirando molta attenzione: i frammenti derivati dal tRNA (tRFs). Sono pezzettini corti di RNA (16-40 nucleotidi) che sembrano avere un ruolo importante nella regolazione genica, legandosi direttamente agli mRNA per bloccarne la traduzione in proteine. Pensate un po’, potrebbero essere dei nuovi bersagli terapeutici super innovativi! Alcuni studi li hanno già indicati come potenziali biomarcatori per diagnosticare Parkinson e Alzheimer.
La Scoperta: tRF-02514, il “Cattivo” della Situazione?
Ed eccoci al dunque. In uno studio recente, di cui vi parlo oggi, i ricercatori hanno fatto una cosa molto interessante. Hanno isolato le EVs dal siero di pazienti con Parkinson (le chiameremo PD-EVs) e le hanno messe a contatto con cellule della microglia. La microglia sono le cellule immunitarie del cervello; nel Parkinson tendono ad attivarsi eccessivamente, causando neuroinfiammazione, un altro fattore chiave della malattia. Analizzando il contenuto di queste PD-EVs con tecniche di sequenziamento avanzate, hanno identificato diversi tRFs espressi in modo diverso rispetto alle EVs di persone sane. Tra tutti, uno spiccava: tRF-02514. Era significativamente più abbondante nelle PD-EVs.
Il Meccanismo: Come tRF-02514 Accende l’Infiammazione
Ma cosa fa di preciso questo tRF-02514? Sembra essere un vero piromane! I ricercatori hanno scoperto che quando le PD-EVs (cariche di tRF-02514) vengono assorbite dalla microglia, scatenano un processo infiammatorio chiamato piroptosi. È una forma di morte cellulare programmata molto “rumorosa”, che rilascia un sacco di citochine pro-infiammatorie come IL-1β e IL-18. Questo succede perché tRF-02514 sembra prendere di mira un gene chiave per l’autofagia, chiamato ATG5. L’autofagia è il sistema di pulizia interna della cellula: elimina proteine danneggiate e organelli vecchi. Inibendo ATG5, tRF-02514 blocca questo processo di pulizia. Una microglia con l’autofagia bloccata è più propensa ad attivare l’inflammasoma NLRP3, un complesso proteico che dà il via alla piroptosi e al rilascio di quelle citochine infiammatorie che danneggiano ulteriormente i neuroni. Insomma, tRF-02514 sembra gettare benzina sul fuoco della neuroinfiammazione nel Parkinson.
La Prova del Nove: Bloccare tRF-02514 Funziona!
A questo punto, la domanda sorge spontanea: e se bloccassimo tRF-02514? I ricercatori hanno provato a farlo, sia in vitro sulle cellule di microglia (BV2) sia in vivo su modelli animali di Parkinson (topi trattati con MPTP, una tossina che mima la malattia). Hanno usato un piccolo RNA interferente (siRNA) specifico per silenziare tRF-02514. I risultati? Davvero promettenti!
- Nelle cellule di microglia: Il trattamento con l’inibitore di tRF-02514 ha ridotto significativamente il rilascio di citochine infiammatorie (IL-1β, IL-18) e l’espressione dei marcatori di piroptosi (NLRP3, Caspase-1) indotti dalle PD-EVs. Inoltre, ha aumentato l’espressione di ATG5, riattivando l’autofagia.
- Nei topi modello di Parkinson: L’iniezione dell’inibitore di tRF-02514 direttamente nel cervello dei topi ha portato a miglioramenti notevoli. I topi mostravano migliori performance motorie nei test comportamentali (rotarod, open field, pole test). A livello molecolare, nel loro cervello e sangue si osservava una riduzione delle citochine pro-infiammatorie e un aumento di quelle anti-infiammatorie (IL-4, IL-10).
Protezione Neuronale e Nuove Speranze
Ma non è tutto. Bloccare tRF-02514 ha mostrato anche effetti neuroprotettivi diretti. Nei topi trattati con l’inibitore, si è osservato:
- Un aumento dei livelli di fattori neurotrofici importantissimi come il BDNF (Brain-Derived Neurotrophic Factor) e il NGF (Nerve Growth Factor), essenziali per la sopravvivenza e la salute dei neuroni.
- Una riduzione della morte cellulare (apoptosi) nel cervello.
- Una maggiore sopravvivenza dei neuroni dopaminergici nella substantia nigra, come evidenziato dalle colorazioni specifiche (Nissl e TH).
- Una diminuzione dei marcatori di piroptosi (NLRP3, GSDMD, Caspase-1) e un aumento del marcatore di autofagia (ATG5) direttamente nel tessuto cerebrale.
Questi risultati suggeriscono che inibire tRF-02514 non solo spegne l’eccessiva infiammazione microgliale, ma promuove anche meccanismi di difesa e riparazione neuronale, rallentando di fatto la progressione della malattia nel modello animale.
Cosa Significa Tutto Questo per il Futuro?
Ragazzi, questa è una scoperta potenzialmente enorme! Ci dice che un piccolo frammento di RNA, tRF-02514, trasportato da quelle minuscole vescicole nel sangue, gioca un ruolo da protagonista negativo nel Parkinson, alimentando l’infiammazione e la morte neuronale attraverso la modulazione dell’autofagia e della piroptosi nella microglia. La cosa ancora più eccitante è che bloccarlo sembra funzionare, almeno nei modelli preclinici.
Questo apre scenari incredibili:
- Biomarcatore: Misurare i livelli di tRF-02514 nelle EVs del sangue potrebbe diventare un nuovo strumento diagnostico o prognostico per il Parkinson.
- Bersaglio Terapeutico: Sviluppare farmaci che inibiscono specificamente tRF-02514 potrebbe rappresentare una nuova strategia terapeutica per rallentare la malattia. L’uso di tecnologie come l’RNA interference (RNAi), magari veicolata proprio tramite EVs ingegnerizzate, sembra promettente.
- Drug Delivery: Le EVs stesse, capaci di attraversare la barriera emato-encefalica, potrebbero essere usate come navicelle per consegnare farmaci (come l’inibitore di tRF-02514) direttamente nel cervello.

Certo, la strada verso l’applicazione clinica è ancora lunga e servono ulteriori studi per confermare questi risultati e valutare la sicurezza e l’efficacia nell’uomo. Ma è innegabile che questa ricerca getti una nuova luce sulla complessa patogenesi del Parkinson e offra una speranza concreta per lo sviluppo di terapie innovative che vadano oltre la semplice gestione dei sintomi. Teniamo d’occhio questo tRF-02514, potrebbe davvero essere una delle chiavi per sconfiggere il Parkinson!
Fonte: Springer