Ingegneria dell’Acqua all’Interfaccia: La Chiave Nascosta per l’Elettrolisi Pura
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi affascina da matti: l’acqua. Sì, proprio lei, H₂O. Sembra banale, ma vi assicuro che nasconde segreti incredibili, specialmente quando si trova vicino a certe superfici. E indovinate un po’? Capire questi segreti potrebbe essere la chiave per sbloccare una produzione di idrogeno davvero pulita ed efficiente, proprio quello di cui abbiamo un disperato bisogno per la transizione energetica.
Viviamo in un’epoca in cui l’abbandono dei combustibili fossili non è più un’opzione, ma una necessità impellente a causa del riscaldamento globale. L’idrogeno si presenta come un candidato ideale per immagazzinare e distribuire energia pulita: ha un’alta densità energetica, è semplice e, se prodotto con energie rinnovabili tramite elettrolisi dell’acqua (WE), può abbattere le emissioni di gas serra fino al 75%! Il problema? Rendere l’elettrolisi efficiente, scalabile e conveniente. Le tecnologie attuali, come quelle alcaline o a membrana a scambio protonico (PEM), hanno i loro limiti. Ma se vi dicessi che la soluzione potrebbe trovarsi… nell’acqua stessa?
L’Acqua “Strana” all’Interfaccia: Benvenuti nel Mondo SOW
L’acqua che conosciamo, quella nel bicchiere o nel fiume, è chiamata “bulk water”. Ma quando l’acqua incontra una superficie, specialmente una idrofila (che ama l’acqua), le cose cambiano. Si forma uno strato chiamato acqua interfacciale, che ha proprietà diverse. Recentemente, abbiamo scoperto zone ancora più estese di acqua ordinata, chiamate acqua auto-organizzata (SOW – Self-Organized Water), che possono estendersi per centinaia di micrometri dalla superficie!
Questa SOW non è la solita acqua. È come se si mettesse in riga: le molecole sono più ordinate, ha un indice di rifrazione e una viscosità maggiori, e addirittura esclude soluti e nanoparticelle (un po’ snob, eh?). Ma la cosa più pazzesca è la separazione di carica: vicino a superfici come il Nafion (un materiale idrofilo), la zona SOW accumula una carica negativa (circa -200 mV), mentre più lontano si forma una zona di acqua protonata (PW) con carica positiva. È come se l’acqua creasse una micro-batteria spontaneamente! Questo fenomeno non si limita al Nafion, ma è stato osservato su vari materiali idrofili, suggerendo che sia una caratteristica universale.

Un Aiutino dalla Luce Infrarossa
Ma non finisce qui. Abbiamo scoperto che l’energia elettromagnetica, in particolare la luce infrarossa (IR), ha un impatto notevole sull’acqua interfacciale. L’IR, che è abbondante sulla Terra, promuove l’espansione delle zone SOW. Esperimenti hanno mostrato che l’IR, anche a potenze simili a quelle della luce visibile o UV, è molto più efficace nell’allargare queste zone. Nel nostro studio, 13 minuti di irradiazione IR hanno espanso significativamente la SOW!
Perché è importante? Perché espandere la SOW significa amplificare quella separazione di carica e, soprattutto, facilitare la dissociazione dell’acqua. L’energia IR fa vibrare le molecole d’acqua, indebolendo i legami idrogeno e aiutando l’acqua (H₂O) a scindersi in ioni idrossido (OH⁻) e protoni (H⁺). Gli OH⁻, più grandi, rimangono intrappolati nella SOW negativa vicino alla superficie, mentre i protoni H⁺, più piccoli e mobili, vengono spinti via verso la zona PW positiva. Questo processo è fondamentale per l’elettrolisi: stiamo praticamente “preparando” l’acqua per essere scissa in idrogeno e ossigeno!
SOW e Reazioni Elettrochimiche: Un Matrimonio Perfetto
Ok, abbiamo quest’acqua strutturata e caricata, potenziata dall’IR. Come si traduce questo in una migliore elettrolisi? Abbiamo fatto dei test usando la voltammetria ciclica con un sistema redox ferri-ferrocianuro. I risultati sono stati chiari: nel sistema SOW, la corrente di picco era significativamente più alta rispetto all’acqua normale (bulk water). Questo indica un trasferimento di elettroni molto più efficiente tra l’elettrodo e le specie chimiche in soluzione.
Perché? Probabilmente grazie a una combinazione di fattori:
- Maggiore conduttività del sistema SOW.
- Maggiore area superficiale efficace dovuta alla struttura ordinata.
- Presenza di protoni (H⁺) vicino all’elettrodo che facilitano le reazioni, specialmente la reazione di sviluppo dell’idrogeno (HER).
- L’allineamento ordinato delle molecole d’acqua nella SOW potrebbe stabilizzare gli stati di transizione delle reazioni e abbassare le barriere di attivazione.
Insomma, l’acqua SOW non è solo “strana”, è attivamente utile per far avvenire le reazioni elettrochimiche più velocemente e con meno energia.

L’Elettrodo Giusto: PEO-Pt/Ti
Ovviamente, per un’elettrolisi efficiente non basta “giocare” con l’acqua. Serve anche un ottimo elettrodo. Nel nostro lavoro, abbiamo sviluppato un elettrodo speciale basato su una eterostruttura platino-titanio (Pt/Ti) trattata con un processo chiamato Plasma Electrolytic Oxidation (PEO).
Il PEO crea sulla superficie dell’elettrodo uno strato nanoporoso con caratteristiche fantastiche:
- Aumenta enormemente l’area superficiale, esponendo più siti catalitici attivi (dove avvengono le reazioni).
- Migliora la diffusione dei reagenti e dei prodotti grazie alla porosità controllata.
- Aumenta la rugosità, migliorando l’adesione del catalizzatore (il platino) e il trasporto di massa.
- Migliora la conduttività elettrica e la stabilità generale dell’elettrodo.
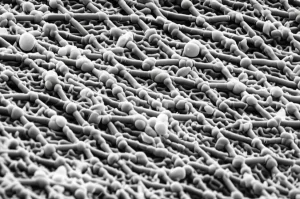
Abbiamo confermato la morfologia e la composizione (platino, titanio, ossigeno) di questi elettrodi PEO-Pt/Ti usando tecniche come la microscopia elettronica a scansione (FE-SEM) e la spettroscopia a dispersione di energia (EDS). Il risultato è un elettrodo robusto, efficiente e potenzialmente più economico, perché la struttura PEO permette di usare meno platino (che è costoso) mantenendo alte prestazioni.

La Sinergia Vincente: SOW + PEO-Pt/Ti + IR = Idrogeno a Go-Go!
Ed ecco il momento clou: abbiamo messo insieme tutti i pezzi. Abbiamo costruito un elettrolizzatore usando i nostri elettrodi PEO-Pt/Ti sia come anodo che come catodo, immersi in acqua pura, creando così un sistema SOW, e abbiamo aggiunto l’irradiazione IR. I risultati sono stati entusiasmanti!
Il nostro sistema SOW potenziato dall’IR con elettrodi PEO-Pt/Ti ha mostrato prestazioni eccellenti:
- Ha raggiunto una densità di corrente di 100 mA cm⁻² a soli 3.1 V di tensione di cella. Un valore notevole per l’elettrolisi di acqua pura.
- La produzione di idrogeno (H₂) a 3.5 V era significativamente maggiore rispetto all’elettrolisi in acqua normale (bulk water) e anche rispetto al sistema SOW senza IR. Abbiamo misurato il volume di gas prodotto nel tempo e confermato la presenza di H₂ e O₂ puri tramite gascromatografia (GC).
- Ha dimostrato una stabilità eccezionale, funzionando per oltre 25 ore consecutive senza degrado significativo delle prestazioni o della struttura dell’elettrodo (verificato con SEM post-operazione). Operare a pH neutro (acqua pura) aiuta molto a evitare problemi di corrosione e dissoluzione del catalizzatore comuni in ambienti acidi o alcalini.
Questo successo è dovuto alla sinergia tra l’acqua SOW (che facilita la dissociazione dell’acqua e il trasporto dei protoni) e l’elettrodo PEO-Pt/Ti (che offre un’ampia superficie attiva, buona conduttività e stabilità). L’IR dà quella spinta energetica in più per ottimizzare la SOW.

Conclusioni e Prospettive Future
Quindi, cosa abbiamo imparato? Che non dobbiamo pensare all’acqua solo come a un reagente passivo nell’elettrolisi. Possiamo attivamente “ingegnerizzare” l’acqua all’interfaccia per migliorare drasticamente il processo. Il nostro approccio, che combina l’ingegneria dell’acqua SOW (potenziata da IR) con l’ingegneria avanzata degli elettrodi (PEO-Pt/Ti), apre una nuova strada per la produzione di idrogeno.
Questo sistema non è solo efficiente, ma anche durevole e potenzialmente più economico rispetto ad alcune alternative. Offre una strategia scalabile per la produzione sostenibile di idrogeno, affrontando alcune delle sfide chiave nella generazione di energia pulita.
È un campo di ricerca ancora giovane, ma i risultati sono incredibilmente promettenti. Continuare a esplorare e capire a fondo le proprietà dell’acqua interfacciale e come sfruttarle potrebbe davvero rivoluzionare le tecnologie per l’energia rinnovabile. Il futuro dell’idrogeno verde potrebbe essere scritto… nell’acqua stessa!
Fonte: Springer