Idrogel Iperelastici: Il Segreto è nella Struttura Gerarchica!
Avete mai pensato a come fanno i nostri tessuti biologici, come muscoli o cartilagini, ad essere così incredibilmente performanti pur essendo composti da elementi relativamente semplici? La risposta sta spesso nella loro struttura gerarchica, un’organizzazione complessa su diverse scale di grandezza, dal nanometro al micrometro e oltre. Replicare questa genialità della natura nei materiali sintetici è una delle grandi sfide della scienza dei materiali, specialmente quando parliamo di idrogel.
Gli idrogel sono materiali affascinanti, ricchi d’acqua come i nostri tessuti, e per questo candidati ideali per applicazioni biomediche, come l’ingegneria tissutale o il rilascio controllato di farmaci. Tuttavia, gli idrogel “classici”, formati da una semplice rete polimerica, spesso non possiedono quella combinazione unica di morbidezza, resistenza, elasticità e capacità di favorire la crescita cellulare che caratterizza i tessuti naturali. Qui entro in gioco io, o meglio, la ricerca che voglio raccontarvi oggi, che svela un approccio innovativo per creare idrogel che non solo imitano la struttura, ma anche le incredibili proprietà meccaniche dei tessuti biologici.
Come Nascono Questi Materiali Straordinari?
Immaginate di avere dei “mattoncini Lego” molecolari speciali: dei copolimeri a triblocco anfifilici. Nel nostro caso, si tratta di molecole lunghe con due estremità idrofobiche (che non amano l’acqua, come il polistirene o PS) e una parte centrale idrofilica (che ama l’acqua, come l’ossido di polietilene o PEO). Sciogliamo questi copolimeri in un solvente organico miscibile con l’acqua (come DMF o THF) e poi iniettiamo rapidamente questa soluzione in acqua.
Cosa succede? È qui che avviene la magia dell’auto-assemblaggio!
- Scala Nanometrica: Le estremità idrofobiche si cercano e si aggregano per sfuggire all’acqua, formando delle minuscole sfere chiamate micelle. Queste micelle funzionano come punti di reticolazione fisica, tenute insieme dalle lunghe catene idrofiliche centrali, creando una rete polimerica nanostrutturata.
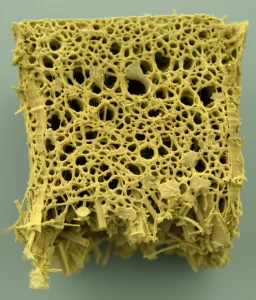
- Scala Micrometrica: Contemporaneamente, a causa dello scambio rapido tra il solvente organico e l’acqua, avviene una separazione di fase che crea dei pori, delle cavità ricche d’acqua, all’interno della rete micellare. Questi pori non sono disposti a caso, ma tendono ad allinearsi lungo la direzione dell’iniezione, formando una microstruttura porosa e orientata.
Il risultato? Una fibra di idrogel con una struttura gerarchica che ricorda sorprendentemente la matrice extracellulare dei tessuti, come l’endomisio del muscolo scheletrico. E tutto questo avviene in un unico passaggio, senza bisogno di stampi complessi o forze esterne!
Un’Architettura su Misura: Il Ruolo Chiave del Solvente
La cosa davvero interessante è che possiamo “accordare” la microstruttura, e quindi le proprietà finali dell’idrogel, semplicemente cambiando le condizioni iniziali, come il tipo di solvente organico usato (DMF o THF) e la concentrazione del polimero.
Abbiamo scoperto che, mentre la nanostruttura (la dimensione e l’organizzazione delle micelle, circa 20 nm di diametro e 80 nm di distanza media) rimane sorprendentemente costante indipendentemente dal solvente o dalla concentrazione usata (come confermato da tecniche come TEM e SAXS), la microstruttura (la dimensione e la disposizione dei pori) cambia drasticamente.
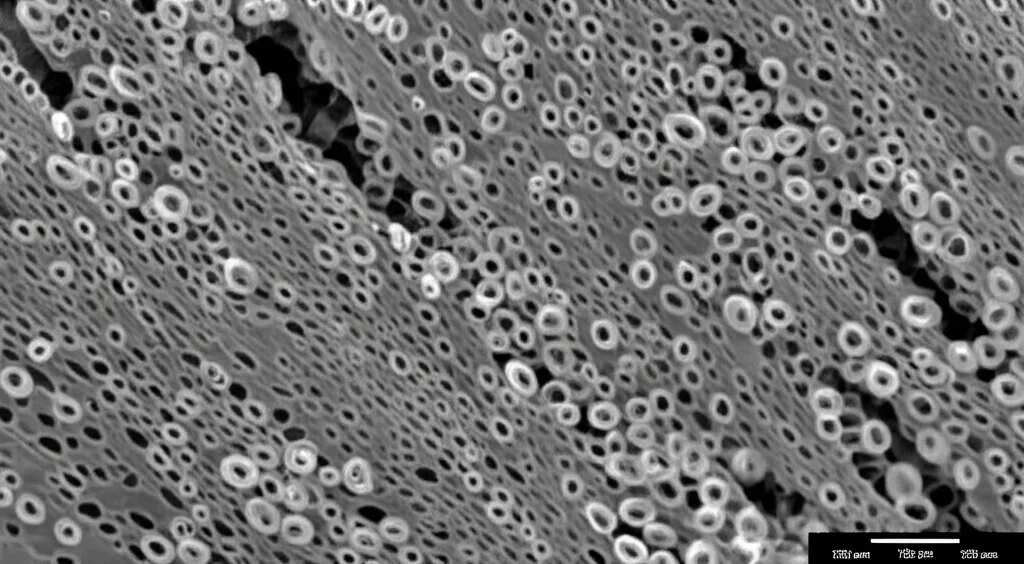
Utilizzando il DMF (N,N-dimetilformammide), otteniamo idrogel con una morfologia “core-sheath”, cioè con un guscio esterno caratterizzato da pori grandi (circa 30 µm) e un nucleo interno con pori molto più piccoli (circa 5 µm). Questa distribuzione bimodale rimane costante anche variando la concentrazione iniziale del polimero.
Se invece usiamo il THF (tetraidrofurano), la storia cambia. Otteniamo una distribuzione di pori più uniforme (monomodale), ma la dimensione media dei pori diminuisce significativamente all’aumentare della concentrazione iniziale del polimero, passando da circa 30 µm a circa 9 µm. Inoltre, i pori diventano più omogenei in dimensione. Tecniche come la microscopia confocale a fluorescenza e la diffusione della luce a piccolo angolo (SALS) confermano questa struttura porosa interconnessa e orientata lungo l’asse della fibra.
Ma perché questa differenza tra DMF e THF? L’ipotesi più probabile è legata ai diversi “percorsi” che la miscela polimero-solvente-acqua segue durante il rapidissimo scambio di solventi, influenzando come e quando avviene la separazione di fase che genera i pori. È un po’ come seguire strade diverse su una mappa di fase ternaria.
La Meccanica della Morbidezza Estrema: Quando la Struttura Fa la Differenza
Ed eccoci al punto cruciale: come questa microstruttura influenza le proprietà meccaniche? In modo stupefacente! Nonostante siano composti per circa il 98% di acqua e abbiano un modulo elastico bassissimo (inferiore a 1 kPa, quindi sono estremamente morbidi), questi idrogel possono essere allungati fino a 12 volte la loro lunghezza iniziale in modo completamente reversibile! Avete capito bene: si allungano enormemente e poi tornano esattamente come prima, ciclo dopo ciclo, senza mostrare segni di fatica o deformazione permanente (isteresi zero), come si vede nei test di carico/scarico ciclico.
Questa combinazione di altissima estensibilità, elasticità quasi perfetta e comportamento non lineare (la resistenza aumenta notevolmente solo a grandi deformazioni, un fenomeno chiamato iperelasticità, tipico della gomma e di molti tessuti biologici) è eccezionale per un idrogel, specialmente se così poroso.

Il segreto sta proprio nella struttura gerarchica e, in particolare, nei pori. Quando applichiamo uno sforzo, inizialmente sono i pori a deformarsi e ad allinearsi, un po’ come accade in una schiuma o una spugna. Questo richiede pochissima forza. Solo quando i pori sono quasi collassati e lo sforzo aumenta, la tensione viene trasferita alla rete nanometrica delle micelle e delle catene polimeriche che le collegano, che iniziano ad allungarsi. Questo meccanismo a due stadi spiega sia la morbidezza iniziale che l’aumento di rigidità (strain-hardening) a grandi deformazioni. Lo abbiamo visto direttamente con misure di microscopia ottica *in situ* durante la deformazione! E, cosa importante, misure SAXS *in situ* hanno confermato che la distanza tra le micelle non cambia significativamente anche a grandi allungamenti (fino a 5 volte la lunghezza iniziale), supportando l’idea che la deformazione iniziale sia assorbita principalmente dalla microstruttura porosa.
È affascinante notare come la diversa microstruttura indotta dai solventi si traduca in diverse curve sforzo-deformazione: gli idrogel fatti con THF, con pori più piccoli e omogenei a concentrazioni più alte, mostrano un aumento di rigidità più marcato e a deformazioni inferiori rispetto a quelli fatti con DMF, con la loro struttura core-sheath. Questo dimostra che possiamo davvero controllare la risposta meccanica agendo sulla microstruttura, senza cambiare la chimica di base del polimero.
Unici nel Loro Genere e Pronti per il Futuro
Se confrontiamo questi idrogel gerarchici con altri materiali avanzati, vediamo quanto siano speciali. Molti idrogel sintetici cercano di mimare una o due proprietà dei tessuti naturali, ma raramente riescono a combinare bassa rigidità, altissima estensibilità, elasticità reversibile e una struttura porosa favorevole alle cellule. Idrogel supramolecolari o a reti interpenetranti possono essere molto elastici, ma spesso soffrono di isteresi a causa della dissipazione viscosa. Altri, come quelli basati su polimeri a spazzola (bottlebrush), mostrano un eccellente strain-stiffening simile ai tessuti, ma mancano della struttura porosa gerarchica.
I nostri idrogel, invece, grazie all’auto-assemblaggio guidato dal processo, raggiungono questa combinazione vincente. La loro posizione in un grafico che mette in relazione resistenza e allungamento a rottura (simile a un diagramma di Ashby) li colloca in una zona unica, caratterizzata da morbidezza estrema ed estensibilità eccezionale, superando molti altri sistemi noti.

Le potenzialità sono enormi. Stiamo parlando di una nuova piattaforma per creare biomateriali su misura. Immaginate scaffold per l’ingegneria tissutale che non solo offrono un ambiente poroso ideale per la crescita cellulare, ma possiedono anche le proprietà meccaniche adatte a specifiche applicazioni, dal tessuto muscolare alla cartilagine. La possibilità di regolare le proprietà meccaniche semplicemente cambiando il solvente o la concentrazione iniziale, mantenendo la stessa chimica di base, apre scenari entusiasmanti per la personalizzazione dei materiali biomedici.
In conclusione, abbiamo dimostrato come sfruttando l’auto-assemblaggio guidato dal processo sia possibile creare idrogel porosi con un’architettura gerarchica ben definita. Questa struttura, in particolare la morfologia dei pori su scala micrometrica, è la chiave per ottenere proprietà meccaniche eccezionali e finemente regolabili, aprendo una nuova strada per la progettazione di biomateriali avanzati, dove è la struttura, e non solo la molecola, a dettare le regole. Il viaggio è appena iniziato, ma la direzione è chiara: imitare la natura, una struttura alla volta!
Fonte: Springer