Intelligenza Artificiale al Microscopio: Rivoluzioniamo l’Analisi dell’Aterosclerosi!
Ciao a tutti! Oggi voglio parlarvi di qualcosa che mi appassiona tantissimo: come l’intelligenza artificiale (IA) sta cambiando radicalmente il modo in cui studiamo una delle malattie più diffuse e pericolose del nostro tempo, l’aterosclerosi. Sapete, quella condizione subdola in cui le nostre arterie si “incrostano” di placche, portando a infarti e ictus. È la prima causa di morte nei paesi industrializzati occidentali, un problema enorme!
La Sfida: Capire le Placche Arteriosclerotiche
Per capire come si formano queste placche e come possiamo combatterle, noi ricercatori usiamo spesso modelli animali, in particolare i topi. Li modifichiamo geneticamente (ad esempio, topi knockout per l’Apolipoproteina E, o Apoe-/-) e li nutriamo con diete ricche di grassi per simulare ciò che accade nel corpo umano. Poi, analizziamo le loro arterie, specialmente la radice aortica, al microscopio.
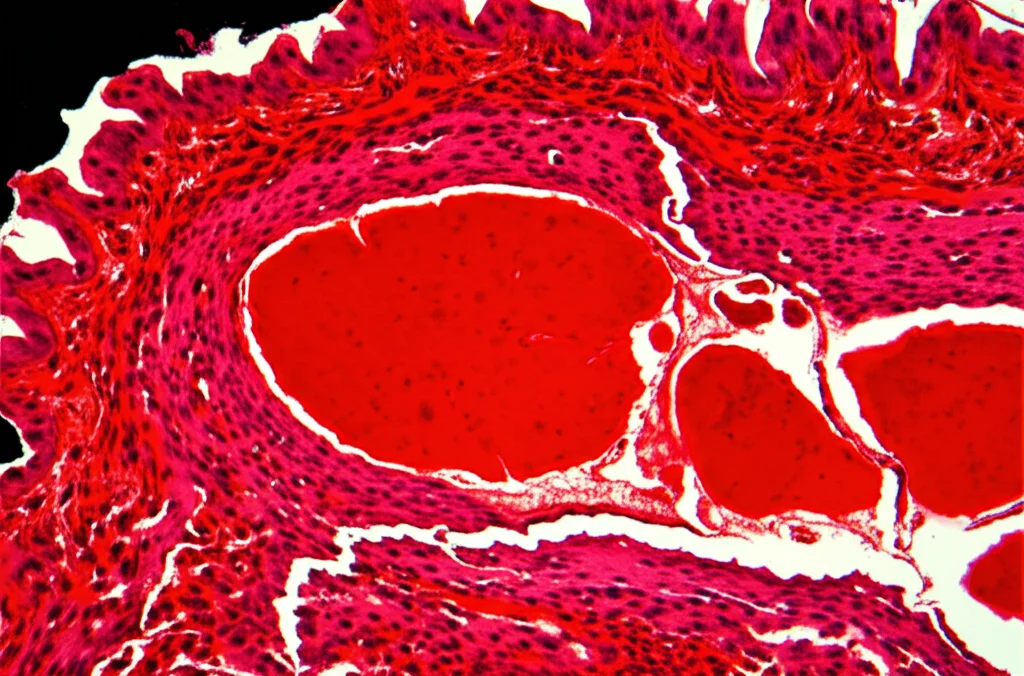
Una tecnica fondamentale è la colorazione con Oil Red O (ORO). Questo colorante ha la fantastica proprietà di evidenziare i lipidi, facendoli apparire di un rosso brillante. Poiché le placche aterosclerotiche sono piene di macrofagi carichi di lipidi, l’ORO ce le fa vedere benissimo su quelle che chiamiamo “immagini di vetrini interi” o Whole Slide Images (WSIs).
Fin qui, tutto bene. Il problema? Analizzare queste immagini è un lavoro lunghissimo e certosino. Tradizionalmente, tecnici specializzati devono mettersi lì, armati di pazienza, e “disegnare” manualmente i contorni dell’arteria e quantificare l’area occupata dalle placche rosse. Immaginate di doverlo fare per centinaia, a volte migliaia, di vetrini… un’impresa titanica, costosa e, diciamocelo, anche un po’ soggettiva. A volte si usano tecniche basate su soglie di colore, ma richiedono comunque un intervento manuale per impostare i parametri giusti.
L’Arrivo dell’IA: Una Soluzione Brillante
Ed è qui che entra in gioco l’intelligenza artificiale! Negli ultimi anni, l’IA ha fatto passi da gigante, aprendo la strada a metodi automatici e rapidi per analizzare queste immagini complesse. Ma attenzione, non è tutto rose e fiori. Applicare l’IA alla patologia presenta delle sfide:
- Spesso abbiamo pochi dati “etichettati” (cioè immagini con contorni già disegnati a mano) per addestrare i modelli.
- Le WSI hanno risoluzioni altissime, difficili da gestire.
- Ci possono essere differenze nella colorazione tra un laboratorio e l’altro, o persino tra diversi esperimenti.
- Anche le impostazioni dei microscopi possono variare.
Per superare questi ostacoli, abbiamo sviluppato una pipeline basata sull’IA, un processo automatico in tre fasi principali che promette di accelerare enormemente la ricerca.

Fase 1: Trovare l’Arteria (ROI Detection)
Prima di tutto, dobbiamo dire all’IA dove guardare. In una WSI c’è un sacco di tessuto circostante che non ci interessa. Usiamo quindi un modello di “object detection” super moderno, chiamato YOLOv8l (You Only Look Once, versione large). È come dare all’IA degli occhiali speciali che riconoscono subito la forma generale della radice aortica e disegnano un “riquadro” attorno ad essa. Questo riquadro è la nostra Regione di Interesse (ROI). Concentrandoci solo sulla ROI, l’analisi successiva diventa molto più precisa ed efficiente.
Fase 2: Disegnare i Contorni dell’Arteria (Segmentazione Supervisionata)
Una volta isolata la ROI, entra in gioco la segmentazione vera e propria. Qui usiamo l’apprendimento supervisionato. Abbiamo “addestrato” delle reti neurali specializzate nel riconoscere i pixel che appartengono alla parete dell’arteria. Abbiamo testato diverse architetture famose come U-Net, U-Net++, FPN, PAN, ma la U-Net++ si è rivelata la migliore per questo compito.
Ma non ci siamo fermati qui! Abbiamo scoperto che usare un “ensemble” di reti U-Net++, cioè far lavorare insieme diverse versioni dello stesso modello (ottenute con una tecnica chiamata “snapshot ensemble”), dà risultati ancora più robusti. È come chiedere il parere a un comitato di esperti invece che a uno solo: si riducono gli errori individuali.
Abbiamo anche sviluppato una strategia di combinazione innovativa: invece di fare semplicemente la media dei risultati, usiamo un metodo di “sovrapposizione” con un parametro regolabile (che abbiamo chiamato α). Questo ci permette di bilanciare la precisione: possiamo decidere se essere più “prudenti” (evitando falsi positivi, cioè aree segnate come arteria che non lo sono) o più “inclusivi” (evitando falsi negativi, cioè parti di arteria mancate). È fantastico perché possiamo adattare l’output quasi in tempo reale! Combinando l’approccio ROI con l’ensemble (il “combined ROI ensemble”), abbiamo ottenuto maschere arteriose di altissima qualità nel 97% dei casi!
Fase 3: Quantificare le Placche (Segmentazione Non Supervisionata)
Ora che abbiamo definito perfettamente l’arteria, dobbiamo trovare le placche rosse al suo interno. Qui la sfida è diversa: spesso non abbiamo maschere disegnate a mano per le placche (ground truth). Come fare? Usiamo l’apprendimento non supervisionato!
Abbiamo adattato un’architettura chiamata W-Net, che è una specie di “autoencoder” intelligente. Impara da sola a raggruppare i pixel con caratteristiche simili, senza bisogno di etichette predefinite. In pratica, le diciamo: “Trova le aree rosse e dense all’interno della maschera dell’arteria che ti abbiamo dato”.
Per migliorare ulteriormente, abbiamo aggiunto due trucchi:
- Trasferimento di Colore: Poiché la colorazione ORO può variare, abbiamo applicato una tecnica per rendere i colori più omogenei su tutte le immagini prima di darle in pasto alla W-Net. Questo aiuta la rete a non confondersi.
- Post-Processing: L’output grezzo della W-Net può essere un po’ “rumoroso”. Applichiamo quindi delle operazioni morfologiche (per pulire i contorni) e un algoritmo (k-nn) per identificare i cluster di placca significativi, eliminando piccoli artefatti.

La Prova del Nove: Funziona Davvero?
Abbiamo testato la nostra pipeline su migliaia di immagini! Per la segmentazione dell’arteria, abbiamo usato un dataset interno enorme (oltre 6000 WSI!). Per la segmentazione delle placche, abbiamo usato un dataset più piccolo (circa 1100 WSI) per cui avevamo, eccezionalmente, delle etichette manuali di riferimento (HLR).
I risultati? Impressionanti! La nostra pipeline combinata (ROI + Ensemble U-Net++) per l’arteria ha raggiunto un mIoU (una metrica di accuratezza della segmentazione) medio di 0.833, un risultato eccellente. Per le placche, la W-Net post-processata ha mostrato una correlazione fortissima (Pearson’s r = 0.94) con le misurazioni manuali. Certo, tende a stimare aree leggermente più piccole, ma questo potrebbe dipendere anche dal fatto che la segmentazione manuale a volte “arrotonda” troppo i contorni complessi delle placche. È importante notare che ha identificato correttamente il 92% dei vetrini che erano effettivamente senza placche.
Un Caso di Studio Reale: Conferma Biologica
La vera prova del fuoco è stata applicare la nostra pipeline a dati di uno studio già pubblicato (Aherrahrou et al., 2023). In questo studio, avevano analizzato manualmente l’aterosclerosi in topi con una particolare modifica genetica (deficit di Cyp17a1) sottoposti a dieta normale o ricca di grassi (Western Type Diet – WTD).
Abbiamo rianalizzato quasi 400 WSI di quello studio con il nostro metodo automatico. Risultato? La nostra pipeline ha replicato quasi perfettamente le conclusioni biologiche dello studio originale! Abbiamo confermato che la modifica genetica promuove l’aterosclerosi nei topi maschi, ma non nelle femmine, specialmente con la dieta WTD. La correlazione tra le nostre misurazioni automatiche delle placche e quelle originali (basate su soglia) è stata altissima (Pearson’s r = 0.91), specialmente dopo aver applicato il trasferimento di colore e il post-processing alla W-Net.

Cosa Significa Tutto Questo?
Significa che abbiamo creato uno strumento potentissimo! Questa pipeline automatica può analizzare centinaia di vetrini in pochi secondi, un lavoro che richiederebbe giorni o settimane a un tecnico. Questo non solo accelera enormemente la ricerca sull’aterosclerosi, ma rende anche i risultati più consistenti e meno dipendenti dalla soggettività umana.
Certo, l’occhio esperto del patologo rimane fondamentale, specialmente per la verifica finale. Ma possiamo ridurre drasticamente il lavoro manuale, liberando tempo prezioso per interpretare i dati e fare nuove scoperte.
Siamo convinti che l’IA applicata all’analisi delle immagini istologiche, come nel nostro caso, avrà un impatto enorme sulla ricerca cardiovascolare e sullo sviluppo di nuove terapie contro l’aterosclerosi. È un campo in rapidissima evoluzione e non vedo l’ora di vedere cosa ci riserverà il futuro!
Fonte: Springer