HKR1: La Nuova Chiave per Capire (e Combattere?) il Cancro alla Prostata
Ciao a tutti! Oggi voglio parlarvi di una scoperta che mi ha davvero appassionato nel campo della ricerca sul cancro alla prostata. Sapete, questa malattia è un osso duro, il tumore maligno più comune nel sistema urinario maschile, con numeri da capogiro ogni anno. Nonostante i progressi, come il test del PSA che ha rivoluzionato la diagnosi precoce, ci troviamo ancora di fronte a sfide enormi. Molti pazienti, anche dopo terapie iniziali efficaci, vanno incontro a recidive e sviluppano forme resistenti ai trattamenti. E non dimentichiamo i falsi negativi del PSA che possono ritardare cure vitali. Insomma, c’è un bisogno disperato di nuovi strumenti, di biomarcatori che ci aiutino a capire meglio chi rischia di più e chi potrebbe rispondere meglio a terapie innovative come l’immunoterapia.
Ed è qui che entra in gioco il protagonista della nostra storia: un gene chiamato HKR1.
HKR1: Chi è Costui?
HKR1, il cui nome completo è Human Krüppel-related gene 1, appartiene a una grande famiglia di geni chiamati KRAB-ZNF. Questi geni sono un po’ come dei “regolatori epigenetici”, capaci di silenziare altri geni influenzando la metilazione del DNA. Si sa che giocano un ruolo nello sviluppo, nella proliferazione cellulare e, ahimè, anche nella formazione dei tumori. Studi precedenti avevano già collegato HKR1 alla metilazione del DNA e persino a malattie neurodegenerative. Qualcuno aveva notato che era più espresso nel cancro al polmone e una mutazione era stata trovata in pazienti con storia familiare di cancro alla prostata. Insomma, c’erano degli indizi, ma il suo ruolo specifico nel cancro alla prostata (PCa) era ancora avvolto nel mistero. Così, mi sono tuffato nell’analisi di dati complessi per cercare di capirci qualcosa di più.
HKR1 e il Cancro alla Prostata: Un Legame Scomodo
La prima cosa che abbiamo scoperto, analizzando montagne di dati da database pubblici come TCGA (The Cancer Genome Atlas) e confrontandoli con le nostre analisi di laboratorio (qPCR su linee cellulari e tessuti reali), è stata piuttosto chiara: l’espressione di HKR1 è significativamente più alta nei tessuti tumorali della prostata rispetto a quelli normali. Non si tratta di piccole differenze, parliamo di un aumento statisticamente robusto (p < 0.05). Anche a livello proteico, i dati dal database HPA (Human Protein Atlas) confermavano questa tendenza: più proteina HKR1 nel tumore che nel tessuto sano. Questo è stato il primo campanello d'allarme: perché questo gene è così "acceso" nel cancro alla prostata?
Prognosi Infelice: Quando HKR1 è Alto
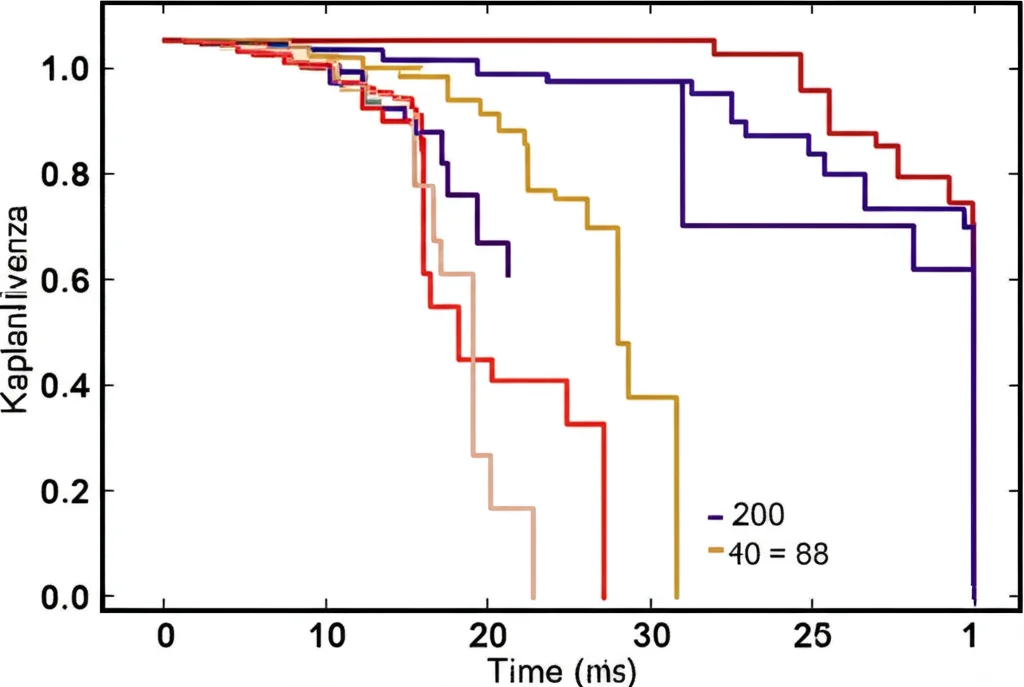
Andando più a fondo, abbiamo esplorato il legame tra i livelli di HKR1 e l’andamento della malattia nei pazienti. Utilizzando i dati clinici associati ai campioni del TCGA, abbiamo fatto un’analisi di sopravvivenza (Kaplan-Meier). Il risultato è stato netto: i pazienti con alti livelli di espressione di HKR1 avevano una prognosi peggiore, una sopravvivenza globale (OS) più breve rispetto a quelli con bassi livelli (p = 0.014). Non solo, ma l’analisi di regressione di Cox, uno strumento statistico che valuta l’influenza di diversi fattori sulla sopravvivenza, ha suggerito che HKR1 potrebbe essere un indicatore prognostico indipendente. In parole povere, il livello di HKR1 sembra fornire informazioni sul rischio del paziente indipendentemente da altri fattori clinici noti come l’età, lo stadio del tumore o il valore del PSA. Abbiamo anche costruito un nomogramma, una specie di calcolatore grafico, che integra HKR1 con altri fattori clinici, e ha mostrato un’ottima capacità predittiva della sopravvivenza a 5 anni.
Dentro le Cellule: Cosa Ci Dice il Single-Cell
Per capire meglio dove si annida HKR1 all’interno del complesso ecosistema tumorale, abbiamo usato una tecnologia potentissima: il sequenziamento dell’RNA a singola cellula (scRNA-Seq), analizzando dati dal dataset GSE141445. Questa tecnica ci permette di guardare l’espressione genica cellula per cellula, un po’ come fare uno zoom incredibile sul tumore. E cosa abbiamo visto? Che HKR1 non è espresso uniformemente, ma si trova principalmente nelle cellule maligne stesse, nelle cellule epiteliali circostanti e anche in alcune popolazioni di cellule immunitarie presenti nel tumore. Questo è affascinante perché suggerisce che HKR1 potrebbe avere ruoli diversi a seconda del tipo di cellula in cui si trova all’interno del microambiente tumorale.
Meccanismi Nascosti: Le Vie del Segnale
Ok, HKR1 è alto, è legato a una brutta prognosi e si trova in cellule chiave. Ma *cosa fa* esattamente? Per indagare sui meccanismi biologici, abbiamo usato un’analisi chiamata GSEA (Gene Set Enrichment Analysis). Questa tecnica cerca di capire quali “percorsi” o “vie di segnalazione” cellulare sono più attive quando HKR1 è altamente espresso. Abbiamo scoperto che HKR1 è significativamente associato a diverse vie cruciali, tra cui:
- La via del Toll-like receptor (TLR): importante per la risposta immunitaria innata.
- La via del TGF-beta: un attore chiave nella crescita cellulare, ma spesso dirottato dai tumori per promuovere la progressione.
- La via del p53: il famoso “guardiano del genoma”, spesso alterato nel cancro.
- Altre vie legate all’infiammazione e alla risposta immunitaria (NOD-like receptor, sensori del DNA citosolico, chemiochine, recettore delle cellule B).
Queste associazioni suggeriscono che HKR1 potrebbe influenzare la crescita del tumore, la sua capacità di sfuggire al sistema immunitario e la sua interazione con l’ambiente circostante agendo su questi snodi molecolari fondamentali.

HKR1 e il Sistema Immunitario: Amici o Nemici?
Il cancro alla prostata è spesso definito un tumore “freddo”, cioè poco reattivo all’immunoterapia perché ha un microambiente che sopprime le risposte immunitarie. Capire come HKR1 interagisce con il sistema immunitario è quindi fondamentale. Le nostre analisi hanno rivelato correlazioni interessanti:
- L’espressione di HKR1 è positivamente correlata con l’infiltrazione di alcuni tipi di cellule immunitarie, in particolare i linfociti T CD8+ (i “killer” del sistema immunitario) e i linfociti T CD4+.
- È associata ai punteggi ESTIMATE, Immune e Stromal, che misurano la presenza di cellule immunitarie e stromali (tessuto connettivo) nel tumore. Livelli alti di questi score sono spesso legati a prognosi peggiore nel PCa.
- È correlata all’espressione di diverse molecole di checkpoint immunitario (come CD274/PD-L1, CD86, CD44, CD40), che sono bersagli chiave dell’immunoterapia.
Questo quadro è complesso: da un lato HKR1 sembra associato alla presenza di cellule immunitarie potenzialmente utili, dall’altro è legato a un microambiente “difficile” e a molecole che possono frenare la risposta immunitaria. Ciò suggerisce che HKR1 potrebbe essere un modulatore chiave dell’interazione tumore-sistema immunitario e, potenzialmente, un bersaglio per rendere i tumori “freddi” più sensibili all’immunoterapia.
Bersagli Terapeutici e Regolatori a Monte
Se HKR1 è così importante, possiamo usarlo a nostro vantaggio? Abbiamo esplorato se i livelli di HKR1 fossero correlati alla sensibilità delle cellule tumorali a farmaci chemioterapici comuni, usando il database “CellMiner”. Abbiamo trovato che alti livelli di HKR1 sono associati a una *minore* sensibilità (cioè maggiore resistenza, misurata come IC50 più alta) a farmaci come chelerythrine, cladribine e fludarabine. Questo potrebbe avere implicazioni per la scelta delle terapie: pazienti con basso HKR1 potrebbero rispondere meglio a questi farmaci.
Infine, ci siamo chiesti: cosa regola HKR1? Utilizzando il database “StarBase”, abbiamo cercato potenziali meccanismi a monte. Abbiamo identificato due possibili “assi regolatori” che coinvolgono delle proteine leganti l’RNA (RBP, in particolare HNRNPA2B1) e dei lunghi RNA non codificanti (lncRNA, specificamente LINC00342 e AP004608.1). In pratica, questi lncRNA potrebbero influenzare l’attività di HNRNPA2B1, che a sua volta potrebbe controllare l’espressione di HKR1. È come aver trovato i possibili “interruttori” che accendono o spengono HKR1 nel cancro alla prostata.
Conclusioni e Prospettive Future
Tirando le somme, il nostro viaggio nell’analisi di HKR1 nel cancro alla prostata ci ha portato a scoperte entusiasmanti. Sembra proprio che HKR1 sia un attore importante: è sovraespresso, è legato a una prognosi peggiore, è coinvolto in vie di segnalazione chiave e modula l’interazione con il sistema immunitario. Potrebbe quindi rappresentare un nuovo biomarcatore prognostico e, chissà, forse anche un bersaglio terapeutico o un indicatore per guidare l’immunoterapia. Abbiamo anche identificato possibili meccanismi che lo regolano.
Certo, siamo ancora all’inizio. Molti di questi risultati derivano da analisi bioinformatiche e dovranno essere confermati con esperimenti in vivo e studi clinici. Ma la strada è tracciata. Aver identificato HKR1 come un pezzo importante del puzzle del cancro alla prostata apre nuove porte per la ricerca e, speriamo, per future strategie diagnostiche e terapeutiche più efficaci per i pazienti. È un campo in continua evoluzione, e non vedo l’ora di vedere cosa scopriremo dopo!
Fonte: Springer