Fullereni “Pimpati” al PEG: La Nuova Frontiera per Trasportare il Carboplatino?
Ciao a tutti! Oggi voglio portarvi con me in un viaggio affascinante nel mondo delle nanotecnologie applicate alla medicina. Immaginate di poter creare dei minuscoli “taxi” molecolari capaci di trasportare farmaci potentissimi, come quelli usati in chemioterapia, direttamente dove servono, riducendo gli effetti collaterali. Sembra fantascienza, vero? Eppure, è proprio quello che stiamo esplorando con strumenti computazionali avanzatissimi!
Nel mio campo, usiamo simulazioni al computer per capire come interagiscono le molecole a un livello incredibilmente dettagliato. Recentemente, ci siamo concentrati su un farmaco chemioterapico molto usato, il carboplatino, e su un potenziale “taxi” davvero speciale: il fullerene C60.
Ma cos’è questo Fullerene C60?
Pensate a una microscopica palla da calcio, fatta però di 60 atomi di carbonio. Questa è la struttura base del fullerene C60. È affascinante per le sue proprietà uniche: grande superficie, buona biocompatibilità (almeno in linea di principio) e la capacità di legarsi a diverse molecole. Un candidato ideale come nanovettore, no?
Però, c’è un “ma”. I fullereni puri non amano molto l’acqua, e il nostro corpo è fatto principalmente d’acqua! Questo limita la loro utilità pratica in medicina. Inoltre, per rendere le cose ancora più interessanti (e potenzialmente utili), abbiamo pensato di “dopare” questo fullerene inserendo un atomo di ferro (Fe) al suo interno, creando quello che chiamiamo Fe@C60. Perché il ferro? Beh, oltre a poter avere effetti terapeutici propri, rende il nostro nanovettore potenzialmente tracciabile con tecniche come la risonanza magnetica (MRI). Immaginate poter seguire il viaggio del farmaco nel corpo in tempo reale!
La “Modifica” Chiave: Il PEG
Per risolvere il problema della solubilità e migliorare ulteriormente la biocompatibilità e il tempo di permanenza nel sangue, abbiamo “funzionalizzato” la superficie del nostro Fe@C60 con delle catene di polietilenglicole (PEG). È un po’ come mettere un cappotto più “socievole” alla nostra palla di fullerene, rendendola più affine all’ambiente acquoso del corpo. Questo processo si chiama PEGilazione ed è una strategia molto usata nel campo dei nanovettori.
Il Bersaglio: Il Carboplatino
Il carboplatino è un’arma potente contro diversi tipi di cancro (ovaio, polmone, testicolo…). Purtroppo, come molte chemioterapie, non è selettivo e può danneggiare anche cellule sane, causando effetti collaterali pesanti (problemi ai reni, tossicità neurologica…). Da qui nasce l’esigenza di un sistema di trasporto che lo porti il più possibile solo alle cellule tumorali. L’idea è: possiamo usare il nostro Fe@C60 “pimpato” con il PEG per trasportare il carboplatino in modo più sicuro ed efficace?
Gli Strumenti del Mestiere: DFT e Dinamica Molecolare
Per rispondere a questa domanda, non siamo entrati subito in laboratorio. Abbiamo usato la potenza dei computer! In particolare, due tecniche computazionali: la Teoria del Funzionale della Densità (DFT) e le simulazioni di Dinamica Molecolare (MD).
La DFT è come una potentissima lente d’ingrandimento che ci permette di studiare la struttura elettronica delle molecole e come interagiscono a livello quantistico. Ci dice quali parti della molecola sono più reattive, come si distribuiscono le cariche, quanto è stabile un legame.
La Dinamica Molecolare, invece, è come girare un film a livello atomico. Simula il movimento delle molecole nel tempo, tenendo conto della temperatura, del solvente (nel nostro caso, l’acqua) e delle forze tra gli atomi. Ci fa vedere come il nostro nanovettore e il farmaco si “comportano” in un ambiente più realistico. Combinare DFT e MD ci dà una visione incredibilmente completa!
Cosa Abbiamo Scoperto: Stabilità e Interazione
Allora, cosa ci hanno detto i nostri computer?
Prima di tutto, abbiamo visto che aggiungere il PEG al Fe@C60 lo rende più stabile. L’energia di formazione (una misura della stabilità) migliora all’aumentare del PEG sulla superficie (anche se sembra esserci un punto ottimale con poche catene di PEG). Non solo: il PEG aumenta anche il momento di dipolo elettrico della struttura. In parole povere, rende il nostro nanovettore più “polare”, e questo favorisce l’interazione con altre molecole polari come il carboplatino. È come creare una calamita molecolare più forte!
E l’interazione con il carboplatino? I calcoli dell’energia di adsorbimento ci dicono che il carboplatino si lega al nostro Fe@C60:PEG in modo stabile, ma non *troppo* forte. L’energia di legame rientra in un intervallo che definiamo di “fisisorbimento”. Questo è fondamentale! Significa che il legame è abbastanza forte da trattenere il farmaco durante il trasporto nel sangue, ma abbastanza debole da permetterne il rilascio una volta raggiunto il sito bersaglio. Un equilibrio delicato ma cruciale. Abbiamo visto che questo legame avviene principalmente tramite legami a idrogeno tra il carboplatino e la superficie del nanovettore.
Abbiamo anche calcolato il “tempo di recupero” (τ), che ci dà un’idea di quanto velocemente il farmaco potrebbe essere rilasciato. I valori ottenuti (da frazioni di secondo a qualche minuto) suggeriscono che potremmo potenzialmente “sintonizzare” la velocità di rilascio modificando la struttura del nanovettore, in particolare il numero di catene di PEG. Più PEG sembra portare a un legame più forte e a un rilascio più lento e sostenuto.
Uno Sguardo Dentro: Proprietà Elettroniche e Spettri
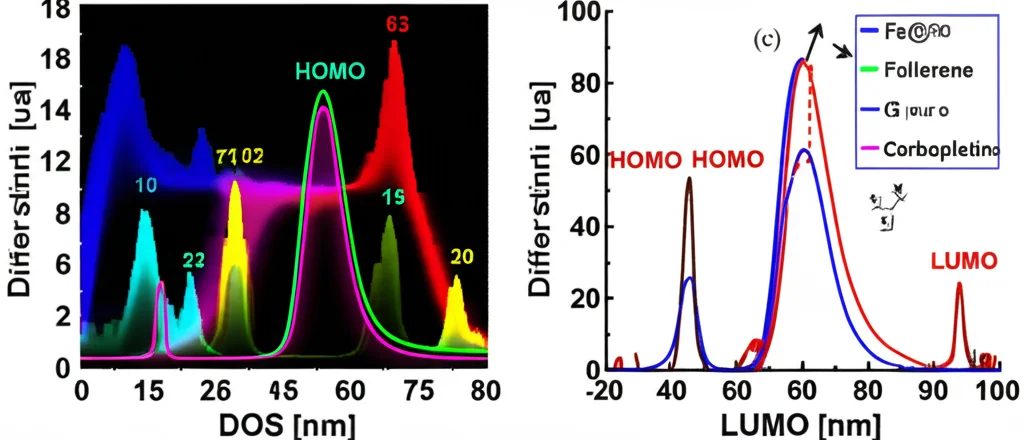
La DFT ci ha permesso di sbirciare anche nelle proprietà elettroniche. Abbiamo analizzato gli orbitali molecolari HOMO (Highest Occupied Molecular Orbital) e LUMO (Lowest Unoccupied Molecular Orbital). La differenza di energia tra HOMO e LUMO (il “band gap”) ci dice quanto facilmente la molecola può essere eccitata elettronicamente, influenzandone la reattività. Abbiamo visto che l’interazione con il carboplatino riduce questo gap energetico, suggerendo che il complesso farmaco-vettore potrebbe essere più reattivo del vettore da solo.
Analizzando la distribuzione spaziale di HOMO e LUMO, abbiamo capito quali parti delle molecole sono più coinvolte nelle interazioni. Nel complesso finale, sembra che il PEG e il C60 siano i protagonisti principali dell’attività elettronica, mentre il carboplatino partecipa in modo più “passivo” (coerente con il fisisorbimento).
Un altro aspetto affascinante è l’analisi degli spettri di assorbimento ottico. Abbiamo simulato come queste strutture assorbono la luce a diverse lunghezze d’onda (principalmente nell’UV-visibile). È emerso che l’interazione con il carboplatino modifica significativamente lo spettro di assorbimento del nanovettore Fe@C60:PEG. Ci sono diversi picchi tra 200 e 600 nm, e la loro posizione e intensità cambiano quando il carboplatino è legato. Questo è super interessante perché suggerisce che potremmo usare tecniche spettroscopiche per “vedere” se il farmaco è stato caricato sul vettore!
Abbiamo anche simulato gli spettri infrarossi (IR). Anche qui, l’aggancio del carboplatino provoca cambiamenti nelle vibrazioni molecolari, visibili come spostamenti o comparsa/scomparsa di picchi nello spettro IR. È un’ulteriore conferma che l’interazione sta avvenendo e sta modificando la struttura del complesso.
Il Balletto Molecolare: Cosa ci dice la Dinamica
Le simulazioni di Dinamica Molecolare (MD) ci hanno regalato una visione dinamica. Abbiamo “osservato” per 50 picosecondi (un tempo brevissimo, ma significativo a livello molecolare!) come si comporta il carboplatino vicino alla superficie del nostro Fe@C60:PEG in acqua. È stato pazzesco vedere come la carica elettrica localizzata sul carboplatino fluttui nel tempo, diventando a tratti più positiva o più negativa. Allo stesso tempo, la distanza tra il carboplatino e la superficie del fullerene variava, oscillando. Sembra esserci una correlazione: quando il farmaco si avvicina alla superficie, tende ad acquisire una carica più negativa (guadagna elettroni), mentre quando si allontana, la carica tende a diventare più positiva (perde elettroni). Questo “balletto” elettrostatico e spaziale è fondamentale per capire la natura dinamica del legame e del potenziale rilascio.
Tirando le Somme
Quindi, cosa abbiamo imparato da questo tuffo nel mondo computazionale?
- Incapsulare il ferro nel C60 gli conferisce proprietà magnetiche (potenzialmente utili per il targeting o l’imaging).
- Funzionalizzare con il PEG aumenta la stabilità e la solubilità del nanovettore.
- Il PEG migliora l’interazione con il carboplatino.
- Il legame carboplatino-vettore è di tipo fisisorbimento, ideale per un caricamento e rilascio controllato.
- L’energia di legame e il tempo di recupero suggeriscono un rilascio potenzialmente sintonizzabile.
- L’interazione modifica le proprietà elettroniche e ottiche, offrendo forse un modo per monitorare l’adsorbimento del farmaco.
- Le simulazioni MD mostrano una dinamica complessa di interazione tra farmaco e vettore.
Certo, siamo ancora a livello di simulazioni computazionali. Il prossimo passo sarà verificare queste predizioni in laboratorio. Ma i risultati sono davvero incoraggianti! Questi fullereni Fe@C60 funzionalizzati con PEG sembrano avere le carte in regola per diventare una nuova piattaforma versatile per la somministrazione mirata di farmaci come il carboplatino, aprendo la strada a terapie potenzialmente più efficaci e con meno effetti collaterali. La ricerca continua, e chissà quali altre meraviglie ci riserverà il mondo nano!
Fonte: Springer







