SPARCE: Spiare i Segreti delle Cellule Rare è Ora Possibile!
Introduzione: Il Mondo Nascosto Dentro le Nostre Cellule
Avete mai pensato a quanto sia incredibilmente complesso capire cosa succede davvero dentro una singola cellula? Non parlo solo del suo DNA, ma di come “parla”, come reagisce, come prende decisioni. Questo linguaggio cellulare è fatto di proteine che si attivano e disattivano, spesso attraverso un piccolo interruttore chimico: l’aggiunta o la rimozione di un gruppo fosfato. Studiare queste proteine “fosforilate” – un campo chiamato fosfoproteomica – è fondamentale per capire la salute e la malattia, specialmente quando le cose vanno storte in specifiche popolazioni cellulari.
Il problema? Spesso le cellule che ci interessano di più, quelle magari coinvolte in una malattia rara o nelle primissime fasi dello sviluppo, sono… beh, rare! Averne poche rende difficilissimo analizzarle con le tecniche tradizionali, che richiedono un sacco di materiale di partenza. È come cercare di capire una conversazione origliando da lontanissimo con tanto rumore di fondo.
La Sfida: Analizzare Poche Cellule è un Grattacapo
Per anni, noi scienziati ci siamo scontrati con questo muro. Le tecniche di sequenziamento di nuova generazione sono fantastiche per leggere il DNA e l’RNA anche di singole cellule, ma non ci dicono nulla su cosa fanno le proteine dopo essere state prodotte, specialmente riguardo alla fosforilazione. La spettrometria di massa è lo strumento d’elezione per la proteomica, e negli ultimi anni è diventata ultrasensibile, permettendoci di analizzare le proteine anche da poche cellule. Ma la fosfoproteomica è un osso più duro.
Perché? Perché per “vedere” le proteine fosforilate, dobbiamo prima “pescarle” selettivamente dal mix cellulare (un processo chiamato arricchimento), e questo passaggio, insieme a tutti gli altri necessari per preparare il campione, causa inevitabilmente delle perdite. Quando parti già con pochissimo materiale, ogni perdita è un dramma. Immaginate di dover preparare una torta avendo solo un cucchiaino di farina: difficile non sprecarne un po’!
Inoltre, tecniche come il FACS (Fluorescence-Activated Cell Sorting), che ci permettono di isolare con precisione le cellule rare che ci interessano, le raccolgono in soluzioni saline e volumi che non vanno molto d’accordo con i metodi standard di preparazione dei campioni per la spettrometria di massa.
La Nostra Soluzione: Vi Presento SPARCE!
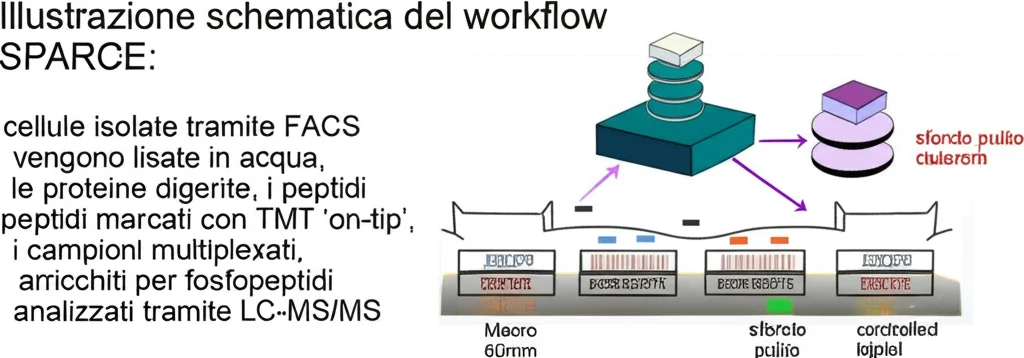
Ed è qui che entriamo in gioco noi, con un’idea e tanto lavoro di ottimizzazione. Abbiamo sviluppato un nuovo metodo che abbiamo chiamato SPARCE (Streamlined Phosphoproteomic Analysis of Rare CElls), pensato apposta per superare questi ostacoli e permettere l’analisi fosfoproteomica multiplexata (cioè analizzando più campioni insieme) partendo da un numero molto basso di cellule.
Cosa fa di speciale SPARCE? Integra e semplifica tutti i passaggi critici:
- Isolamento cellulare compatibile con FACS: Possiamo prendere le cellule appena isolate e iniziare subito la preparazione.
- Lisi cellulare in acqua: Invece dei soliti detergenti o agenti caotropici (come l’urea), usiamo semplice acqua e cicli di congelamento/riscaldamento. Sorprendentemente, abbiamo scoperto che questo metodo non solo funziona benissimo per rompere le cellule e liberare le proteine (anche quelle di membrana!), ma è molto più efficiente per quantità minime di materiale, riducendo le perdite e migliorando la successiva digestione delle proteine.
- Marcatura TMT “on-tip”: Usiamo delle etichette chimiche speciali (TMT, Tandem Mass Tags) che ci permettono di “marcare” i peptidi (frammenti di proteine) provenienti da campioni diversi. Questo ci consente di mixarli e analizzarli tutti insieme (multiplexing). La novità qui è che facciamo la marcatura direttamente sulla punta di una pipetta speciale (ZipTip) che serve anche per purificare i peptidi (desalting). Questo approccio “on-tip” si è rivelato molto più efficiente della marcatura classica “in soluzione”, specialmente per piccole quantità, perché concentra reagenti e peptidi, migliorando la cinetica della reazione e riducendo drasticamente le perdite. Un bonus? Recuperiamo meglio anche i peptidi idrofilici, che sono particolarmente importanti perché i gruppi fosfato rendono i peptidi più affini all’acqua!
- Arricchimento dei fosfopeptidi dopo il multiplexing: Solo dopo aver marcato e unito i campioni, procediamo all’arricchimento specifico per i fosfopeptidi. Fare l’arricchimento su un campione combinato e più abbondante è molto più robusto e meno soggetto a perdite stocastiche rispetto a farlo su tanti piccoli campioni separati.
Messo alla Prova: SPARCE Funziona Davvero?
Ok, bello sulla carta, ma la scienza vive di prove. Abbiamo messo alla prova SPARCE usando un modello biologicamente rilevante: linee cellulari derivate da pazienti con glioblastoma, un tumore cerebrale molto aggressivo. Queste cellule, coltivate in laboratorio mantenendo le loro caratteristiche originali, ci hanno fornito materiale eterogeneo e riproducibile.
Abbiamo isolato con il FACS gruppi di sole 1000 cellule (pochissime!) e di 20.000 cellule (come controllo “high-input”) da quattro diverse linee cellulari di glioblastoma. Abbiamo applicato il nostro protocollo SPARCE, usando la tecnica del “carrier channel” per i campioni da 1000 cellule. In pratica, abbiamo aggiunto a questi campioni piccolissimi un campione “carrier” molto più abbondante (ottenuto da 160.000 cellule mixate) marcato con un’etichetta TMT diversa. Questo “carrier” aiuta a “trascinare” i segnali dei peptidi rari durante l’analisi in spettrometria di massa, aumentandone l’identificazione, senza (come abbiamo verificato) compromettere troppo l’accuratezza quantitativa.
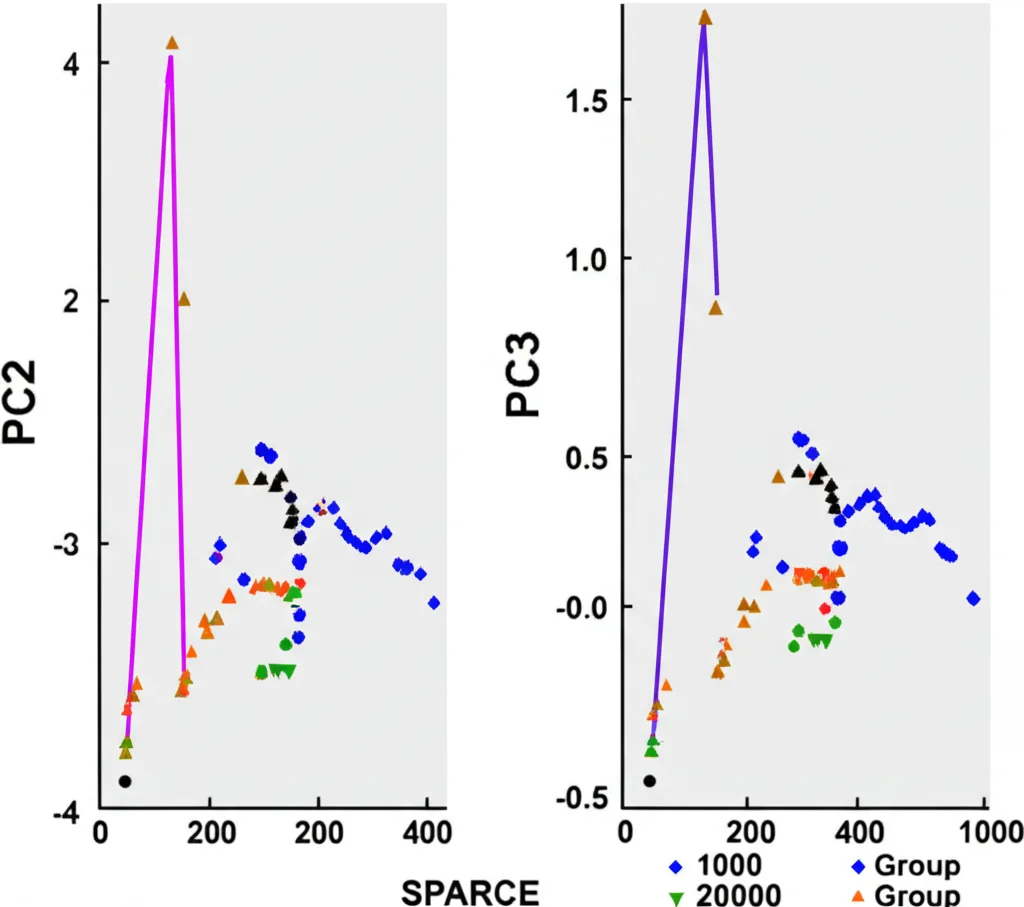
I risultati? Eccezionali! Anche partendo da sole 1000 cellule, siamo riusciti a quantificare in modo affidabile oltre 1600 siti di fosforilazione per campione (oltre 2500 nel caso delle 20.000 cellule). La riproducibilità tra le repliche tecniche era ottima (Coefficienti di Variazione mediani intorno al 21%), molto simile tra i campioni a basso e alto input. L’analisi statistica (PCA, analisi di abbondanza differenziale) ha mostrato che le diverse linee cellulari si raggruppavano coerentemente e che le differenze biologiche tra loro erano rilevate in modo consistente sia nei campioni da 1000 che da 20.000 cellule.
Non solo: siamo riusciti a ottenere informazioni funzionali! Analizzando i pattern di fosforilazione, abbiamo potuto inferire l’attività di specifici enzimi (le chinasi) responsabili di queste modifiche. Abbiamo visto profili di attività chinasica distinti per le diverse linee cellulari, suggerendo vie di segnalazione cellulare differenti, che potrebbero essere legate ai diversi comportamenti di queste cellule tumorali. E tutto questo, ripeto, partendo da un numero di cellule che fino a poco tempo fa sarebbe stato considerato insufficiente per questo tipo di analisi.
Perché SPARCE è Importante: Aprire Nuove Porte nella Ricerca
Cosa significa tutto questo in pratica? Significa che SPARCE apre la porta all’esplorazione della fosfoproteomica in contesti dove prima era quasi impossibile. Pensate a:
- Studiare popolazioni di cellule staminali rare.
- Capire i meccanismi di segnalazione durante lo sviluppo embrionale, dove le cellule specifiche sono pochissime.
- Indagare le origini di malattie complesse analizzando sottopopolazioni cellulari specifiche da biopsie o modelli animali.
- Lavorare con organismi modello da cui è difficile ottenere grandi quantità di cellule specifiche.
La cosa bella è che SPARCE, pur essendo all’avanguardia, non richiede necessariamente robotica ultra-specializzata o strumentazione fuori dal comune (a parte un buon spettrometro di massa, ovvio!). È un flusso di lavoro ottimizzato che può essere implementato in molti laboratori attrezzati per la proteomica.
Certo, la tecnologia non si ferma mai. Nuovi approcci di acquisizione dati in spettrometria di massa (come la DIA, Data-Independent Acquisition) promettono ancora maggiore sensibilità, ma al momento non offrono lo stesso livello di multiplexing del TMT, che è un vantaggio chiave quando si lavora con campioni multipli a bassissimo input. SPARCE si posiziona quindi come uno strumento potentissimo e accessibile per chi vuole combinare l’isolamento cellulare di precisione (FACS) con l’analisi profonda della segnalazione cellulare (fosfoproteomica multiplexata).
Conclusione: Un Passo Avanti per Capire la Vita Cellulare
SPARCE non è solo un nuovo acronimo o un metodo complicato per addetti ai lavori. È la dimostrazione che, con ingegno e ottimizzazione, possiamo superare limiti tecnici che sembravano invalicabili. È uno strumento che ci permette di “ascoltare” più da vicino le conversazioni silenziose ma fondamentali che avvengono all’interno delle cellule, anche le più rare ed elusive. E capire queste conversazioni è la chiave per svelare i meccanismi più profondi della biologia e della malattia.
Fonte: Springer