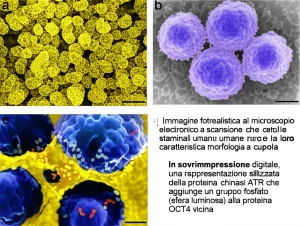
Forze Nascoste: Come le Cellule dell’Orecchio si Mettono in Fila Indiana (e perché è Fondamentale per Sentirci Bene)
Ciao a tutti, appassionati di scienza e curiosi! Oggi voglio portarvi in un viaggio incredibile all’interno di una delle strutture più affascinanti e delicate del nostro corpo: l’orecchio interno, e più precisamente l’epitelio uditivo, quella parte magica che ci permette di trasformare le vibrazioni sonore in segnali che il cervello può capire. Avete mai pensato a come fa questo tessuto a essere così incredibilmente preciso? Non si tratta solo di avere le cellule giuste al posto giusto, ma anche di farle “guardare” tutte nella stessa direzione! Sembra fantascienza, ma è pura biologia dello sviluppo, e la chiave, come scopriremo, sta in un intricato balletto di forze meccaniche a livello delle giunzioni tra le cellule.
L’Ordine è Tutto: Posizione e Direzione nell’Epitelio Uditivo
Immaginate l’epitelio uditivo come un mosaico vivente. Ci sono due tipi principali di tessere: le cellule ciliate (HC), le vere star dello show che sentono il suono grazie a dei ciuffetti specializzati chiamati fasci ciliari, e le cellule di supporto (SC), che le circondano e le aiutano a funzionare correttamente. Per sentire bene, questo mosaico deve avere due tipi di ordine:
- Ordine posizionale: Ogni cellula ciliata deve essere costantemente circondata da cellule di supporto. Niente contatti diretti tra cellule ciliate! Questo è cruciale per mantenere l’equilibrio chimico necessario alla trasduzione del suono.
- Polarità planare cellulare (PCP): Ogni cellula ciliata ha un suo “nord” intrinseco, dato dalla posizione eccentrica del suo fascio ciliare. La PCP si riferisce al fatto che tutte queste “bussole” cellulari devono puntare nella stessa direzione attraverso l’intero tessuto. Pensate a un campo di girasoli tutti rivolti verso il sole: è essenziale per una risposta coordinata e sensibile al suono.
La cosa strabiliante è che questi due livelli di ordine – posizione e orientamento – emergono contemporaneamente durante lo sviluppo, nonostante il tessuto sia in continuo movimento e riarrangiamento cellulare. Come è possibile? Qual è il legame tra i movimenti su larga scala del tessuto e i meccanismi interni delle singole cellule? Questa è la domanda a cui un recente studio, pubblicato su Nature Communications, ha cercato di rispondere, usando come modello l’epitelio uditivo del pulcino (la papilla basilare).
Un Balletto di Forze Meccaniche Guidato dalla Miosina
La risposta, amici miei, sembra risiedere in un preciso schema di forze giunzionali. Le giunzioni sono i punti di contatto tra cellule vicine, e non sono strutture statiche. Al loro interno agisce un complesso molecolare chiamato actomiosina, dove la miosina II non muscolare (NMII) funge da motore, generando tensione e contrattilità. L’attività di questo motore è finemente regolata dalla fosforilazione della sua catena leggera regolatrice (RLC). Esistono due forme principali: mono-fosforilata (p-RLC) e di-fosforilata (pp-RLC).
Lo studio ha scoperto qualcosa di fondamentale: queste due forme di RLC non sono distribuite a caso!
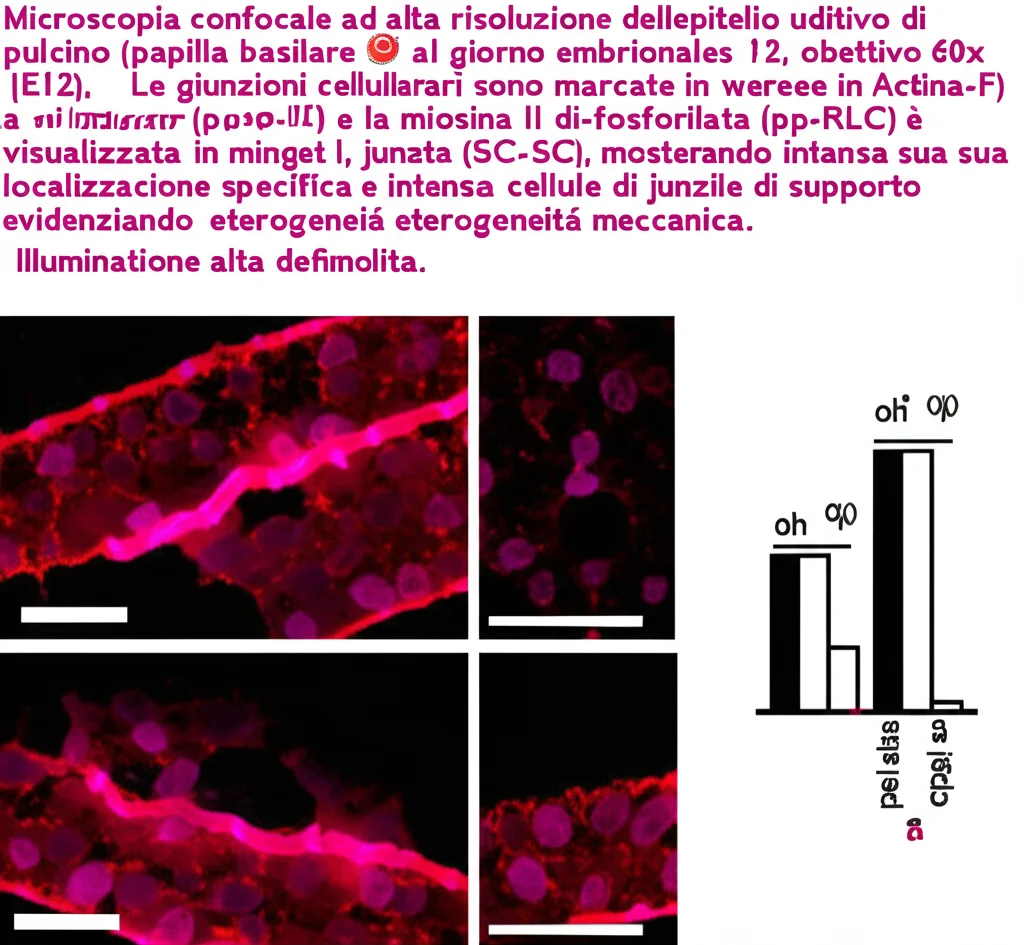
- La pp-RLC, associata a una maggiore stabilità e forza contrattile, si trova esclusivamente sulle giunzioni tra cellule di supporto (SC-SC).
- La p-RLC, legata a una dinamica più rapida e forse a minor forza, si trova sia sulle giunzioni SC-SC che su quelle tra cellule ciliate e di supporto (HC-SC).
Questa differenza non è da poco. Analizzando le fluttuazioni nella lunghezza delle giunzioni (un indicatore della loro dinamica e tensione) tramite live imaging, si è visto che le giunzioni SC-SC (ricche di pp-RLC) fluttuano molto meno di quelle HC-SC. Questo suggerisce che le giunzioni SC-SC sono più “tese”, più contrattili.
Modelli al Computer e Prove Sperimentali Confermano l’Ipotesi
Per capire se questa diversa contrattilità fosse sufficiente a spiegare l’ordine posizionale, i ricercatori hanno usato modelli computazionali chiamati “modelli a vertici 2D”. Immaginate di simulare il tessuto come una rete di poligoni (le cellule) che cercano di minimizzare una certa “energia” basata su area, forma e tensione delle giunzioni.
Ebbene, solo introducendo nel modello una maggiore contrattilità specifica per le giunzioni SC-SC (simulando l’effetto della pp-RLC), si riusciva a replicare ciò che si vede in natura: le cellule ciliate finiscono circondate da cellule di supporto, e i contatti diretti HC-HC vengono evitati o risolti attivamente. Inoltre, simulando la crescita in area delle cellule ciliate (un altro evento dello sviluppo), il modello mostrava un aumento dell’ordine posizionale (misurato con un parametro chiamato “ordine esatico”), proprio come osservato sperimentalmente.
Ma la scienza non si ferma ai computer! Per testare l’ipotesi nel mondo reale, hanno trattato espianti di papilla basilare con inibitori farmacologici. Bloccando la MLCK (l’enzima che produce pp-RLC specificamente nelle SC), hanno visto esattamente quello che il modello prediceva: la pp-RLC spariva dalle giunzioni SC-SC, queste diventavano meccanicamente più simili alle giunzioni HC-SC (maggiori fluttuazioni), comparivano contatti anomali HC-HC e l’ordine posizionale diminuiva. Ancora più interessante, anche la polarità planare veniva perturbata! E la cosa fantastica? Rimuovendo l’inibitore (esperimento di “wash-out”), sia l’ordine posizionale che l’allineamento della polarità venivano in gran parte ripristinati. Questo suggerisce fortemente che l’eterogeneità meccanica guidata dalla pp-RLC non solo crea l’ordine posizionale, ma è anche accoppiata all’orientamento cellulare.
Un Secondo Livello di Regolazione per l’Allineamento Polare
Ma come fa questa meccanica a guidare anche l’allineamento preciso dei fasci ciliari (la polarità)? Qui entra in gioco un secondo livello di regolazione, ancora più fine, che modula la contrattilità in modo asimmetrico durante una finestra temporale critica (tra il giorno embrionale E10 e E12):
- Sulle giunzioni HC-SC: La p-RLC (la forma “meno tesa”) diventa temporaneamente arricchita sulle giunzioni lontane dalla base del fascio ciliare (il chinetocilio). Questo è legato all’attività di un complesso proteico (LGN-Gαi) noto per controllare la polarità intrinseca della cellula ciliata. In pratica, la cellula ciliata rende le giunzioni “dietro” di sé meno contrattili.
- Sulle giunzioni SC-SC: La pp-RLC (la forma “più tesa”) diventa temporaneamente arricchita su quelle giunzioni che sono allineate con l’asse principale del tessuto (l’asse prossimo-distale, P-D).

Cosa significa tutto ciò? Tornando ai modelli al computer, introducendo queste asimmetrie “sintonizzate” (giunzioni HC-SC più contrattili vicino al chinetocilio, giunzioni SC-SC più contrattili lungo l’asse P-D), il modello mostrava che le cellule ciliate tendevano ad allineare il loro asse di polarità lungo la direzione superiore-inferiore (S-I), perpendicolare all’asse P-D. Si formavano delle specie di “catene” sovra-cellulari di giunzioni ad alta contrattilità lungo l’asse P-D, e questo costringeva le cellule ciliate ad allinearsi. Inizialmente, però, l’allineamento era “nematico”, cioè le cellule si allineavano lungo l’asse S-I ma puntavano a caso verso S o verso I.
Il Ruolo della Via PCP e della Curvatura del Tessuto
Come si stabilisce l’asse di riferimento P-D per l’arricchimento di pp-RLC? Qui entra in gioco la famosa via di segnalazione della Polarità Cellulare Planare (PCP). Una proteina chiave di questa via, chiamata Vangl2, mostrava un arricchimento proprio sulle giunzioni SC-SC allineate all’asse P-D, in modo simile alla pp-RLC. Esperimenti di knockdown genetico (eliminando Vangl2 in alcune cellule) confermavano il suo ruolo: senza Vangl2, la pp-RLC diminuiva su quelle giunzioni, e sia l’ordine posizionale che la polarità planare venivano compromessi. Quindi, la via PCP sembra fornire le “istruzioni” direzionali per modulare la contrattilità delle giunzioni SC-SC.
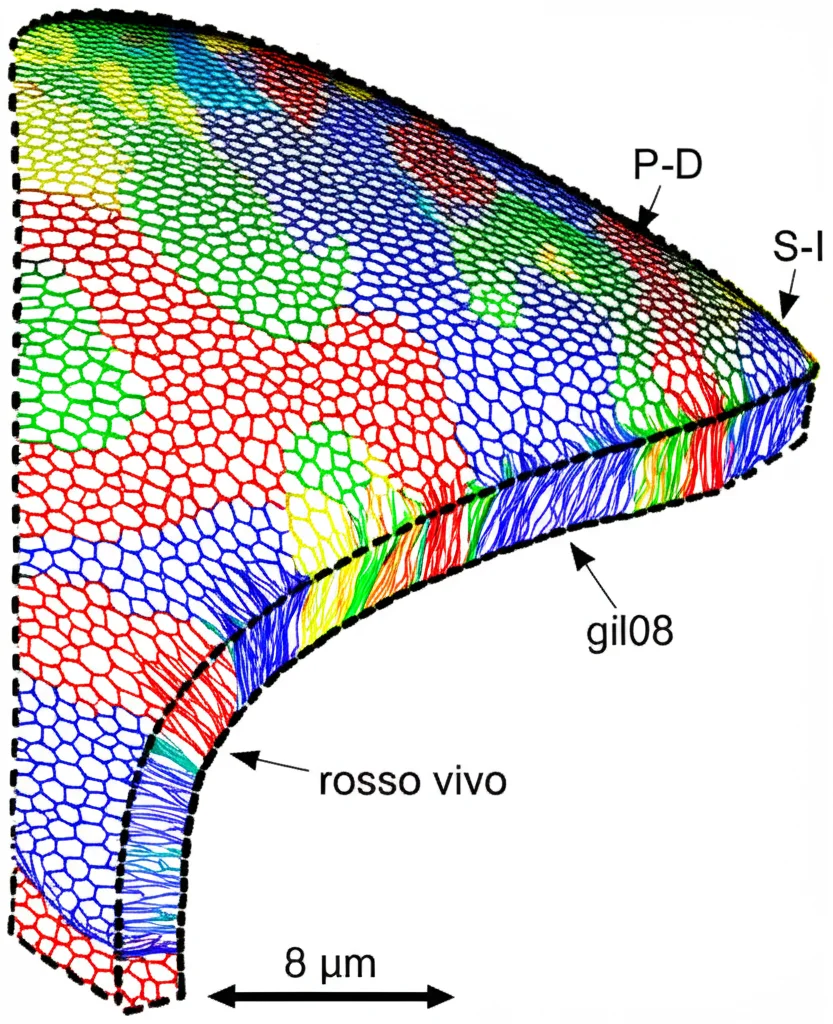
Ma rimaneva il problema dell’allineamento nematico (S o I a caso) nel modello. Cosa poteva “rompere” questa simmetria e far puntare tutte le cellule ciliate nella stessa direzione (ad esempio, verso I, come avviene in gran parte della papilla basilare)? I ricercatori hanno notato che la papilla basilare non è piatta, ma curva, a forma di falce. Introducendo questa curvatura nel modello, le simulazioni mostravano che le cellule ciliate sviluppavano una preferenza per una direzione specifica (ad esempio, l’inferiore), perché la curvatura induce uno stiramento differenziale tra il bordo superiore (più lungo) e quello inferiore (più corto), favorendo l’allineamento delle giunzioni HC-SC meno contrattili (quelle “dietro” il chinetocilio) verso il lato più lungo (superiore).
Conclusioni: Un Capolavoro di Meccano-Biologia
È affascinante pensare a come processi biologici così complessi e precisi possano essere orchestrati da principi meccanici relativamente semplici, ma finemente regolati a livello molecolare. Questo studio ci mostra un quadro elegante in cui:
- Differenze fondamentali nella contrattilità tra tipi cellulari (pp-RLC solo su SC-SC) guidano l’ordine posizionale di base.
- Una sintonizzazione temporanea e spaziale di questa contrattilità (asimmetrie su HC-SC legate alla polarità intrinseca, e su SC-SC legate all’asse tissutale via PCP/Vangl2) guida l’allineamento della polarità planare.
- Proprietà geometriche globali come la curvatura possono contribuire a stabilire una direzione polare univoca.
Questo meccanismo di “force patterning” giunzionale, dove le forze vengono modellate e direzionate in modo specifico, potrebbe essere un principio generale per l’organizzazione di molti altri tessuti epiteliali composti da più tipi cellulari, non solo nell’orecchio ma forse anche in altri organi sensoriali o durante lo sviluppo embrionale. La prossima volta che ascolterete la vostra musica preferita, pensate a questo incredibile balletto di forze molecolari che permette alle vostre cellule uditive di essere perfettamente ordinate e allineate per catturare ogni nota!
Fonte: Springer