Vescica Infiammata, Tessuto Cicatrizzato: Abbiamo Trovato i Colpevoli!
Ciao a tutti! Oggi voglio portarvi con me in un viaggio affascinante nel microscopico mondo della nostra vescica, un organo incredibile ma che, ahimè, può andare incontro a problemi seri come l’infiammazione cronica. E quando l’infiammazione persiste, si rischia un guaio chiamato fibrosi.
Cos’è la Fibrosi e Perché Dovrebbe Interessarci?
Immaginate la fibrosi come una sorta di “cicatrice interna”. Invece del tessuto normale, funzionale, il nostro corpo inizia a produrre eccessivamente una matrice extracellulare (ECM) densa e rigida, un po’ come se stesse costruendo un muro dove non serve. Nella vescica, questo processo patologico è un bel problema: il tessuto cicatriziale rende la parete vescicale meno elastica, meno “accomodante”. Il risultato? La vescica perde la sua capacità di riempirsi correttamente, diventa iperattiva, e compaiono quei fastidiosissimi sintomi di urgenza e minzione frequente. Pensate a quanto possa impattare sulla qualità della vita!
Mentre in organi come polmoni, reni, fegato e cuore la fibrosi è stata studiata a fondo, sulla vescica c’era ancora molto da scoprire. Un punto chiave in questo processo è la trasformazione di cellule chiamate fibroblasti in miofibroblasti. Questi ultimi sono i veri “operai” della fibrosi, quelli che producono materialmente la cicatrice. Ma nella vescica, chi sono esattamente questi fibroblasti che decidono di “cambiare mestiere”?
Alla Ricerca dei Fibroblasti “Cattivi”: Le Cellule PDGFRα+
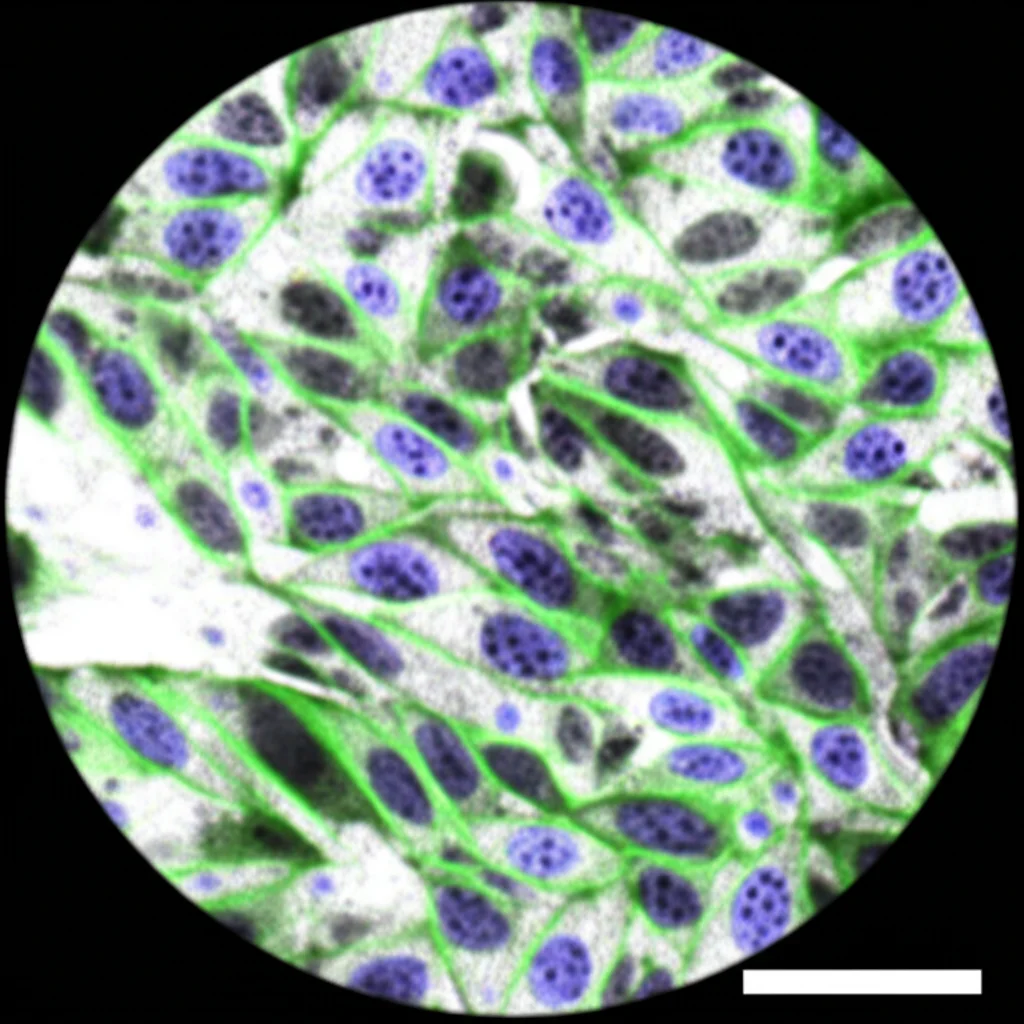
Recentemente, la ricerca ha puntato i riflettori su una popolazione particolare di cellule presenti nella vescica, caratterizzate dall’esprimere un recettore chiamato PDGFRα (Platelet-Derived Growth Factor Receptor Alpha). Queste cellule PDGFRα+ sono state identificate come i fibroblasti della vescica. La cosa interessante è che non sono tutte uguali! Ne esistono diverse popolazioni, distinte a seconda della loro “residenza” all’interno della parete vescicale. C’erano quelle nello strato muscolare (il detrusore) e quelle proprio sotto il rivestimento interno (l’urotelio), chiamate cellule PDGFRα+ suburoteliali.
Data questa eterogeneità, la domanda cruciale era: quale di queste popolazioni di fibroblasti PDGFRα+ è responsabile della trasformazione in miofibroblasti e quindi della fibrosi durante l’infiammazione? Per scoprirlo, abbiamo usato un modello sperimentale nei topi. Abbiamo indotto un’infiammazione vescicale ricorrente utilizzando un farmaco chemioterapico, la ciclofosfamide (CYP). Questo farmaco, purtroppo noto per causare cistite emorragica come effetto collaterale, ci permette di mimare in laboratorio alcune caratteristiche dell’infiammazione cronica e della sindrome della vescica dolorosa/cistite interstiziale umana, inclusa la fibrosi.
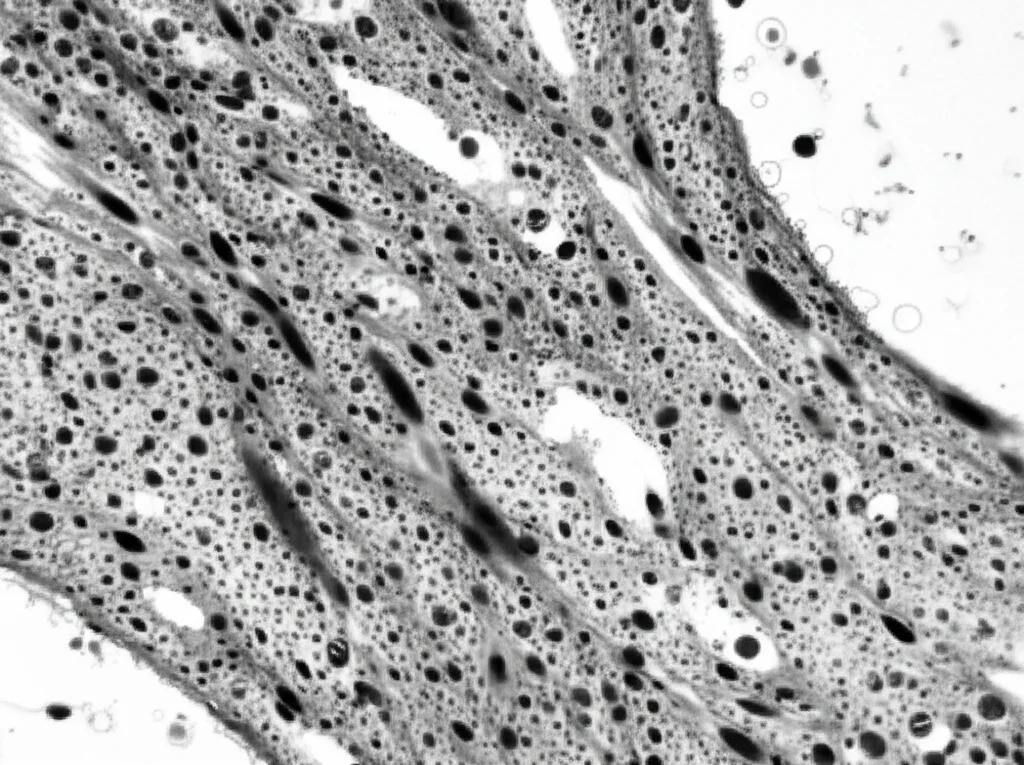
Le Prove si Accumulano: Le Cellule Suburoteliali Sotto i Riflettori
Analizzando i nostri topi modello, abbiamo fatto scoperte davvero illuminanti! Innanzitutto, abbiamo confermato che le cellule PDGFRα+ sono molto più abbondanti nella regione suburoteliale rispetto allo strato muscolare del detrusore. Ma non è solo una questione di numero. Analizzando l’espressione genica (cioè quali geni sono “accesi” o “spenti” in queste cellule), abbiamo visto che le cellule PDGFRα+ suburoteliali e quelle del detrusore hanno profili genetici distinti. Sono come due famiglie diverse che abitano nello stesso palazzo, ma con abitudini e compiti differenti.
E qui arriva il bello: le cellule PDGFRα+ suburoteliali esprimevano già di base livelli più alti di geni legati alla fibrosi (come quelli per il collagene – Col1a1, Col1a2 – e la fibronectina – Fn1, oltre a geni regolatori come Timp1e2, Tgfb2, Smad3) rispetto alle loro “cugine” del detrusore e alle altre cellule non-PDGFRα+. Erano, in un certo senso, già “predisposte” a diventare protagoniste della fibrosi.
L’Infiammazione Scatena la Trasformazione
Cosa è successo quando abbiamo trattato i topi con la ciclofosfamide (CYP)? Proprio quello che sospettavamo!
- Il numero di cellule PDGFRα+ suburoteliali è aumentato drasticamente.
- In queste cellule specifiche, l’espressione dei geni chiave della fibrosi, come Pdgfra stesso, Col1a1 (collagene di tipo 1) e Fn1 (fibronectina), è schizzata alle stelle.
- Abbiamo osservato un aumento significativo delle proteine tipiche della fibrosi: l’α-actina muscolare liscia (α-SMA) – un marcatore classico della trasformazione in miofibroblasti – il collagene e la fibronectina, proprio nella zona suburoteliale.
Era la prova che cercavamo: l’infiammazione indotta da CYP spingeva proprio le cellule PDGFRα+ suburoteliali a proliferare e a trasformarsi in miofibroblasti attivi, i veri costruttori della cicatrice fibrotica. Al contrario, nel muscolo detrusore, questi cambiamenti erano minimi o assenti.
Svelare il Meccanismo: Come Vengono Date le “Istruzioni” per la Fibrosi?
Ma come avviene questa trasformazione a livello molecolare? Sappiamo che durante l’infiammazione cronica, i livelli di due “messaggeri” pro-fibrotici, il TNF-α (Tumor Necrosis Factor-alpha) e il TGF-β (Transforming Growth Factor-beta), rimangono elevati. Queste molecole agiscono come interruttori, attivando specifiche vie di segnalazione all’interno delle cellule.
Abbiamo indagato proprio su queste vie. Il TNF-α attiva principalmente un fattore di trascrizione chiamato NF-κB, mentre il TGF-β attiva i fattori della famiglia Smad (in particolare SMAD2 e SMAD3). Normalmente, questi fattori se ne stanno buoni nel citoplasma della cellula. Ma quando arrivano i segnali da TNF-α e TGF-β, NF-κB e gli Smad si spostano nel nucleo cellulare. Una volta nel nucleo, agiscono come “direttori d’orchestra”, accendendo i geni responsabili della produzione di collagene, fibronectina e altre componenti della matrice extracellulare, oltre a promuovere la trasformazione in miofibroblasti.
Ebbene, nei nostri topi trattati con CYP, abbiamo osservato proprio questo:
- Nel citoplasma delle cellule della mucosa (dove risiedono le nostre cellule suburoteliali), i livelli di IκBα (un inibitore che trattiene NF-κB nel citoplasma) e di SMAD2/SMAD3 diminuivano.
- Contemporaneamente, nel nucleo, i livelli di NF-κB, SMAD2 e SMAD3 aumentavano significativamente!
Questo ci ha dato la conferma: l’infiammazione indotta da CYP attiva le vie di segnalazione del TNF-α e del TGF-β nelle cellule PDGFRα+ suburoteliali, spingendole verso il loro destino fibrotico.
Perché Questa Scoperta è Importante?
Identificare con precisione le cellule responsabili della fibrosi vescicale e i meccanismi molecolari che le guidano è un passo fondamentale. Capire che sono proprio le cellule PDGFRα+ suburoteliali le principali indiziate, e che rispondono ai segnali di TNF-α e TGF-β, apre nuove strade per lo sviluppo di terapie mirate.
In futuro, potremmo pensare a farmaci che blocchino selettivamente l’attivazione di queste cellule specifiche o che interferiscano con le vie di segnalazione di TNF-α e TGF-β nella vescica, senza magari intaccare altre funzioni importanti. L’obiettivo finale è quello di prevenire o addirittura invertire la fibrosi, migliorando così la funzione vescicale e alleviando i sintomi debilitanti che affliggono tanti pazienti con infiammazioni croniche o cistite interstiziale.
Il nostro viaggio nel mondo microscopico della vescica ci ha permesso di smascherare i “colpevoli” della fibrosi in questo modello. È un tassello importante nel grande puzzle della comprensione delle malattie vescicali, un passo avanti verso terapie più efficaci e personalizzate. La ricerca continua!
Fonte: Springer