Radioembolizzazione Epatica: La Mappa del Tesoro è Precisa? SPECT/CT vs PET/MRI
Ciao a tutti! Oggi voglio parlarvi di qualcosa di affascinante che sta cambiando il modo in cui affrontiamo i tumori al fegato: la radioembolizzazione transarteriosa (TARE). Immaginate di poter colpire i tumori dall’interno, usando minuscole sfere radioattive. Sembra fantascienza, vero? Eppure, è una realtà clinica sempre più diffusa.
I tumori al fegato, sia quelli primari come l’epatocarcinoma (HCC) o il colangiocarcinoma intraepatico (ICC), sia le metastasi da altri organi (colon-retto, mammella, polmone…), sono un bel problema. Sono tra i tumori più comuni e impattano pesantemente sulla sopravvivenza. Trovare modi efficaci per trattarli è cruciale.
Sfruttare la Vascolarizzazione Unica del Fegato
Qui entra in gioco una particolarità del fegato: mentre il tessuto sano riceve sangue principalmente dalla vena porta, i tumori si nutrono quasi esclusivamente dalle arterie epatiche. Questa differenza è la chiave della TARE. Possiamo iniettare delle microsfere caricate con un isotopo radioattivo, l’Ittrio-90 (Y-90), direttamente nelle arterie che irrorano il tumore. L’idea è semplice: concentrare una dose elevata di radiazioni proprio lì dove serve, risparmiando il più possibile il tessuto sano circostante. Geniale, no?
La Sfida della Pianificazione: La “Mappa” Pre-Trattamento
Ma come facciamo a sapere quanta radioattività iniettare? E come possiamo essere sicuri che le microsfere vadano davvero dove vogliamo? Qui le cose si fanno interessanti. Prima del trattamento vero e proprio, dobbiamo fare una sorta di “prova generale”. Si esegue un’angiografia per studiare l’anatomia vascolare del fegato e poi si inietta un tracciante, il Tecnezio-99m marcato con macroaggregati di albumina (Tc-99m MAA), seguito da un esame chiamato SPECT/CT.
L’assunto fondamentale è che queste particelle di MAA si distribuiscano in modo simile a come faranno poi le microsfere di Y-90. La SPECT/CT ci dà una “mappa” predittiva della distribuzione della dose. Usando questa mappa, calcoliamo la dose che arriverà al tumore e al tessuto sano, cercando di massimizzare l’efficacia sul primo e minimizzare la tossicità sul secondo. Esistono diversi metodi per farlo, ma quelli più moderni, detti “multicompartimentali”, considerano separatamente tumore e tessuto sano, permettendo calcoli più raffinati.
Tuttavia, c’è un “ma”… Le particelle di MAA e le microsfere di Y-90 (che possono essere di vetro o di resina, con caratteristiche diverse tra loro) non sono identiche. Differiscono per:
- Numero di particelle (molte di più quelle di resina rispetto a quelle di vetro)
- Attività per sfera
- Dimensioni (le MAA hanno un range più ampio)
- Stabilità (le MAA possono essere lentamente eliminate, le microsfere restano lì)
Queste differenze fisiche potrebbero far sì che la distribuzione reale delle microsfere non sia esattamente quella prevista dalla SPECT/CT con MAA. E qui nasce la domanda cruciale: quanto è affidabile la nostra mappa pre-trattamento?

La Verifica Post-Trattamento: Vedere Davvero Dove Vanno le Microsfere
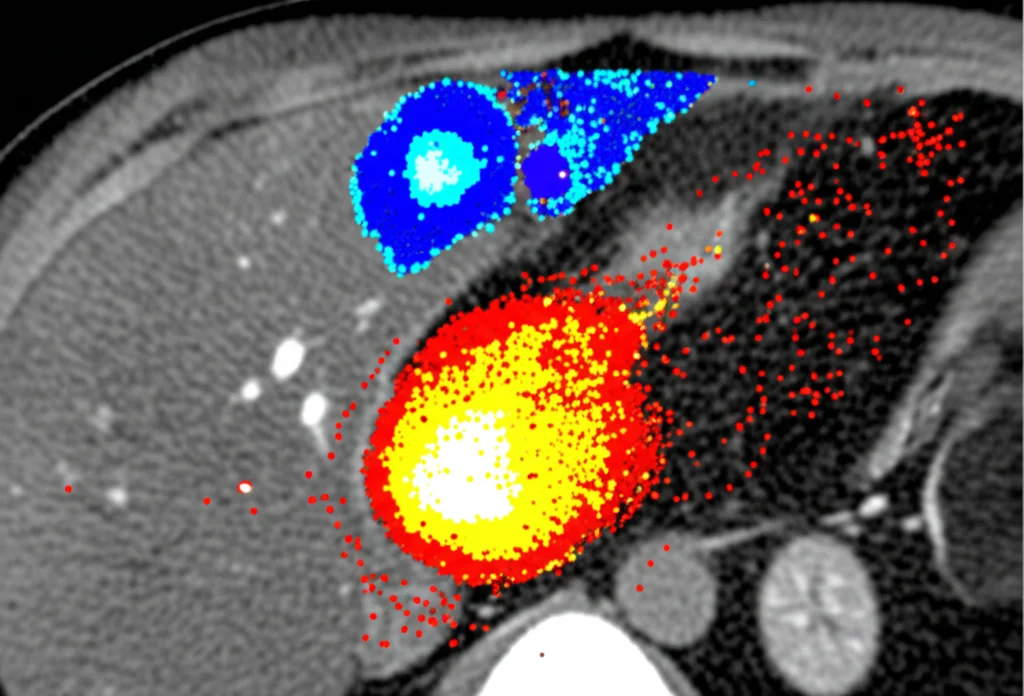
Fortunatamente, l’Y-90, pur essendo principalmente un emettitore beta (le particelle che fanno il “lavoro sporco” sul tumore), ha anche una piccolissima emissione di positroni. Questo ci permette di “vedere” dove sono andate a finire le microsfere dopo il trattamento, usando la PET (Tomografia a Emissione di Positroni). In questo studio specifico, abbiamo utilizzato un sistema ibrido PET/MRI (Risonanza Magnetica).
La PET/MRI è fantastica perché combina la sensibilità della PET nel rilevare la radioattività con l’eccezionale dettaglio anatomico e il contrasto dei tessuti molli della Risonanza Magnetica. Questo ci permette non solo di vedere la distribuzione delle microsfere, ma anche di delineare con grande precisione i tumori e il fegato sano, il tutto in un’unica sessione e con immagini perfettamente co-registrate. Potrebbe offrirci una dosimetria post-trattamento più accurata.
Il Confronto Diretto: SPECT/CT Predittiva vs PET/MRI Reale
Ed eccoci al cuore del nostro lavoro. Ci siamo chiesti: quanto sono diverse le dosi calcolate con la SPECT/CT pre-trattamento rispetto a quelle misurate con la PET/MRI post-trattamento? Non ci siamo limitati a guardare la dose media, ma abbiamo usato un approccio più sofisticato: la dosimetria voxel-based. In pratica, abbiamo analizzato la dose in ogni singolo “cubetto” (voxel) di tessuto, sia nel tumore che nel fegato sano. Questo ci permette di creare degli istogrammi dose-volume (DVH), grafici che mostrano quale percentuale di un certo volume (es. il tumore) riceve almeno una certa dose. È un modo molto più dettagliato per capire l’eterogeneità della distribuzione della dose.
Abbiamo analizzato i dati di 47 trattamenti (su 41 pazienti, alcuni ritrattati) eseguiti sia con microsfere di vetro che di resina. Abbiamo confrontato:
- La dose media assorbita dal tumore
- La dose media assorbita dal tessuto epatico sano (sia totale che solo quello perfuso dalle microsfere)
- Il rapporto tra dose al tumore e dose al tessuto sano normale (T/N ratio)
- Valori specifici degli DVH del tumore, come D10, D50 e D90 (la dose minima ricevuta rispettivamente dal 10%, 50% e 90% del volume tumorale).
Cosa Abbiamo Scoperto? Luci e Ombre della Predizione
I risultati sono stati illuminanti!
Per il tessuto epatico sano: Qui la SPECT/CT pre-trattamento se l’è cavata piuttosto bene! Le dosi medie predette per il fegato sano (sia totale che perfuso) erano molto simili a quelle misurate con la PET/MRI post-trattamento, con un’ottima correlazione statistica (valori di ICC, Intraclass Correlation Coefficient, alti, >0.87 per il tessuto perfuso e >0.92 per il fegato intero). Questo è fondamentale, perché la tossicità sul fegato sano è uno dei principali fattori limitanti della TARE. Sapere che possiamo prevederla con buona affidabilità ci dà sicurezza nella pianificazione.
Per il tumore e il T/N ratio: Qui le cose si sono complicate. La correlazione tra le dosi tumorali predette dalla SPECT/CT e quelle misurate dalla PET/MRI era solo moderata (ICC tra 0.73 e 0.77). Ancora più bassa la correlazione per il T/N ratio, specialmente con le microsfere di resina (ICC ~0.5). Abbiamo trovato differenze significative, soprattutto con le microsfere di vetro, tra la dose tumorale media predetta e quella effettiva. In generale, la SPECT/CT sembrava avere più difficoltà a prevedere con precisione quanta dose sarebbe arrivata al bersaglio tumorale.

Perché questa discrepanza? Le ragioni possono essere molteplici:
- La risoluzione inferiore della SPECT rispetto alla PET potrebbe “sfumare” i dettagli, specialmente nei tumori piccoli, rendendo difficile separare bene il segnale del tumore da quello del tessuto sano.
- L’uso di una TC a bassa dose nella SPECT/CT richiede una registrazione successiva con immagini diagnostiche migliori (RM o TC con contrasto), introducendo potenziali imprecisioni. La PET/MRI, invece, acquisisce tutto insieme.
- Le già citate differenze fisiche tra le particelle di MAA e le microsfere di Y-90.
- Fattori tecnici durante l’iniezione (posizione del catetere, velocità, possibile vasospasmo) che possono variare leggermente tra la simulazione con MAA e il trattamento reale.
Uno Sguardo più Profondo: Gli Istogrammi Dose-Volume (DVH)
Analizzando i DVH, abbiamo notato altre differenze interessanti.
Il valore D90 (la dose minima ricevuta dal 90% del tumore, un indicatore delle zone potenzialmente “sottodosate”) era più alto quando calcolato con la SPECT/CT rispetto alla PET/MRI. Questo suggerisce che la SPECT/CT potrebbe non riuscire a “vedere” piccole aree fredde (a bassa attività) all’interno del tumore, sovrastimando la copertura omogenea della dose.
Al contrario, il valore D10 (la dose minima ricevuta dal 10% più “caldo” del tumore) era più alto con la PET/MRI rispetto alla SPECT/CT. Questo potrebbe essere dovuto alla maggiore capacità della PET di rilevare “hot spot” (piccole aree ad altissima attività), forse legati a eterogeneità microscopiche nella distribuzione delle microsfere, o potenzialmente anche ad artefatti di ricostruzione dell’immagine PET data la bassa statistica di conteggio dell’Y-90.
Il valore D50 (dose mediana) non mostrava invece differenze significative tra le due metodiche.
Queste differenze nei DVH sono importanti perché suggeriscono che la SPECT/CT e la PET/MRI non solo danno valori medi diversi per il tumore, ma descrivono anche in modo differente l’eterogeneità della distribuzione della dose al suo interno. E sappiamo che questa eterogeneità può influenzare la risposta al trattamento: le zone fredde potrebbero essere quelle da cui il tumore ricresce.

Il Ruolo Cruciale della SPECT/CT e il Valore Aggiunto della PET/MRI
Quindi, cosa ci portiamo a casa da tutto questo? La SPECT/CT con Tc-99m MAA rimane uno strumento fondamentale e insostituibile nella pianificazione della TARE. La sua capacità di predire in modo affidabile la dose al fegato sano ci permette di personalizzare il trattamento in sicurezza, spingendo la dose al tumore il più possibile senza superare i limiti di tolleranza del tessuto sano.
Tuttavia, dobbiamo essere consapevoli dei suoi limiti nel predire con precisione la dose che arriverà effettivamente al tumore e la sua distribuzione interna. Qui entra in gioco la PET/MRI post-trattamento. Ci offre una visione molto più veritiera di ciò che è successo, permettendoci di:
- Verificare la dose effettivamente rilasciata.
- Studiare la relazione tra dose e risposta tumorale in modo più accurato.
- Potenzialmente, in futuro, usare queste informazioni per affinare ulteriormente le strategie di pianificazione o per guidare trattamenti successivi.
L’uso della PET/MRI, con la sua superiore risoluzione spaziale e il contrasto tissutale intrinseco, potrebbe rappresentare un passo avanti per una dosimetria post-radioembolizzazione ancora più precisa.
Certo, il nostro studio ha delle limitazioni (pazienti eterogenei, focus su trattamenti unilobari), e c’è ancora molto da ricercare, ad esempio esplorando metriche dosimetriche più avanzate come la Dose Biologicamente Effettiva (BED) o la Dose Uniforme Equivalente (EUD).
Ma la strada è tracciata: la combinazione di una pianificazione attenta basata sulla SPECT/CT e una verifica accurata con la PET/MRI ci avvicina sempre di più a una radioembolizzazione davvero personalizzata e ottimizzata per ogni paziente. La caccia al tesoro per colpire il tumore nel modo più preciso possibile continua, e abbiamo strumenti sempre più potenti per seguirne la mappa!
Fonte: Springer