Dieta Ricca di Grassi e Stress Cronico: Un Mix Esplosivo per Ansia e Depressione (e C’entrano gli Astrociti!)
Ragazzi, parliamoci chiaro: quanti di noi si sentono un po’ giù o più ansiosi del solito quando mangiano male per un po’ o sono sotto stress pesante? Credo parecchi. Ebbene, non è solo una sensazione campata in aria. C’è una scienza affascinante dietro, che collega direttamente quello che mettiamo nel piatto e lo stress che viviamo con quello che succede nel nostro cervello, fino a influenzare il nostro umore. Recentemente, mi sono imbattuto in uno studio che getta nuova luce proprio su questo legame, e devo dire che è piuttosto illuminante (e un po’ preoccupante!).
Obesità e Depressione: Un Circolo Vizioso?
Sappiamo da tempo che obesità e depressione spesso vanno a braccetto. Chi è obeso ha un rischio maggiore di sviluppare depressione, e viceversa. Ma *perché*? I meccanismi esatti sono ancora un po’ un mistero, anche se si sospettano cose come infiammazione cronica, problemi metabolici, e persino alterazioni del nostro asse intestino-cervello. Lo studio che ho letto ha cercato di scavare più a fondo, usando un modello che, secondo me, rispecchia molto bene la realtà di tante persone oggi: una combinazione di dieta ricca di grassi (pensate al cibo da fast food, snack ipercalorici…) e stress cronico.
L’Esperimento: Topi, Cibo Grasso e Stress
I ricercatori hanno preso dei topolini (i classici C57BL/6, per i più tecnici) e li hanno divisi in gruppi. Alcuni mangiavano normalmente, altri seguivano una dieta “high-fat” (HFD) per 8 settimane (l’equivalente di ingozzarsi di cibi grassi per noi!), altri ancora subivano uno stress cronico da costrizione (CRS) per 3 settimane (immaginatevi essere bloccati in uno spazio stretto per ore ogni giorno… non proprio una passeggiata). E poi c’era il gruppo “sfortunato”: quelli che si beccavano sia la dieta grassa *che* lo stress. L’idea era vedere come questa combinazione micidiale influenzasse comportamenti simili all’ansia e alla depressione.
Risultati Comportamentali: Un Quadro Preoccupante
E i risultati? Beh, come potevamo immaginare, non buoni. I topi sottoposti sia a HFD che a CRS mostravano segni evidenti di peggioramento:
- Meno piacere per le cose dolci: Nel test di preferenza per la saccarosio (un indicatore di anedonia, cioè l’incapacità di provare piacere), questi topi erano molto meno interessati all’acqua zuccherata rispetto agli altri. Un classico segno depressivo.
- Più “rassegnazione”: Nei test di nuoto forzato e sospensione per la coda (che misurano comportamenti simili alla disperazione), rimanevano immobili per più tempo.
- Più ansia: Nel test dell’open field, passavano meno tempo ad esplorare il centro dell’arena, preferendo rimanere rintanati lungo i bordi (un segno di ansia).
- Difficoltà di apprendimento e memoria: Nel labirinto acquatico di Morris (un test per la memoria spaziale), ci mettevano molto più tempo a imparare e ricordare dove fosse la piattaforma nascosta per mettersi in salvo.
Insomma, la combinazione di dieta grassa e stress cronico sembrava davvero esacerbare tutti questi comportamenti negativi, molto più di quanto facessero i singoli fattori da soli.

Ma Cosa Succede nel Cervello? Entrano in Scena gli Astrociti
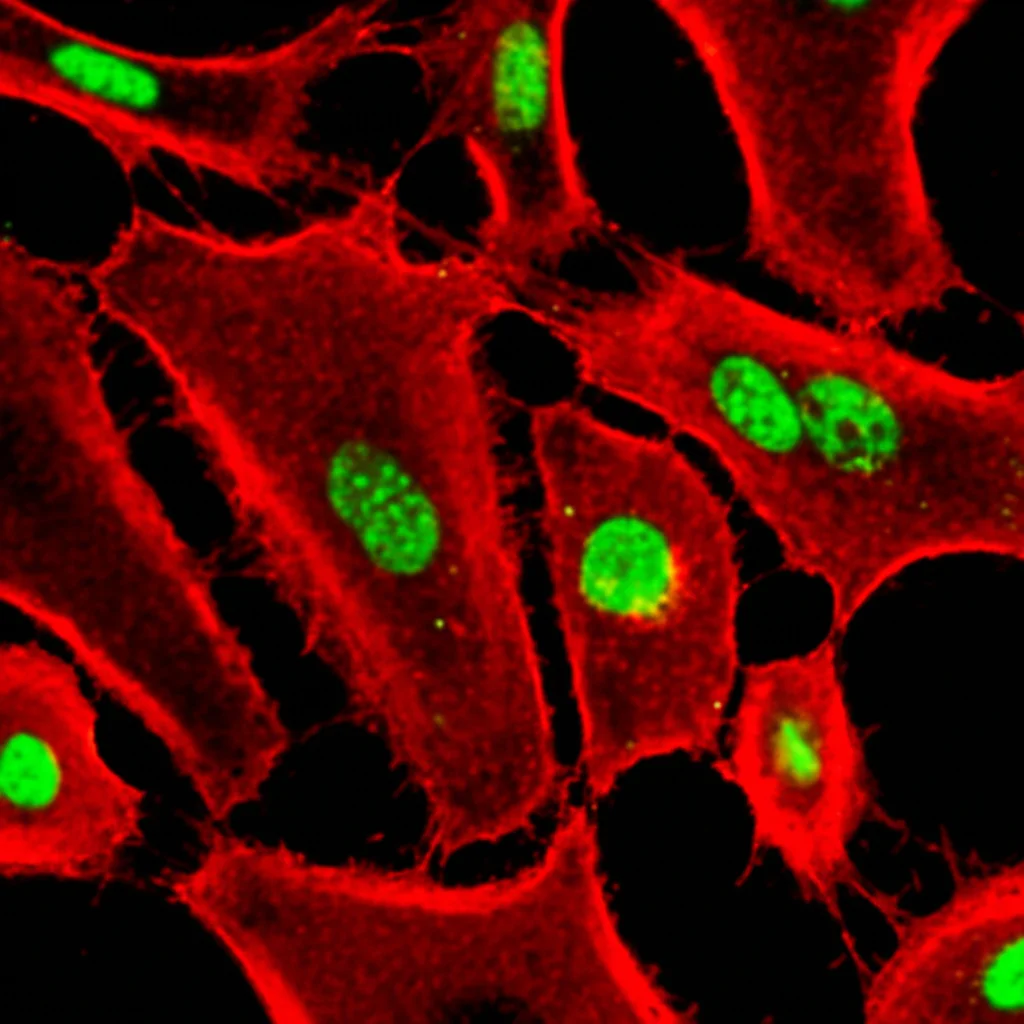
Qui la cosa si fa ancora più interessante. Gli scienziati non si sono fermati ai comportamenti, ma sono andati a vedere cosa succedeva a livello cellulare nel cervello, in particolare nell’ippocampo (un’area cruciale per memoria e umore). Hanno puntato i riflettori sugli astrociti. Non sono i neuroni “famosi”, ma cellule di supporto fondamentali, che però oggi sappiamo essere molto più attive e dinamiche di quanto pensassimo. Possono persino cambiare “personalità”!
Esistono principalmente due fenotipi di astrociti reattivi:
- Astrociti A1: Considerati “cattivi” o neurotossici. Producono sostanze infiammatorie che possono danneggiare le sinapsi e i neuroni.
- Astrociti A2: Considerati “buoni” o neuroprotettivi. Rilasciano fattori che aiutano la sopravvivenza e la riparazione neuronale.
E indovinate un po’? Nei topi HFD + CRS, i ricercatori hanno trovato un aumento massiccio di un marcatore specifico degli astrociti A1, la proteina C3. Addirittura, l’espressione di C3 nell’ippocampo di questi topi era tre volte superiore a quella dei topi di controllo! Allo stesso tempo, non c’erano cambiamenti significativi nei marcatori degli astrociti A2 (come S100A10). Questo suggerisce fortemente che la combinazione di dieta grassa e stress spinga gli astrociti a trasformarsi nel fenotipo “cattivo” A1. E c’era una correlazione diretta: più C3 c’era, peggiori erano i risultati nei test comportamentali.
Il Meccanismo Molecolare: La Via di Segnalazione Wnt/β-catenina
Ok, ma *come* avviene questa trasformazione? I ricercatori hanno indagato su una specifica via di comunicazione cellulare, chiamata Wnt/β-catenina. Questa via è importantissima per un sacco di processi biologici, inclusi sviluppo e plasticità neuronale, ed è già stata implicata nella depressione e nella differenziazione degli astrociti.
Hanno scoperto che nei topi HFD + CRS, l’attività della via Wnt/β-catenina era significativamente inibita. Meno Wnt3a, meno β-catenina attiva, meno fosforilazione di GSK3β (che sono tutti attori chiave di questa via).
Per confermare il tutto anche *in vitro* (cioè in laboratorio, su cellule coltivate), hanno usato cellule di astrociti (la linea C8-D1A) e le hanno trattate con acido palmitico (PA, per mimare la dieta grassa) e corticosterone (Cort, l’ormone dello stress, per mimare il CRS). I risultati? Esattamente gli stessi: PA + Cort aumentavano i marcatori degli astrociti A1 (C3 e GFAP, un altro marcatore generale di attivazione astrocitaria) e inibivano la via Wnt/β-catenina.
La Prova del Nove: Riattivare la Via Wnt Salva la Situazione?
A questo punto, la domanda sorge spontanea: se l’inibizione della via Wnt/β-catenina causa la trasformazione in astrociti A1 e peggiora i comportamenti, cosa succede se la *riattiviamo*?
Detto, fatto. Hanno preso i topi HFD + CRS e li hanno trattati con un farmaco chiamato SKL2001, che è un attivatore della via Wnt/β-catenina. I risultati sono stati notevoli!
- A livello cellulare (in vitro): Il trattamento con SKL2001 ha ridotto l’espressione dei marcatori A1 (C3 e GFAP) negli astrociti trattati con PA + Cort, pur non influenzando i marcatori A2. Ha anche aumentato l’attività della via Wnt (più Wnt3a e più β-catenina nel nucleo, segno di attivazione).
- A livello comportamentale (in vivo): I topi HFD + CRS trattati con SKL2001 hanno mostrato un netto miglioramento! Erano meno ansiosi, meno depressi (più interesse per il saccarosio, meno immobilità nei test di stress) e le loro capacità di apprendimento e memoria nel labirinto acquatico erano significativamente migliori rispetto ai topi HFD + CRS non trattati.
Cosa Ci Portiamo a Casa?
Questo studio, secondo me, è davvero importante. Ci dice che la combinazione, così comune oggi, di una dieta poco sana e ricca di grassi e dello stress cronico non solo ci fa sentire male, ma può letteralmente indurre cambiamenti fisici nel nostro cervello, spingendo gli astrociti verso uno stato pro-infiammatorio e neurotossico (A1). E lo fa, almeno in parte, “spegnendo” una via di segnalazione cruciale come la Wnt/β-catenina.
La buona notizia? Aver identificato questo meccanismo apre potenzialmente nuove strade terapeutiche. Agire sulla via Wnt/β-catenina potrebbe essere un modo per contrastare gli effetti negativi di dieta e stress sulla salute mentale, magari aiutando a prevenire o trattare ansia e depressione associate a questi fattori.
Certo, è uno studio su topi, e ci sono ancora cose da approfondire (differenze di genere, altri pathway coinvolti, marcatori metabolici sistemici, ecc.), come ammettono gli stessi autori. Ma ci dà un indizio potente su quanto il nostro stile di vita possa plasmare il nostro cervello a livello cellulare e molecolare, e su come potremmo intervenire in futuro. Nel frattempo, forse un motivo in più per cercare di mangiare meglio e gestire lo stress, no? Il nostro cervello (e i nostri astrociti!) potrebbero ringraziarci.

Fonte: Springer