CYR61: Un Turbo per i Vasi Sanguigni nella Guarigione delle Fratture?
Ciao a tutti! Oggi voglio parlarvi di qualcosa di affascinante che sta emergendo nel campo della riparazione ossea. Immaginate di rompervi un osso – un’esperienza non proprio piacevole, vero? La guarigione può essere un processo lungo e, a volte, complicato. Uno dei fattori chiave, spesso sottovalutato, è l’apporto di sangue alla zona fratturata. Senza un’adeguata rete di vasi sanguigni, le cellule responsabili della ricostruzione dell’osso faticano a ricevere ossigeno e nutrienti, e il rischio che la frattura non si saldi correttamente (quella che i medici chiamano pseudoartrosi) aumenta.
Ecco, è proprio qui che entra in gioco una proteina dal nome un po’ tecnico, ma dalle potenzialità intriganti: la CYR61 (o CCN1, se preferite). Pensate a lei come a un possibile “direttore dei lavori” specializzato nella costruzione di nuovi vasi sanguigni, un processo chiamato angiogenesi.
Il Problema: Ossa Rotte e Vasi Sanguigni “Pigri”
Quando un osso si rompe, il corpo avvia un complesso processo di riparazione. Le cellule che formano nuovo osso, gli osteoblasti, hanno bisogno di essere vicinissime ai vasi sanguigni per sopravvivere e lavorare al meglio. Inoltre, le cellule progenitrici, quelle che danno origine agli osteoblasti, arrivano sul “cantiere” della frattura proprio attraverso i vasi. Se questa rete vascolare è danneggiata o non si riforma abbastanza in fretta, tutto il processo rallenta o si blocca. Questo è un problema serio, specialmente in ossa con scarso apporto sanguigno periferico o in difetti ossei molto grandi, dove manca non solo l’osso ma anche la rete vascolare originale. Trovare un modo per stimolare la formazione di nuovi vasi (neovascolarizzazione) potrebbe davvero fare la differenza.
CYR61: Una Proteina al Centro dell’Attenzione
La ricerca ha iniziato a puntare i riflettori sulla CYR61. Si tratta di un fattore di crescita matricellulare, una molecola che interagisce con la matrice extracellulare (la “struttura” che circonda le cellule) e con le cellule stesse, in particolare quelle endoteliali che formano le pareti dei vasi sanguigni. Studi precedenti avevano già suggerito un suo ruolo nello sviluppo dello scheletro e nella riparazione delle fratture. Sappiamo anche che la sua espressione può essere influenzata dagli stimoli meccanici – il modo in cui l’osso viene caricato dopo la frattura. Curiosamente, la CYR61 è un bersaglio diretto di altre molecole (YAP/TAZ) che sono note per rispondere agli stimoli meccanici, ma che non possono essere usate direttamente come terapia perché legate anche allo sviluppo di tumori. Ecco perché la CYR61 diventa così interessante: potrebbe essere un mediatore più sicuro per ottenere effetti benefici.
Cosa Abbiamo Scoperto: Indagini in Laboratorio e nel Modello Animale
Per capirci di più, in questo studio abbiamo voluto fare due cose principali:
- Mappare dove si trova la CYR61 prodotta naturalmente dal corpo (endogena) durante la riparazione di una frattura.
- Valutare cosa succede se forniamo CYR61 extra (ricombinante) direttamente sulla frattura, soprattutto in relazione alla formazione di vasi e alla stabilità meccanica.
Per prima cosa, abbiamo osservato un modello di frattura del femore nei topi. Abbiamo visto che la CYR61 endogena si concentra soprattutto nel midollo osseo vicino alla frattura, proprio dove ci sono molti vasi sanguigni e dove è presente anche il suo “regista” molecolare, YAP. Nel callo cartilagineo, invece, la sua presenza era minore, anche se YAP era abbondante. Questo ci suggerisce che CYR61 potrebbe essere rilasciata nella matrice vicino ai vasi e rimanere lì anche quando l’attività di YAP diminuisce in quella specifica zona.
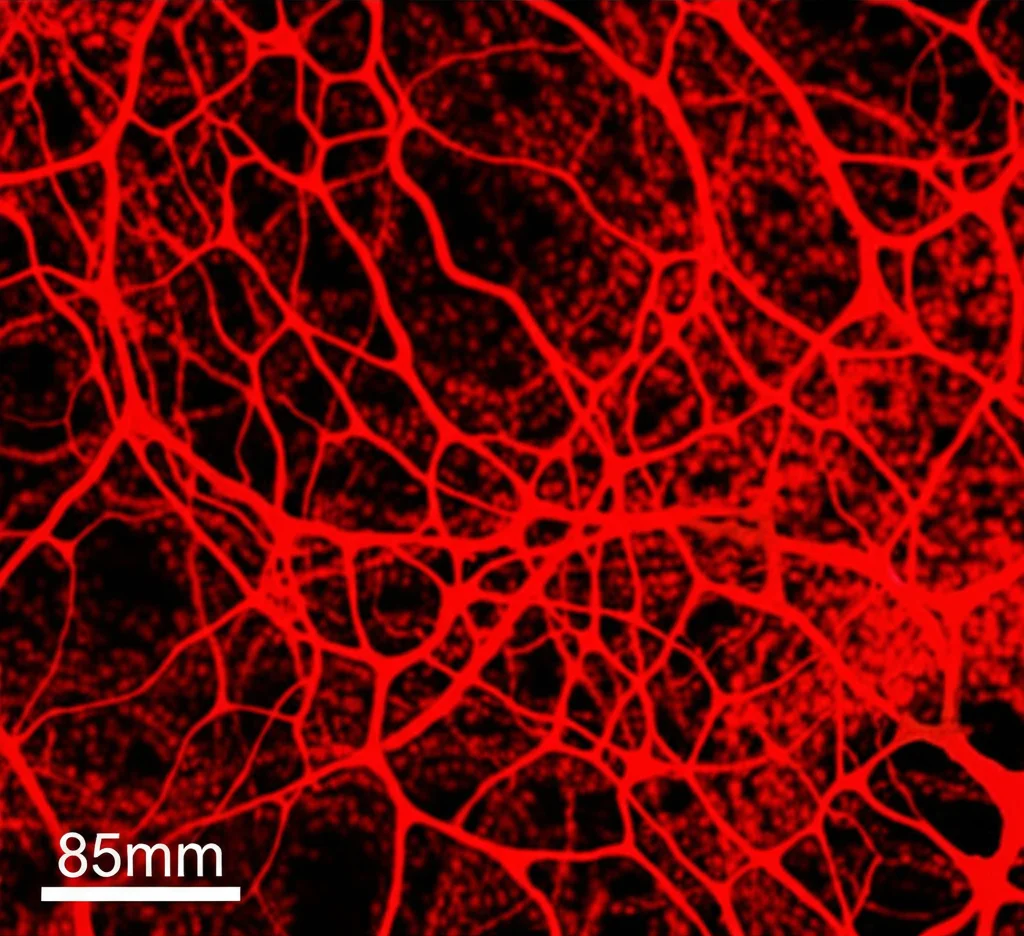
Poi siamo passati ai test in vitro, usando cellule umane in coltura. Abbiamo trattato cellule staminali mesenchimali (quelle che possono diventare osso o cartilagine) e cellule endoteliali (quelle dei vasi) con CYR61. I risultati? La CYR61 non ha mostrato grandi effetti nello stimolare la formazione di cartilagine (condrogenesi) o l’espressione di geni tipici della formazione ossea (osteogenesi). Ha avuto solo un piccolo effetto su un gene (RUNX2), ma non sugli altri marcatori chiave. Invece, l’effetto sull’angiogenesi è stato notevole! La CYR61 ha promosso significativamente la formazione di strutture tubulari simili a vasi sanguigni da parte delle cellule endoteliali, aumentandone la lunghezza e la maturità. Bingo! Sembra proprio che il suo “superpotere” sia legato ai vasi.
La Prova del Nove: CYR61 nella Frattura Reale (e la Sorpresa Meccanica)
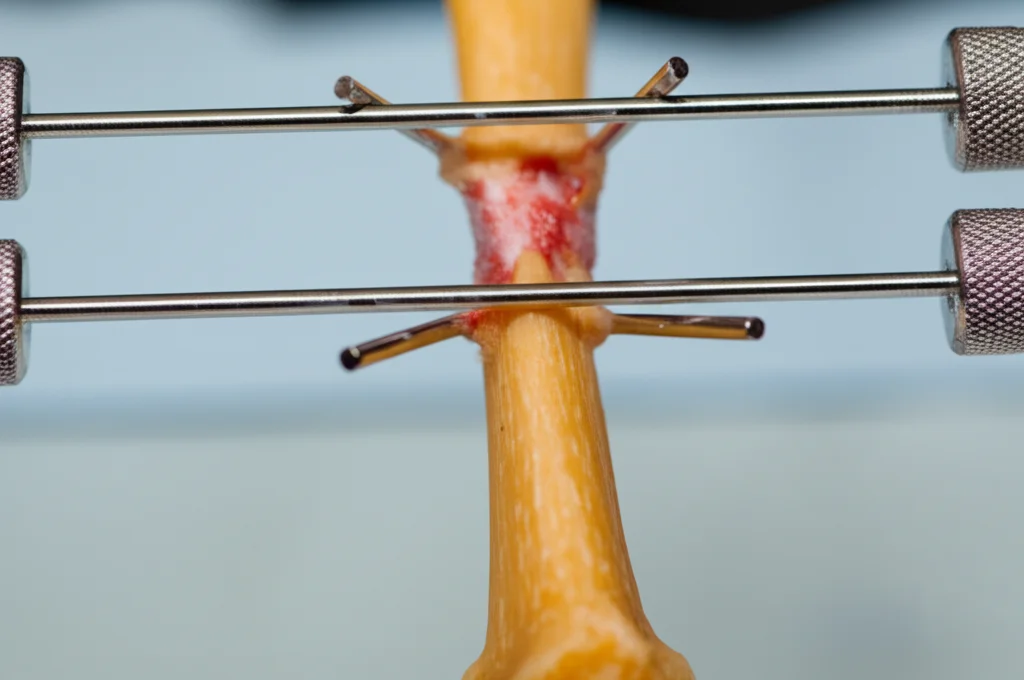
A questo punto, siamo tornati al nostro modello di frattura nel topo. Abbiamo applicato uno scaffold (una sorta di impalcatura biocompatibile fatta di GelMA/fibrina) caricato con CYR61 direttamente nel sito della frattura. Per rendere le cose più interessanti, abbiamo usato due tipi di fissazione esterna per stabilizzare la frattura: una molto rigida (che limita i movimenti) e una più “compliant” o flessibile (che permette un certo micro-movimento dovuto al carico dell’animale). Questo ci permette di studiare l’interazione tra CYR61 e l’ambiente meccanico.
I risultati a 14 giorni sono stati illuminanti. Proprio come in vitro, la somministrazione di CYR61 non ha aumentato significativamente la quantità di osso o cartilagine formata nel callo. Anzi, con la fissazione rigida, sembrava esserci un po’ più di tessuto fibroso. Ma l’effetto sui vasi sanguigni? Con la fissazione rigida, la CYR61 ha dato una bella spinta alla formazione di nuovi vasi (neovascolarizzazione) rispetto al controllo senza CYR61. Ma – ed ecco la sorpresa – con la fissazione compliant, questo effetto positivo svaniva! Sembra che il carico meccanico precoce, permesso dalla fissazione meno stabile, annulli i benefici pro-angiogenici della CYR61.
Il Carico Meccanico: Questione di Timing
Questo legame tra CYR61, angiogenesi e carico meccanico ci ha incuriosito molto. Sapevamo già da studi precedenti che il carico meccanico può sia ostacolare (se applicato troppo presto e con troppa intensità) sia favorire (se applicato più tardi) la formazione di vasi. Per approfondire, abbiamo usato un sistema avanzato in vitro chiamato “vascular network-on-a-chip”: una sorta di mini-rete vascolare coltivata su un microchip che permette di applicare un carico meccanico controllato (una compressione).
Abbiamo testato tre condizioni: nessun carico, carico applicato fin dall’inizio (giorno 0) e carico applicato in modo ritardato (dal giorno 4). In tutte le condizioni, abbiamo aggiunto CYR61 o un controllo. I risultati hanno confermato quanto visto nel topo:
- La CYR61 aumentava la lunghezza e l’area dei vasi in condizioni statiche (senza carico) e con carico ritardato.
- Il carico precoce disturbava la formazione della rete vascolare (aumentando le “terminazioni cieche” dei vasi).
- La CYR61 riusciva a contrastare questo effetto negativo del carico precoce, migliorando la connettività della rete. Tuttavia, l’effetto pro-angiogenico più forte si vedeva senza carico o con carico ritardato.

Cosa Ci Portiamo a Casa?
Tirando le somme, questo studio ci dice che la CYR61 è effettivamente una molecola pro-angiogenica potente, capace di stimolare la formazione di nuovi vasi sanguigni sia in vitro che durante la riparazione di una frattura in vivo. Tuttavia, non sembra avere un effetto diretto significativo sulla formazione di osso o cartilagine nelle condizioni testate.
La scoperta cruciale è che l’efficacia della CYR61 nel promuovere l’angiogenesi dipende fortemente dall’ambiente meccanico. Funziona al meglio quando la frattura è stabile (fissazione rigida) o quando il carico meccanico non è applicato troppo precocemente. Un carico precoce e instabile sembra annullare i suoi benefici vascolari.
Questo ha implicazioni importanti per le potenziali terapie. Somministrare CYR61 potrebbe essere una strategia promettente per migliorare la guarigione in fratture con problemi di vascolarizzazione (come alcune fratture della tibia o grandi difetti ossei), ma solo se associate a una fissazione stabile che crei un ambiente meccanico favorevole alla crescita dei vasi. Non è una bacchetta magica universale, ma uno strumento mirato che richiede di considerare attentamente le condizioni meccaniche della frattura.
Ovviamente, siamo ancora all’inizio. Serviranno ulteriori studi per capire come ottimizzare la somministrazione di CYR61 (magari legandola meglio alla matrice?) e per testarla in modelli di frattura più complessi e clinicamente rilevanti. Ma la strada è aperta, e la possibilità di dare un “turbo” ai vasi sanguigni per aiutare le ossa a guarire meglio è decisamente eccitante!
Fonte: Springer