Batteri con le Stanze Segrete: Come un Compartimento Senza Muri Controlla la Loro Pericolosità
Ciao a tutti! Oggi voglio raccontarvi una storia affascinante che arriva direttamente dal mondo microscopico dei batteri, un mondo che spesso immaginiamo come semplice, quasi un sacchetto pieno di roba. Beh, preparatevi a cambiare idea! Abbiamo scoperto qualcosa che assomiglia a delle vere e proprie “stanze” interne ai batteri, ma senza muri, che giocano un ruolo cruciale nel decidere quanto possano essere pericolosi per noi. Sembra fantascienza, vero? Eppure è scienza pura!
Un Mondo Nascosto Dentro i Batteri
Tutto è iniziato studiando batteri come l’*Escherichia coli* enteropatogeno (EPEC), uno di quei tipacci responsabili di brutte infezioni alimentari. Sapevamo già che questi batteri usano una specie di “siringa” molecolare, chiamata sistema di secrezione di tipo III (T3SS), per iniettare sostanze nelle nostre cellule e farci ammalare. La costruzione e l’uso di questa siringa sono controllati in modo super preciso. Tra i registi di questo processo c’è una proteina chiamata CsrA.
CsrA è un po’ un factotum: lega l’RNA messaggero (l’istruzione per costruire proteine) e, a seconda di dove si lega, può bloccare la produzione di una proteina o, al contrario, aiutarla stabilizzando l’RNA. Un vero e proprio controllore del traffico molecolare! La sua attività è a sua volta modulata da piccoli RNA regolatori, come CsrB e CsrC, che funzionano un po’ come delle spugne, “catturando” CsrA e impedendole di legarsi agli mRNA.
La Sorpresa: CsrA si Raggruppa!
Studiando CsrA in EPEC, abbiamo fatto una scoperta inaspettata. Usando tecniche di microscopia a fluorescenza (attaccando una proteina fluorescente verde, la GFP, a CsrA), abbiamo visto che CsrA non se ne stava sparsa a caso nella cellula. No, formava dei foci, dei puntini luminosi ben definiti, spesso uno solo per batterio, vicino al bordo della cellula. Era come se CsrA si riunisse in un punto specifico!
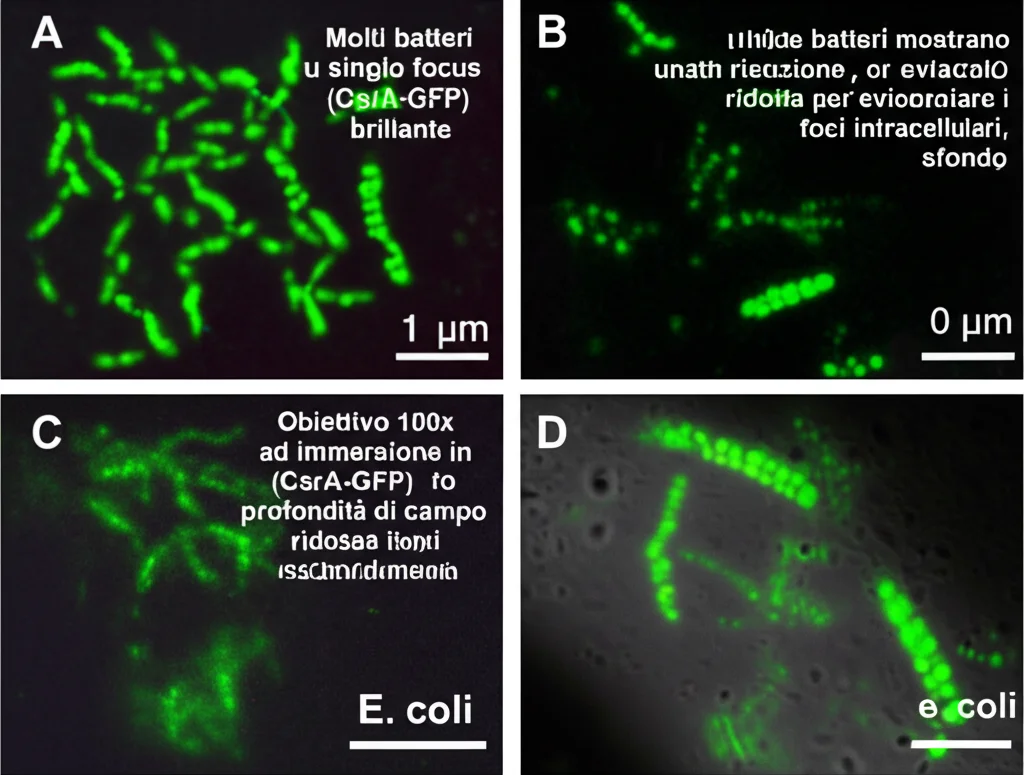
Ci siamo chiesti: è una cosa solo di EPEC? Abbiamo controllato altri batteri patogeni noti per usare CsrA per regolare la loro virulenza, come Salmonella, Citrobacter, Vibrio cholerae… e sorpresa! Anche in molti di loro CsrA formava questi foci. Quindi, non era un caso isolato, ma un fenomeno più diffuso. Era chiaro che avevamo per le mani qualcosa di importante.
Come Nasce un Focus? Il Ruolo Chiave dell’RNA
Ma come si formano questi aggregati? CsrA lavora in coppia (è un dimero) e ha due siti per legare l’RNA. La nostra ipotesi era che CsrA potesse fare da “ponte” tra diverse molecole di RNA che hanno più siti di legame, creando una sorta di rete che si condensa in un focus. Per verificarlo, abbiamo creato delle versioni mutate di CsrA incapaci di legare l’RNA. Risultato? Niente foci! Questo ci ha confermato che l’interazione tra CsrA e l’RNA è fondamentale per la formazione di questi compartimenti.
E quale RNA è il principale responsabile? I sospetti sono caduti subito su CsrB e CsrC, le “spugne” di CsrA, che hanno tantissimi siti di legame. Usando un’altra tecnica ingegnosa (etichettando CsrB e CsrC con un marcatore riconoscibile da un’altra proteina fluorescente), abbiamo visto che sì, sia CsrB che CsrC si trovavano proprio dentro i foci di CsrA. Anzi, eliminando il gene per CsrB, la formazione dei foci era fortemente compromessa, soprattutto nelle fasi iniziali della crescita batterica. Sembra proprio che CsrB sia il motore principale che guida l’assemblaggio di questi compartimenti.
Cosa C’è Dentro la “Stanza Segreta”?
Ok, dentro ci sono CsrA, CsrB e CsrC. Ma c’è altro? Per scoprirlo, abbiamo messo a punto un metodo per purificare questi foci intatti e analizzare il loro contenuto. È stato come aprire uno scrigno! Oltre ai componenti del sistema CSR (CsrA, CsrB, CsrC), abbiamo trovato in abbondanza le proteine del degradosoma. Il degradosoma è il complesso incaricato di degradare l’RNA nella cellula, una specie di centro di riciclaggio molecolare. La sua proteina chiave, la RNasi E, era una delle più abbondanti nei foci purificati.
Confermando con la microscopia, abbiamo visto che i foci di CsrA si formavano spesso proprio in corrispondenza di uno dei punti dove si localizza la RNasi E nella cellula. Questo suggerisce che questi foci non sono solo luoghi di accumulo, ma veri e propri centri di regolazione e forse anche di degradazione dell’RNA. Un hub super organizzato!
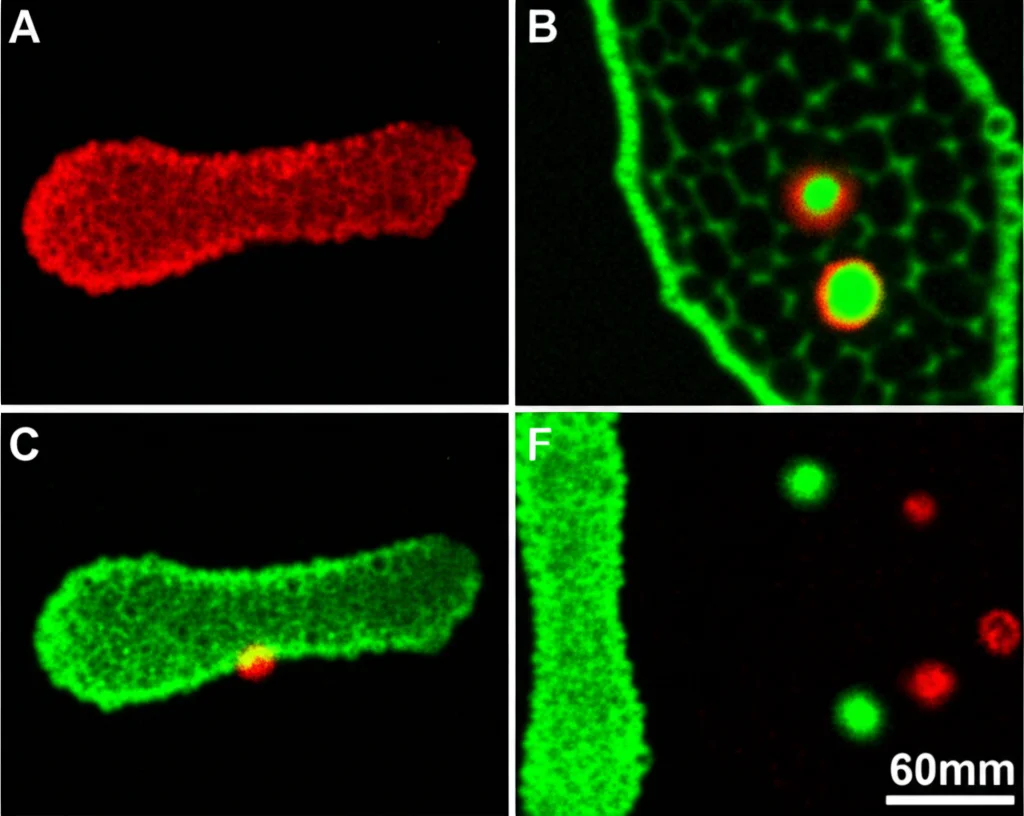
Abbiamo anche analizzato quali specifici mRNA venivano “intrappolati” nei foci. Oltre a CsrB e CsrC, abbiamo trovato diversi altri piccoli RNA regolatori e, soprattutto, mRNA che codificano per proteine coinvolte nel metabolismo, nell’acquisizione del ferro e… nella virulenza! In particolare, abbiamo trovato gli mRNA per i geni LEE1 e LEE7, che sono cruciali per attivare la produzione della famosa “siringa” T3SS.
L’Interruttore della Virulenza: Da Promotore a Repressore
Qui le cose si fanno davvero interessanti. Sappiamo che CsrA può sia promuovere che reprimere la virulenza. Come fa a decidere? La nostra scoperta dei foci ci ha dato la chiave.
- Fase iniziale (pochi batteri, pochi o piccoli foci): La concentrazione di CsrA nel citoplasma è relativamente bassa. È sufficiente per aiutare la produzione di alcune proteine essenziali della siringa T3SS (quelle codificate da LEE4), ma non abbastanza alta da bloccare la produzione di Ler (il regolatore chiave codificato da LEE1). Risultato: la virulenza è ACCESA. Il batterio si prepara all’attacco.
- Fase tardiva (tanti batteri, foci grandi e concentrati): Man mano che i batteri si moltiplicano, i foci crescono e la concentrazione di CsrA al loro interno aumenta molto. Gli mRNA di LEE1 e LEE7 vengono reclutati nei foci. Qui, l’alta concentrazione di CsrA riesce a bloccare la produzione di Ler. Senza Ler, l’intera produzione della siringa T3SS si ferma. Risultato: la virulenza è SPENTA. Il batterio, magari in attesa di condizioni migliori o non a contatto con le cellule ospiti, risparmia energia.
È un meccanismo geniale! Il batterio usa la formazione di questo compartimento senza membrana per “sentire” la propria densità e decidere quando è il momento giusto per essere aggressivo e quando invece è meglio stare tranquillo.
Il Doppio Gioco di CsrB
E c’è un’ultima sorpresa. CsrB, che di solito agisce come un antagonista di CsrA (sequestrandola), nel contesto del focus sembra cambiare ruolo. Quando abbiamo forzato la produzione di CsrB, ci aspettavamo che inibisse CsrA e quindi alleviasse la repressione su Ler. Invece, è successo il contrario! Più CsrB c’era, più forte era la repressione di Ler mediata da CsrA. Sembra che dentro al focus, CsrA e CsrB collaborino per spegnere la virulenza. Un doppio gioco inaspettato che sottolinea la complessità di questo hub regolatorio.
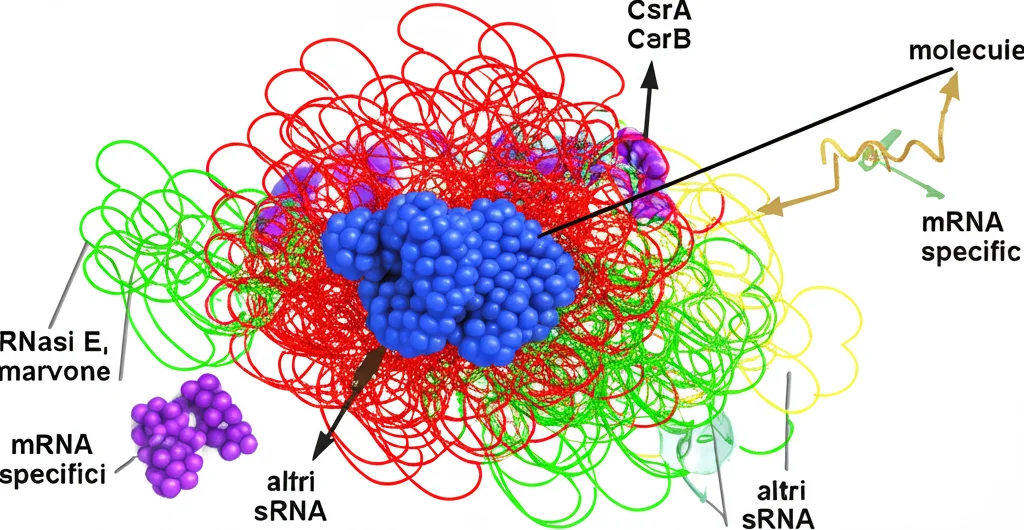
Il “CSRsome”: Una Strategia Diffusa?
Abbiamo chiamato questo compartimento regolatorio senza membrana “CSRsome“. Dato che il sistema CSR è presente in tantissimi batteri diversi e regola una miriade di processi (metabolismo, biofilm, virulenza…), pensiamo che la formazione di CSRsomi possa essere una strategia regolatoria molto diffusa nel regno batterico. Ogni batterio potrebbe aver adattato questo meccanismo alle proprie esigenze specifiche.
Questa scoperta apre una nuova finestra sulla biologia batterica, mostrandoci un livello di organizzazione interna che non sospettavamo. Capire come funzionano questi CSRsomi potrebbe darci nuove idee per combattere le infezioni batteriche, magari trovando modi per interferire con questo interruttore della virulenza.
Insomma, anche nel più piccolo dei batteri si nascondono meccanismi incredibilmente sofisticati e affascinanti. La prossima volta che penserete a un batterio, non immaginatelo come un semplice sacchetto, ma come una micro-città organizzata, con i suoi quartieri funzionali, anche senza bisogno di muri!
Fonte: Springer